Clear Sky Science · pl
Synteza i charakterystyka nanocząstek żelatynowych wrażliwych na NIR z kurkuminą do ukierunkowanego dostarczania leków w 3D raku jelita grubego
Przekształcenie przyprawy w inteligentnego przeciwnika raka
Wiele osób zna kurkuminę jako jasnożółty związek w kurkumie, powszechnej przyprawie kuchennej. Poza kulinarną sławą kurkumina potrafi hamować wzrost komórek nowotworowych w laboratorium. Problem w tym, że organizm słabo ją wchłania, a ona sama szybko się rozkłada. W tym badaniu naukowcy pokazują, jak przekształcili kurkuminę w „inteligentne” leczenie raka jelita grubego, zamykając ją w maleńkich cząstkach żelatynowych, które uwalniają ładunek leku po delikatnym ogrzaniu światłem bliskiej podczerwieni.
Dlaczego guzy jelita są trudne do leczenia
Rak jelita grubego pozostaje jednym z najczęstszych i najgroźniejszych nowotworów na świecie. Tradycyjne metody, takie jak operacja, chemioterapia i radioterapia, mogą ratować życie, ale często uszkadzają zdrowe tkanki i zawodzą, gdy guzy stają się oporne. Badacze szukają więc terapii, które skoncentrują działanie w obrębie guza, oszczędzając resztę organizmu. Zespół stojący za tą pracą skupił się na opracowaniu systemu lekowego reagującego na zewnętrzny bodziec — światło — tak by większość działania odbywała się tylko tam, gdzie jest potrzebna, wewnątrz lub blisko guza w jelicie.
Projektowanie maleńkich nośników z żelatyny
Naukowcy zbudowali swój system dostarczania z żelatyny, dobrze znanego materiału spożywczego i medycznego, który organizm może bezpiecznie rozłożyć. Rozpuszczoną żelatynę i kurkuminę wymieszano, a następnie za pomocą krótkich impulsów ultradźwięków utworzono nanocząstki — kulki tysiące razy mniejsze od ziarenka piasku. Poprzez staranne dostrojenie czasu mieszania i stosunku kurkuminy do żelatyny uzyskano stabilne cząstki o średnicy około 20–40 nanometrów, które zatrzymywały około dwóch trzecich dostępnej kurkuminy. Zespół testów fizycznych potwierdził rozmiar, strukturę i stabilność cząstek oraz zasugerował, że kurkumina jest utrzymywana głównie przez słabe siły fizyczne, a nie trwałe wiązania chemiczne, co ułatwia jej uwalnianie na żądanie. 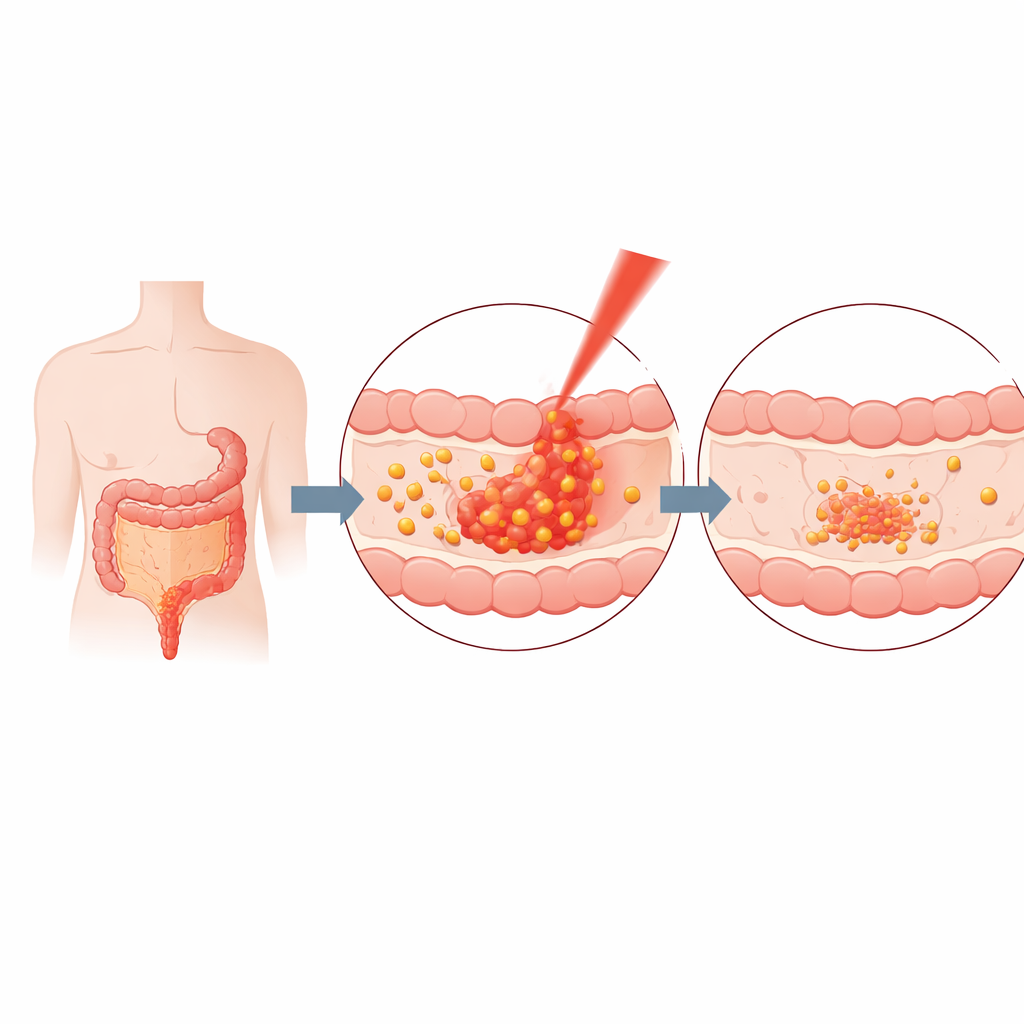
Użycie delikatnego ciepła jako włącznika
Następnie zespół zbadał, jak światło bliskiej podczerwieni (NIR) może działać jak pilot zdalnego sterowania uwalnianiem leku. Światło NIR, niewidoczne dla oka, przenika tkanki głębiej niż światło widzialne i jest już stosowane w niektórych urządzeniach medycznych. Gdy cząstki kurkumina–żelatyna były wystawione na działanie lampy na podczerwień, która ogrzała je do około 38 °C — nieco powyżej normalnej temperatury ciała — ich rozmiar zwiększał się, a kurkumina zaczynała szybciej się wydostawać. Przy tej łagodnej temperaturze uwolniona została około połowa załadowanego leku, a całkowite tempo uwalniania w czasie było nawet o jedną trzecią szybsze niż bez światła. Co ważne, efekt ten można było osiągnąć już po 30 sekundach naświetlania, co pokazuje szybki, czuły na temperaturę przełącznik uruchamiający uwalnianie leku. 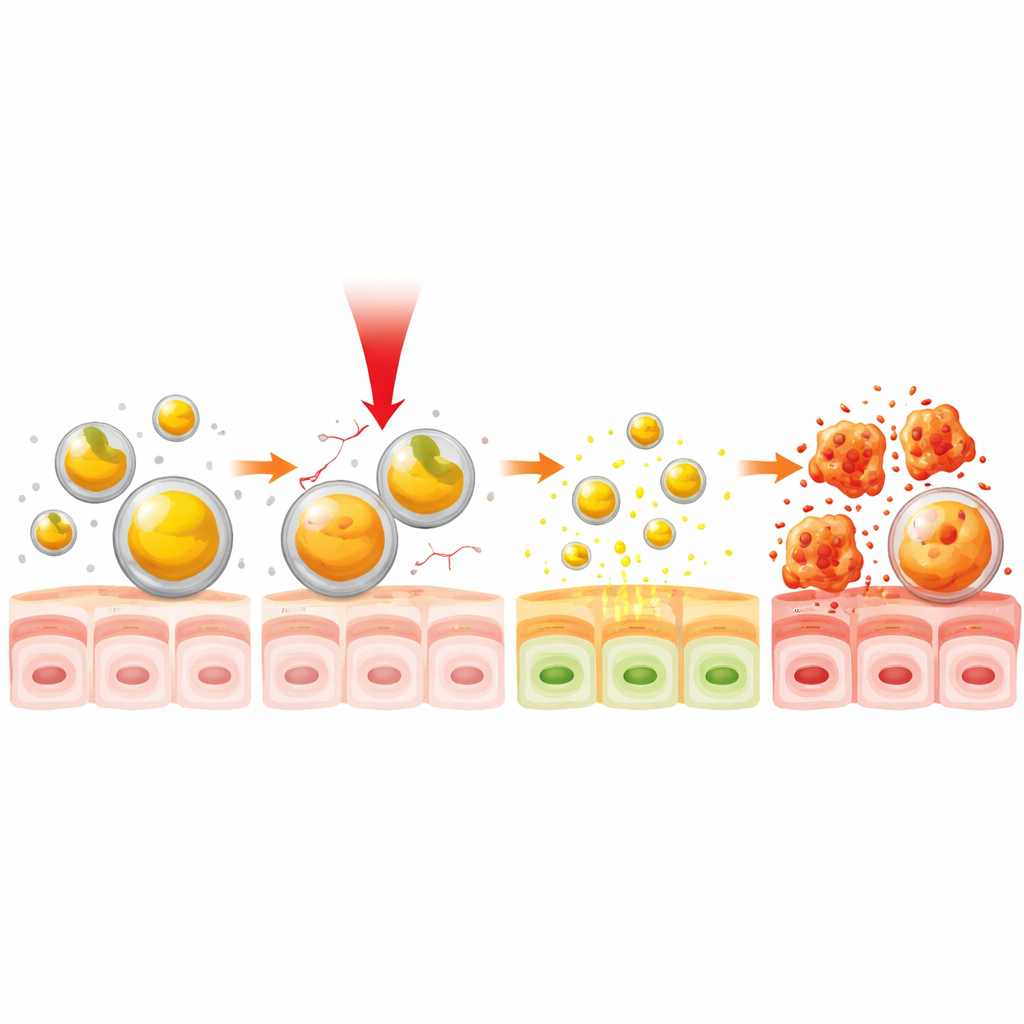
Testowanie systemu w modelach guza 2D i 3D
Aby sprawdzić, czy system aktywowany światłem rzeczywiście szkodzi komórkom nowotworowym, badacze przetestowali go na dwóch ludzkich liniach komórek raka jelita grubego oraz na zdrowych komórkach wyściełających naczynia krwionośne hodowanych w naczyniach. Zbudowali też bardziej realistyczny trójwymiarowy model, w którym komórki raka jelita rosły razem z komórkami śródbłonka, odtwarzając mini‑guz z jego towarzyszącymi naczyniami. Ponieważ kurkumina naturalnie świeci pod pewnym światłem, zespół mógł obserwować wejście nanocząstek do komórek i ich akumulację w cytoplazmie. Przy dawce odpowiadającej 25 mikrogramom kurkuminy na mililitr cząstki istotnie zmniejszały przeżywalność, ruchliwość i zdolność inwazji komórek nowotworowych, zwłaszcza w połączeniu z ogrzewaniem NIR. Dla porównania, zdrowe komórki były znacznie mniej dotknięte przy tych samych lub niższych dawkach, co sugeruje pewien stopień selektywności wobec tkanki nowotworowej.
Jak cząstki popychają komórki nowotworowe w stronę śmierci
Ponad samo liczenie żywych komórek, badacze sprawdzili, jak leczenie zmienia zachowanie komórek. Komórki nowotworowe wystawione na działanie cząstek kurkuminy aktywowanych NIR wykazały typowe oznaki kontrolowanej śmierci komórkowej, czyli apoptozy: kondensację DNA, fragmentację jąder oraz utratę normalnego potencjału elektrycznego i kurczenie się mitochondriów. W testach gojenia ran i Transwell mierzących tempo rozprzestrzeniania i inwazji, cząstki poddane NIR znacznie spowalniały migrację i inwazję komórek nowotworowych w porównaniu z cząstkami bez ekspozycji na światło. Zmiany te są zgodne ze znanymi właściwościami kurkuminy polegającymi na obniżaniu szkodliwych reaktywnych form tlenu i tłumieniu sygnałów zapalnych — szlaków, które sprzyjają wzrostowi i rozprzestrzenianiu się guzów.
Co to może oznaczać dla przyszłej opieki onkologicznej
Mówiąc prościej, praca ta przekształca aktywny składnik kurkumy w ukierunkowane, „zdalnie sterowane” leczenie przeciwnowotworowe. Ukrywając kurkuminę w biodegradowalnych kulkach żelatynowych i używając delikatnego ogrzewania bliską podczerwienią jako włącznika, badacze osiągnęli szybkie, kontrolowane uwalnianie leku i silne efekty przeciwnowotworowe w realistycznych modelach laboratoryjnych, przy jednoczesnym względnym oszczędzaniu zdrowych komórek. Chociaż potrzeba znacznie więcej badań na zwierzętach i ludziach, badanie wskazuje drogę do terapii raka jelita grubego, które mogą być bardziej precyzyjne, mniej toksyczne i potencjalnie łatwiejsze w produkcji, otwierając drzwi do mądrzejszych, prowadzonych światłem terapii opartych na bezpiecznych, naturalnych związkach.
Cytowanie: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
Słowa kluczowe: rak jelita grubego, kurkumina, nanocząstki, światło bliskiej podczerwieni, ukierunkowane dostarczanie leków