Clear Sky Science · tr
3B kolon kanserinde hedefe yönelik ilaç teslimi için NIR-duyarlı kurkumin-jelatin nanopartiküllerinin sentezi ve karakterizasyonu
Bir Baharatı Akıllı Bir Kanser Savaşçısına Dönüştürmek
Kurkumin, birçok kişinin mutfakta sıkça kullandığı zerdeçalın parlak sarı bileşiği olarak tanıdığı bir maddedir. Aşçılık alanındaki ününün ötesinde, kurkumin laboratuvarda kanser hücrelerinin büyümesini yavaşlatabiliyor. Sorun şu ki, vücut tarafından iyi emilmiyor ve hızla parçalanıyor. Bu çalışma, bilim insanlarının kurkumini, hafifçe ısıtarak yakın‑kızılötesi (NIR) ışıkla serbest bırakılan ilaç yükünü taşıyan küçük jelatin parçacıkları içine paketleyerek kolon kanseri için nasıl “akıllı” bir tedaviye dönüştürdüklerini gösteriyor.
Kolon Tümörlerinin Neden Tedavi Edilmesi Zor
Kolon kanseri dünya çapında en yaygın ve ölümcül kanserlerden biri olmaya devam ediyor. Cerrahi, kemoterapi ve radyasyon gibi geleneksel tedaviler hayat kurtarabiliyor ancak genellikle sağlıklı dokulara zarar verebiliyor ve tümörler direnç geliştirdiğinde başarısız olabiliyor. Bu nedenle araştırmacılar etkinliği tümörde yoğunlaştıran ve vücudun geri kalanını koruyan terapiler arıyor. Bu makalenin arkasındaki ekip, dışarıdan bir tetikleyici—ışık—ile yanıt veren bir ilaç sistemi oluşturmayı amaçladı, böylece çoğu etkinlik yalnızca ihtiyaç duyulan yerde, kolon içindeki veya yakınındaki tümörde gerçekleşir.
Küçük Jelatin Taşıyıcılar Tasarlamak
Bilim insanları teslimat sistemini, vücut tarafından güvenle parçalanabilen tanıdık bir gıda ve tıbbi malzeme olan jeletten inşa etti. Eritilmiş jelatin ile kurkumini karıştırdılar ve ardından nanopartiküller oluşturmak için kısa ultrasonik darbeler kullandılar—kum tanesinden binlerce kat daha küçük küreler. Karıştırma süresini ve kurkumin‑jelatin oranını dikkatle ayarlayarak yaklaşık 20–40 nanometre çapında, mevcut kurkuminin yaklaşık üçte ikisini yakalayan kararlı parçacıklar elde ettiler. Bir dizi fiziksel test parçacıkların boyutunu, yapısını ve stabilitesini doğruladı ve kurkuminin kalıcı kimyasal bağlardan ziyade zayıf fiziksel etkileşimlerle tutulduğunu, böylece talep üzerine serbest bırakılmasının daha kolay olduğunu gösterdi. 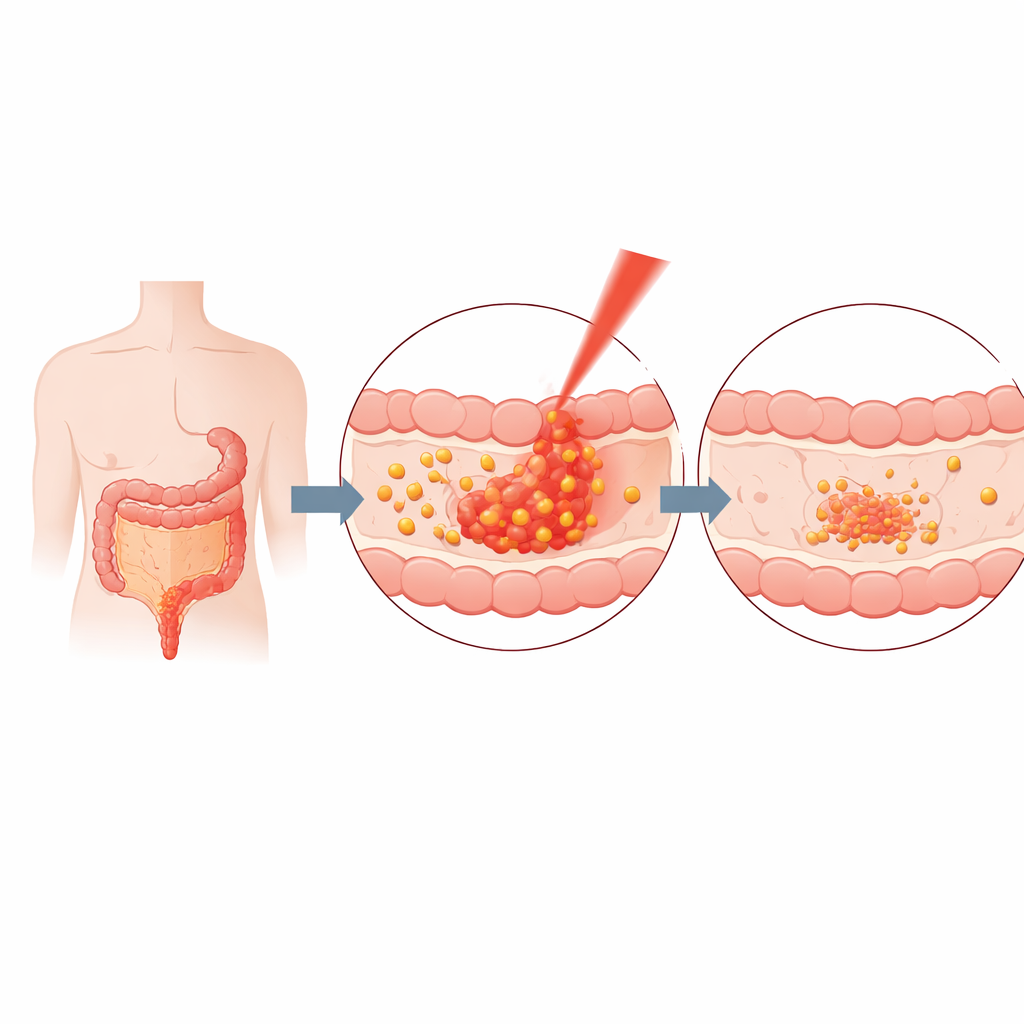
Hafif Isıyı Açma‑Kapatma Düğmesi Olarak Kullanmak
Sonraki adımda ekip, yakın‑kızılötesi (NIR) ışığın ilaç salımında uzaktan kumanda olarak nasıl kullanılabileceğini inceledi. Göze görünmeyen NIR ışığı, görünür ışıktan daha derin dokulara penetrasyon sağlayabilir ve bazı tıbbi cihazlarda zaten kullanılmaktadır. Kurkumin‑jelatin partikülleri yaklaşık 38 °C’ye—normal vücut sıcaklığının biraz üzeri—ısıtan bir kızılötesi lamba ile ışıklandırıldığında parçacıkların şiştiği ve kurkumini daha hızlı sızdırmaya başladığı gözlendi. Bu hafif sıcaklıkta, yakalanmış ilacın yaklaşık yarısı serbest kaldı ve zamana bağlı toplam salım ışık uygulanmayan duruma göre yüzde otuzlara kadar daha hızlı oldu. Önemli olarak, bu etki yalnızca 30 saniyelik aydınlatma ile sağlanabildi; bu da ilaç salımını açıp kapayan hızlı, sıcaklığa duyarlı bir anahtar olduğunu gösteriyor. 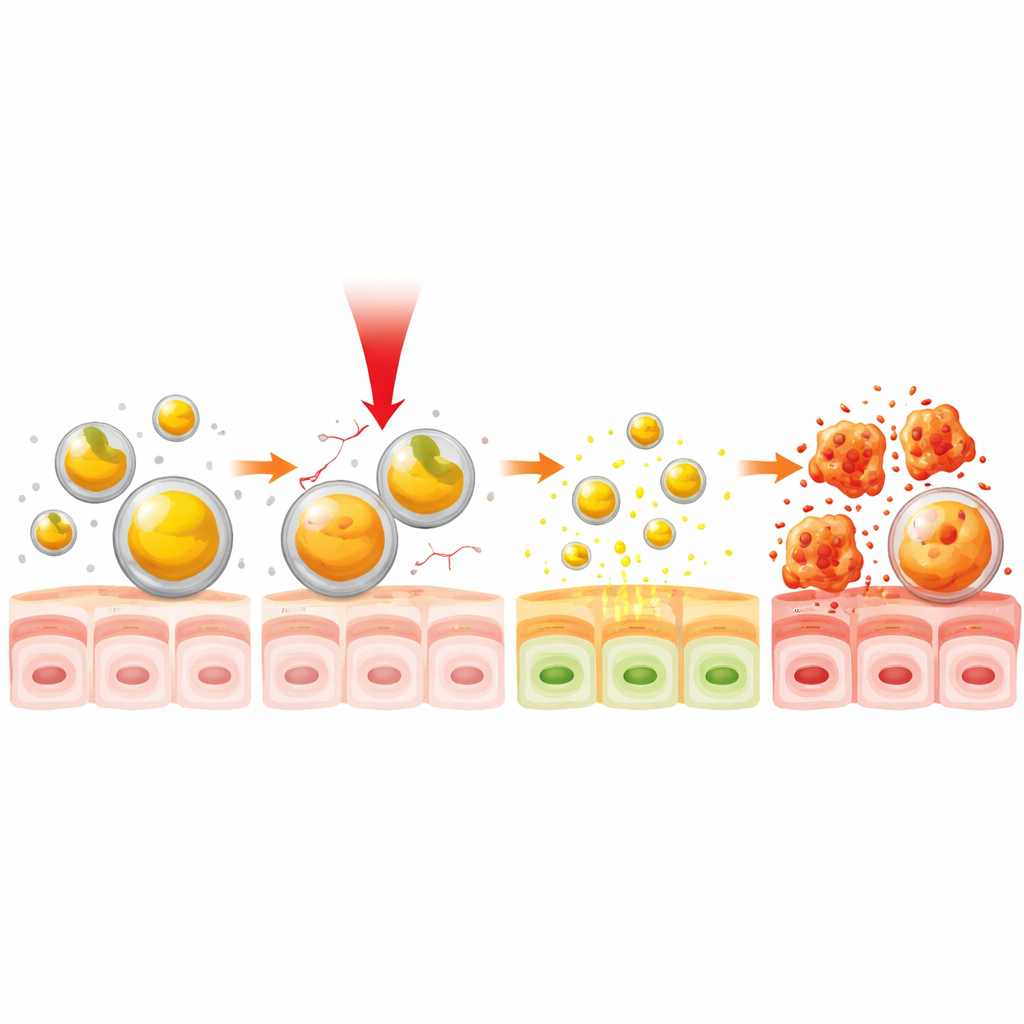
Sistemi 2B ve 3B Tümör Modellerinde Test Etmek
Bu ışıkla aktive edilen sistemin gerçekten kanser hücrelerine zarar verip vermediğini görmek için araştırmacılar iki insan kolon kanseri hücre hattı ve kültürlerde büyütülen sağlıklı damar hücreleri üzerinde test yaptılar. Ayrıca kolon kanseri hücrelerinin endotel hücreleriyle birlikte büyüdüğü, destekleyici kan damarlarını taklit eden daha gerçekçi üç boyutlu bir mini‑tümör modeli oluşturdular. Kurkumin belirli ışık altında doğal olarak floresan verdiği için ekip nanopartiküllerin hücrelere girmesini ve hücre sıvısında birikmesini izleyebildi. Kurkumin eşdeğeri dozu 25 mikrogram/mililitre olduğunda parçacıklar, özellikle NIR ısıtma ile kombinasyon halinde, kanser hücresi hayatta kalmasını, hareketini ve istila yeteneğini anlamlı şekilde azalttı. Buna karşılık, aynı veya daha düşük dozlarda sağlıklı hücreler çok daha az etkilendi; bu da doku açısından belirli bir seçicilik olduğunu düşündürüyor.
Partiküller Kanser Hücrelerini Ölüm Yönünde Nasıl İter
Yalnızca yaşayan hücreleri saymanın ötesinde, araştırmacılar tedavinin hücre davranışını nasıl değiştirdiğini incelediler. NIR ile aktive edilmiş kurkumin partiküllerine maruz kalan kanser hücreleri, kontrollü hücre ölümü yani apoptozun klasik işaretlerini gösterdi: DNA’ları yoğunlaştı, çekirdekleri parçalandı ve enerji üreten mitokondriler normal elektrik yüklerini kaybedip küçüldü. Hücrelerin yayılma ve istila hızını ölçen yara‑iyileşme ve Transwell testlerinde, NIR ile muamele edilmiş parçacıklar kanser hücresi göçünü ve invazyonunu ışık uygulanmamış parçacıklardan çok daha fazla yavaşlattı. Bu değişiklikler, kurkuminin zararlı reaktif oksijen moleküllerini azaltma ve tümör büyümesini ve yayılmasını destekleyen iltihap sinyallerini yatıştırma bilinen yeteneğiyle tutarlıdır.
Geleceğin Kanser Bakımı İçin Anlamı Ne Olabilir
Basitçe söylemek gerekirse, bu çalışma zerdeçalın aktif bileşenini hedefe yönelik, “uzaktan kontrollü” bir kanser tedavisine dönüştürüyor. Kurkumini biyobozunur jelatin küreleri içine gizleyip hafif yakın‑kızılötesi ısıtmayı açma‑kapama anahtarı olarak kullanarak araştırmacılar gerçekçi laboratuvar modellerinde hızlı, kontrollü ilaç salımı ve güçlü anti‑tümör etkiler elde etti; aynı zamanda sağlıklı hücreleri büyük ölçüde korudu. Hayvanlar ve insanlarda çok daha fazla test gerekse de, çalışma daha hassas, daha az toksik ve potansiyel olarak üretimi daha kolay kolon kanseri tedavilerine giden bir yol öneriyor; güvenli, doğal bileşiklere dayanan, ışıkla yönlendirilen daha akıllı tedavilere kapı aralıyor.
Atıf: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
Anahtar kelimeler: kolon kanseri, kurkumin, nanopartiküller, yakın kızılötesi ışık, hedefe yönelik ilaç taşıma