Clear Sky Science · ar
تخليق وتوصيف جسيمات نانوية من الكركمين والجلاتين حساسة للأشعة تحت الحمراء القريبة لتوصيل دوائي مستهدف في سرطان القولون ثلاثي الأبعاد
تحويل بهار إلى مقاتل ذكِي ضد السرطان
يعرف الكثيرون الكركمين على أنه المركب الأصفر الزاهي في الكركم، ذلك التوابل الشائعة في المطبخ. إلى جانب شهرته الطهوية، يستطيع الكركمين إبطاء نمو خلايا السرطان في المختبر. المشكلة هي أن أجسامنا تمتصه بشكل سيئ، وينحل بسرعة. تُظهر هذه الدراسة كيف حوّل العلماء الكركمين إلى علاج «ذكي» لسرطان القولون عن طريق تعبئته داخل جسيمات صغيرة من الجلاتين تطلق حمولتها الدوائية عند تسخينها بلطف بواسطة ضوء قريب من الأشعة تحت الحمراء.
لماذا يصعب علاج أورام القولون
لا يزال سرطان القولون من أكثر السرطانات شيوعًا وفتكًا على مستوى العالم. قد تنقذ العلاجات التقليدية مثل الجراحة والعلاج الكيميائي والإشعاعي الأرواح لكنها غالبًا ما تضر الأنسجة السليمة وقد تفشل عندما تصبح الأورام مقاومة. لذلك يسعى الباحثون إلى علاجات تركز تأثيرها داخل الأورام مع الحفاظ على باقي الجسم. ركز فريق هذه الورقة على بناء نظام دوائي يستجيب لمحفز خارجي—الضوء—حتى تجري معظم الفعالية فقط حيث يُحتاج إليها، داخل الورم أو بالقرب منه في القولون.
تصميم حوامل صغيرة من الجلاتين
بنَى العلماء نظام التوصيل من الجلاتين، وهو مادة غذائية وطبية مألوفة يمكن للجسم تحللها بأمان. مزجوا جلاتينًا مذابًا مع الكركمين، ثم استخدموا دفعات قصيرة من الموجات فوق الصوتية لتشكيل جسيمات نانوية—كرات أصغر آلاف المرات من حبة رمل. وعن طريق ضبط وقت الخلط ونسبة الكركمين إلى الجلاتين بعناية، حصلوا على جسيمات ثابتة بحجم نحو 20–40 نانومتر تحجز نحو ثلثي الكركمين المتاح. أكدت سلسلة اختبارات فيزيائية حجم الجسيمات وبنيتها واستقرارها، وأشارت إلى أن الكركمين محتجز في الأساس بقوى فيزيائية ضعيفة بدلًا من روابط كيميائية دائمة، مما يجعل إطلاقه أسهل عند الطلب. 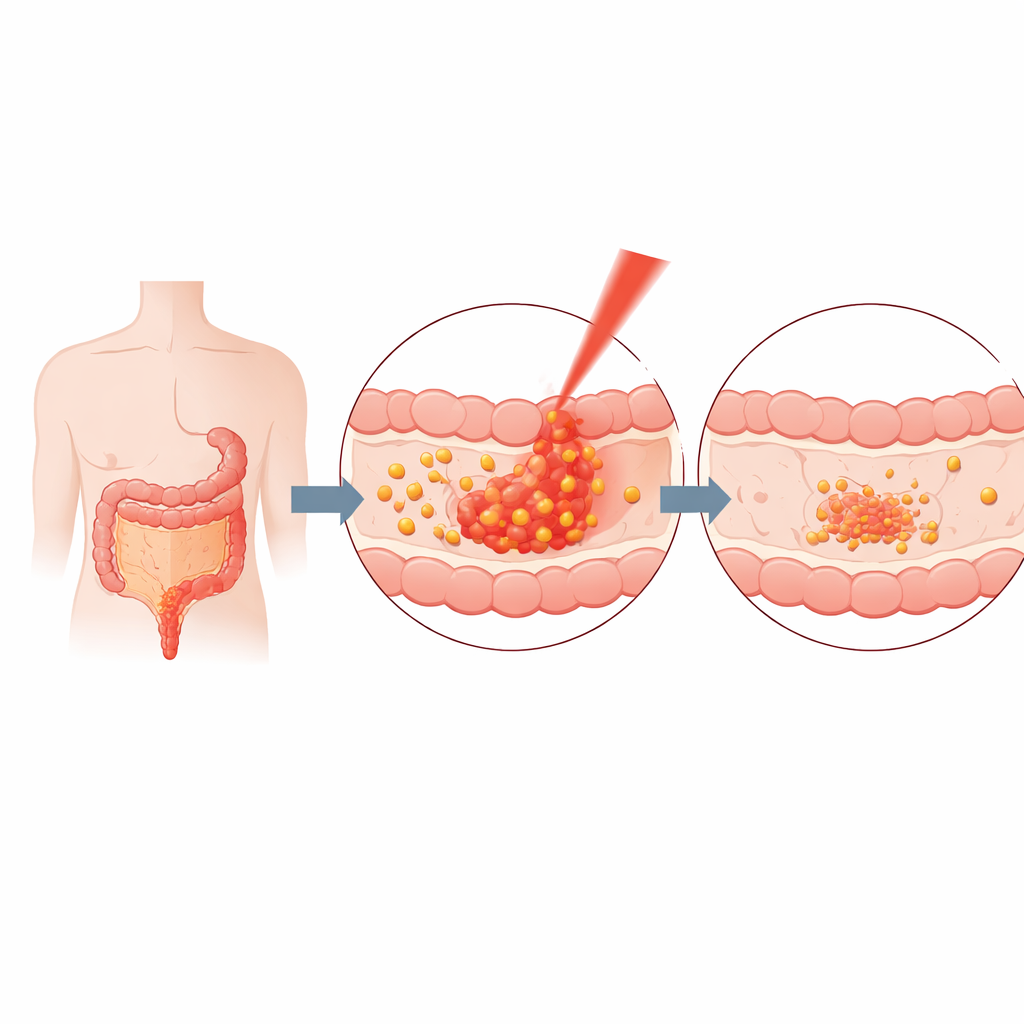
استخدام حرارة لطيفة كمفتاح تشغيل/إيقاف
بعد ذلك استكشف الفريق كيف يمكن للضوء القريب من الأشعة تحت الحمراء أن يعمل كتحكم عن بُعد لإطلاق الدواء. الضوء القريب من تحت الحمراء، غير المرئي للعين، يمكنه اختراق الأنسجة أعمق من الضوء المرئي ويُستخدم بالفعل في بعض الأجهزة الطبية. عندما تعرّضت جسيمات الكركمين–الجلاتين لمصباح تحت أحمر دفأها إلى نحو 38 °م—قليلًا أعلى من درجة حرارة الجسم الطبيعية—تضخمت أحجامها وبدأت تسرب الكركمين بسرعة أكبر. عند هذه الحرارة المعتدلة أُطلق نحو نصف الدواء المحتجز، وكان معدل الإفراج العام مع مرور الزمن أسرع لما يقارب ثلث أثناء التعرض للضوء مقارنةً بعدم التعرض. والأهم أن هذا التأثير تحقق خلال 30 ثانية فقط من الإضاءة، مما يبرهن على وجود مفتاح حساس لدرجة الحرارة لتشغيل إطلاق الدواء بسرعة. 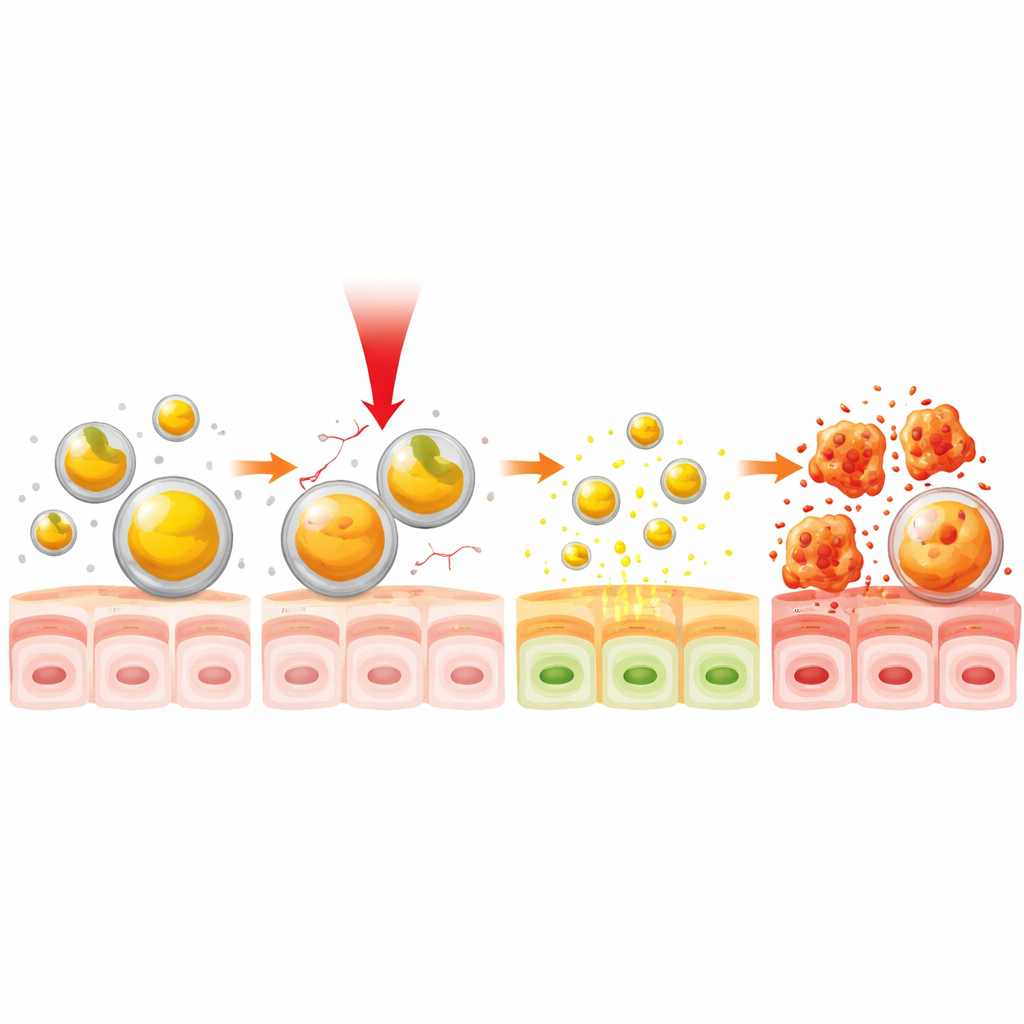
اختبار النظام في نماذج أورام ثنائية وثلاثية الأبعاد
للسؤال عمّا إذا كان هذا النظام المحفَّز بالضوء يضر خلايا السرطان فعلاً، اختبر الباحثون النظام على خطيْن بشرييْن لخلايا سرطان القولون وخلايا الأوعية الدموية السليمة المزروعة في أطباق. كما بنوا نموذجًا ثلاثي الأبعاد أكثر واقعية نما فيه خلايا سرطان القولون مع خلايا بطانية للأوعية، محاكيًا ورمًا مصغرًا مع أوعيته الداعمة. لأن الكركمين يفلِئ طبيعيًا تحت إضاءة معينة، تمكن الفريق من مراقبة دخول الجسيمات إلى الخلايا وتراكمها في سائِل الخلية. عند جرعة مكافئة للكركمين مقدارها 25 ميكروغرام لكل مليلتر، قللت الجسيمات بشكل كبير من بقاء خلايا السرطان وحركتها وغزوها، خاصة عند الجمع مع التسخين القريب من الأشعة تحت الحمراء. بالمقابل، تأثرت الخلايا السليمة أقل بكثير عند نفس الجرعات أو جرعات أقل، مما يشير إلى درجة من الانتقائية نحو نسيج الورم.
كيف تدفع الجسيمات خلايا السرطان نحو الموت
بعيدًا عن مجرد عد الخلايا الحية، فحص الباحثون كيف تغيّر المعالجة سلوك الخلايا. أظهرت خلايا السرطان المعالجة بجسيمات الكركمين المنشط بالضوء أدلة كلاسيكية على الموت الخلوي المبرمج، أو الاستماتة: تكثّفت الحمض النووي داخلها، تشظت نواتها، وفقدت الميتوكوندريا المنتجة للطاقة شحنتها الكهربائية الطبيعية وانكمشت. في اختبارات شفاء الجروح وTranswell التي تقيس سرعة انتشار الخلايا وغزوها، أبطأت الجسيمات المعالجة بالضوء هجرة وغزو خلايا السرطان أكثر بكثير من الجسيمات غير المعالجة بالضوء. تتوافق هذه التغيرات مع قدرة الكركمين المعروفة على خفض جزيئات الأكسجين التفاعلية الضارة وتهدئة إشارات الالتهاب، المسارات التي تساعد الأورام على النمو والانتشار.
ماذا قد يعني هذا لرعاية السرطان المستقبلية
بعبارة بسيطة، تحول هذه الدراسة المكوّن الفعّال في الكركم إلى علاج سرطاني مستهدف «يمكن التحكم فيه عن بُعد». عبر إخفاء الكركمين داخل كرات جلاتين قابلة للتحلل واستخدام تسخين لطيف بالأشعة تحت الحمراء القريبة كمفتاح تشغيل/إيقاف، حقق الباحثون إطلاقًا سريعًا ومتحكمًا للدواء وتأثيرات قوية مضادة للأورام في نماذج مخبرية واقعية، مع الحفاظ إلى حد كبير على سلامة الخلايا السليمة. وعلى الرغم من الحاجة لمزيد من الاختبارات في الحيوانات والبشر، تشير الدراسة إلى مسار لعلاجات سرطان القولون أكثر دقة وأقل سمية وربما أسهل تصنيعًا، فاتحة الباب لعلاجات أذكى موجهة بالضوء ومستندة إلى مركبات طبيعية وآمنة.
الاستشهاد: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
الكلمات المفتاحية: سرطان القولون, الكركمين, جسيمات نانوية, الضوء القريب من الأشعة تحت الحمراء, توصيل دوائي مستهدف