Clear Sky Science · de
Synthese und Charakterisierung von NIR-empfindlichen Curcumin-Gelatine-Nanopartikeln für gezielte Wirkstofffreisetzung in 3D-Darmkrebsmodellen
Aus einem Gewürz wird ein intelligenter Krebsbekämpfer
Viele kennen Curcumin als den leuchtend gelben Bestandteil von Kurkuma, einem gebräuchlichen Küchengewürz. Über seine kulinarische Bekanntheit hinaus kann Curcumin im Labor das Wachstum von Krebszellen verlangsamen. Das Problem ist, dass der Körper es schlecht aufnimmt und es schnell abgebaut wird. Diese Studie zeigt, wie Wissenschaftler Curcumin in eine „intelligente“ Behandlung für Darmkrebs verwandelt haben, indem sie es in winzige Gelatinepartikel verpackten, die ihre Wirkstoffladung bei leichter Erwärmung durch nahes Infrarotlicht freisetzen.
Warum Tumoren im Dickdarm schwer zu behandeln sind
Darmkrebs bleibt eine der weltweit häufigsten und tödlichsten Krebserkrankungen. Traditionelle Behandlungen wie Operation, Chemotherapie und Strahlentherapie können Leben retten, schädigen jedoch oft gesundes Gewebe und versagen manchmal, wenn Tumoren resistent werden. Forscher suchen daher nach Therapien, die ihre Wirkung im Tumor konzentrieren und den Rest des Körpers schonen. Das Team dieser Arbeit konzentrierte sich auf den Aufbau eines Wirkstoffsystems, das auf einen externen Auslöser – Licht – reagiert, sodass die meiste Wirkung genau dort stattfindet, wo sie benötigt wird, im Inneren oder in der Nähe des Tumors im Darm.
Entwurf winziger Gelatine-Träger
Die Wissenschaftler bauten ihr Trägersystem aus Gelatine, einem vertrauten Lebensmittel- und Medizinmaterial, das der Körper sicher abbauen kann. Sie mischten gelöste Gelatine mit Curcumin und setzten dann kurze Ultraschallpulse ein, um Nanopartikel zu bilden – Kugeln, die Tausende Male kleiner sind als ein Sandkorn. Durch sorgfältiges Abstimmen der Mischzeit und des Verhältnisses von Curcumin zu Gelatine erzielten sie stabile Partikel von etwa 20–40 Nanometern Durchmesser, die ungefähr zwei Drittel des verfügbaren Curcumins einschlossen. Eine Reihe physikalischer Tests bestätigte Größe, Struktur und Stabilität der Partikel und deutete darauf hin, dass Curcumin hauptsächlich durch schwache physikalische Wechselwirkungen und nicht durch permanente chemische Bindungen gehalten wird, was die bedarfsgerechte Freisetzung erleichtert. 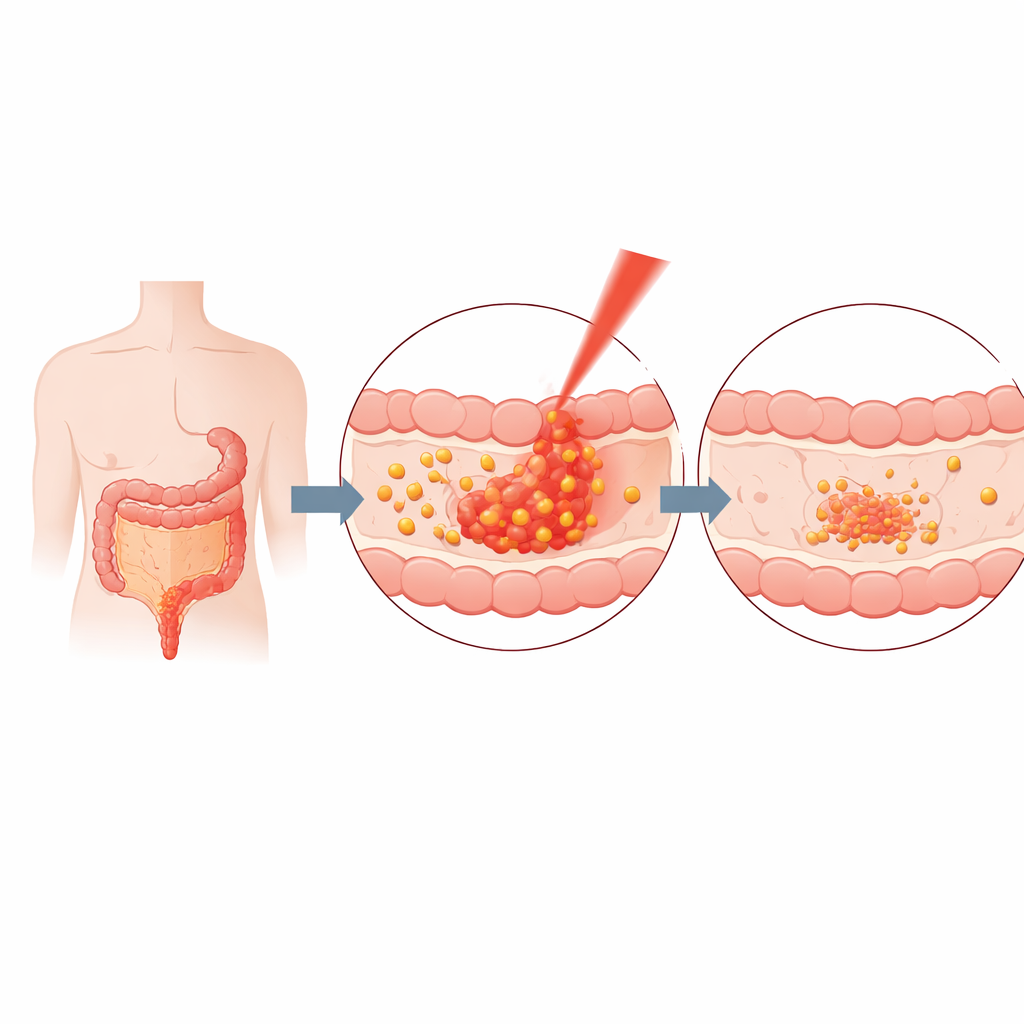
Sanfte Wärme als Ein-/Ausschalter
Im nächsten Schritt untersuchte das Team, wie nahes Infrarotlicht (NIR) als Fernsteuerung für die Wirkstofffreisetzung dienen könnte. NIR-Licht, das für das Auge unsichtbar ist, kann Gewebe tiefer durchdringen als sichtbares Licht und wird bereits in einigen medizinischen Geräten verwendet. Wenn die Curcumin-Gelatine-Partikel mit einer Infrarotlampe bestrahlt wurden, die sie auf etwa 38 °C erwärmte – nur geringfügig über der normalen Körpertemperatur – quollen sie an und begannen, Curcumin schneller freizusetzen. Bei dieser milden Temperatur wurde etwa die Hälfte des eingeschlossenen Wirkstoffs freigesetzt, und die Gesamtrate der Freisetzung über die Zeit war bis zu einem Drittel schneller als ohne Licht. Wichtig ist, dass dieser Effekt schon nach nur 30 Sekunden Beleuchtung erreicht werden konnte, was einen schnellen, temperaturabhängigen Schalter für das Einleiten der Wirkstofffreisetzung demonstriert. 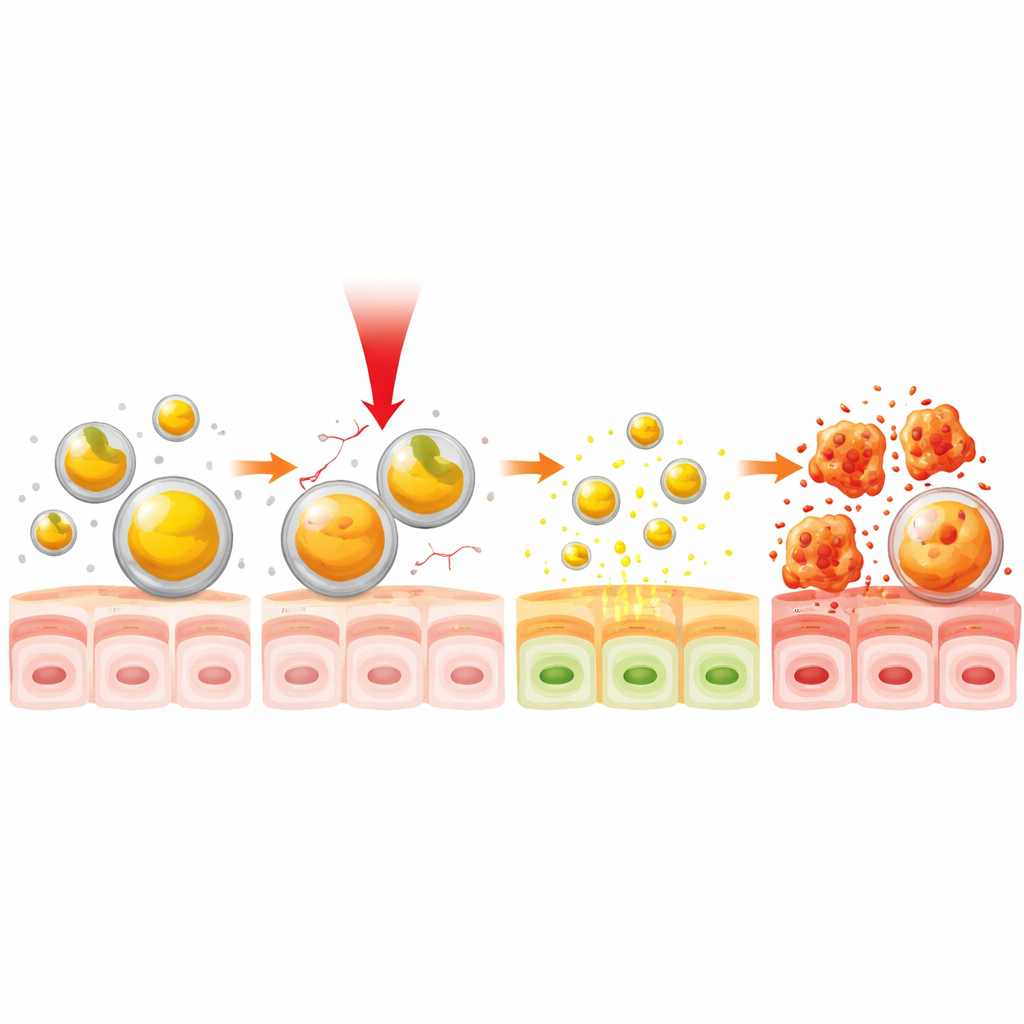
Prüfung des Systems in 2D- und 3D-Tumormodellen
Um zu prüfen, ob dieses lichtaktivierte System Krebszellen tatsächlich schadet, testeten die Forscher es an zwei menschlichen Darmkrebszelllinien und an gesunden Gefäßzellen, die in Kultur gezüchtet wurden. Außerdem bauten sie ein realistischeres dreidimensionales Modell, in dem Darmkrebszellen zusammen mit Endothelzellen wuchsen und so einen Mini-Tumor mit seinen unterstützenden Blutgefäßen nachahmten. Da Curcumin unter bestimmtem Licht natürlich fluoresziert, konnte das Team verfolgen, wie die Nanopartikel in Zellen eindrangen und sich im Zellplasma ansammelten. Bei einer Curcumin-Äquivalenzdosis von 25 Mikrogramm pro Milliliter verringerten die Partikel das Überleben, die Beweglichkeit und die Invasivität der Krebszellen deutlich, besonders in Kombination mit NIR-Erwärmung. Im Gegensatz dazu waren gesunde Zellen bei gleichen oder niedrigeren Dosen deutlich weniger betroffen, was auf eine gewisse Selektivität gegenüber Tumorgewebe hindeutet.
Wie die Partikel Krebszellen in Richtung Zelltod treiben
Über die einfache Zählung überlebender Zellen hinaus untersuchten die Forscher, wie die Behandlung das Zellverhalten veränderte. Krebszellen, die NIR-aktivierten Curcumin-Partikeln ausgesetzt waren, zeigten klassische Anzeichen des programmierten Zelltods, der Apoptose: ihre DNA kondensierte, die Zellkerne fragmentierten, und ihre energieproduzierenden Mitochondrien verloren ihr normales Membranpotenzial und schrumpften. In Wundheilungs- und Transwell-Tests, welche die Geschwindigkeit der Zellausbreitung und Invasion messen, verlangsamten NIR-behandelte Partikel das Zellmigration und die Invasion von Krebszellen deutlich stärker als Partikel ohne Lichteinwirkung. Diese Veränderungen stimmen mit Curcumins bekannter Fähigkeit überein, schädliche reaktive Sauerstoffspezies zu verringern und entzündliche Signale zu dämpfen – Signalwege, die Tumoren beim Wachsen und Ausbreiten unterstützen.
Was das für die künftige Krebsbehandlung bedeuten könnte
Einfach gesagt verwandelt diese Arbeit den Wirkstoff von Kurkuma in eine gezielte, „ferngesteuerte“ Krebstherapie. Indem Curcumin in biologisch abbaubaren Gelatinekugeln versteckt und sanfte NIR-Erwärmung als Ein-/Ausschalter genutzt wurde, erzielten die Forscher eine schnelle, kontrollierte Wirkstofffreisetzung und starke anti-tumorale Effekte in realistischen Labormodellen, während gesunde Zellen weitgehend verschont blieben. Obwohl deutlich mehr Tests an Tieren und Menschen erforderlich sind, deutet die Studie auf einen Weg zu Darmkrebstherapien hin, die präziser, weniger toxisch und potenziell leichter herstellbar sind und damit den Weg für intelligentere, lichtgeführte Behandlungen auf Basis sicherer, natürlicher Verbindungen öffnen.
Zitation: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
Schlüsselwörter: Darmkrebs, Curcumin, Nanopartikel, nahes Infrarotlicht, gezielte Wirkstoffabgabe