Clear Sky Science · ru
Синтез и характеристика чувствительных к ближнему ИК излучению куркумин‑желатиновых наночастиц для целевой доставки лекарств в 3D‑колоректальном раке
Превращение специи в «умного» борца с раком
Многие знают куркумин как ярко‑жёлтое соединение в куркуме, обычной кухонной специи. Помимо кулинарной известности, куркумин способен замедлять рост раковых клеток в лаборатории. Проблема в том, что организм плохо его усваивает, и он быстро разрушается. В этой работе показано, как учёные превратили куркумин в «умное» средство против рака толстой кишки, упаковав его в крошечные желатиновые частицы, которые высвобождают лекарство при мягком нагреве ближним инфракрасным светом.
Почему опухоли толстой кишки трудно лечить
Рак толстой кишки остаётся одним из самых распространённых и смертоносных видов рака в мире. Традиционные методы — операция, химио‑ и лучевая терапия — могут спасти жизни, но часто повреждают здоровые ткани и могут оказаться неэффективными при развитии резистентности опухолей. Поэтому исследователи ищут терапии, которые концентрируют воздействие внутри опухоли, щадя остальной организм. Группа авторов сосредоточилась на создании лекарственной системы, реагирующей на внешний триггер — свет — чтобы основное действие происходило только там, где это нужно, внутри или рядом с опухолью в кишечнике.
Проектирование крошечных желатиновых носителей
Учёные создали систему доставки на основе желатина — знакомого пищевого и медицинского материала, который организм безопасно расщепляет. Они растворили желатин и куркумин, затем с помощью кратковременных ультразвуковых импульсов сформировали наночастицы — сферические структуры в тысячи раз мельче песчинки. Тщательно подбирая время смешивания и соотношение куркумина и желатина, им удалось получить стабильные частицы диаметром примерно 20–40 нанометров, удерживающие примерно две трети доступного куркумина. Ряд физических тестов подтвердил размер, структуру и стабильность частиц и указал на то, что куркумин удерживается в основном слабыми физическими взаимодействиями, а не прочными химическими связями, что облегчает его высвобождение по требованию. 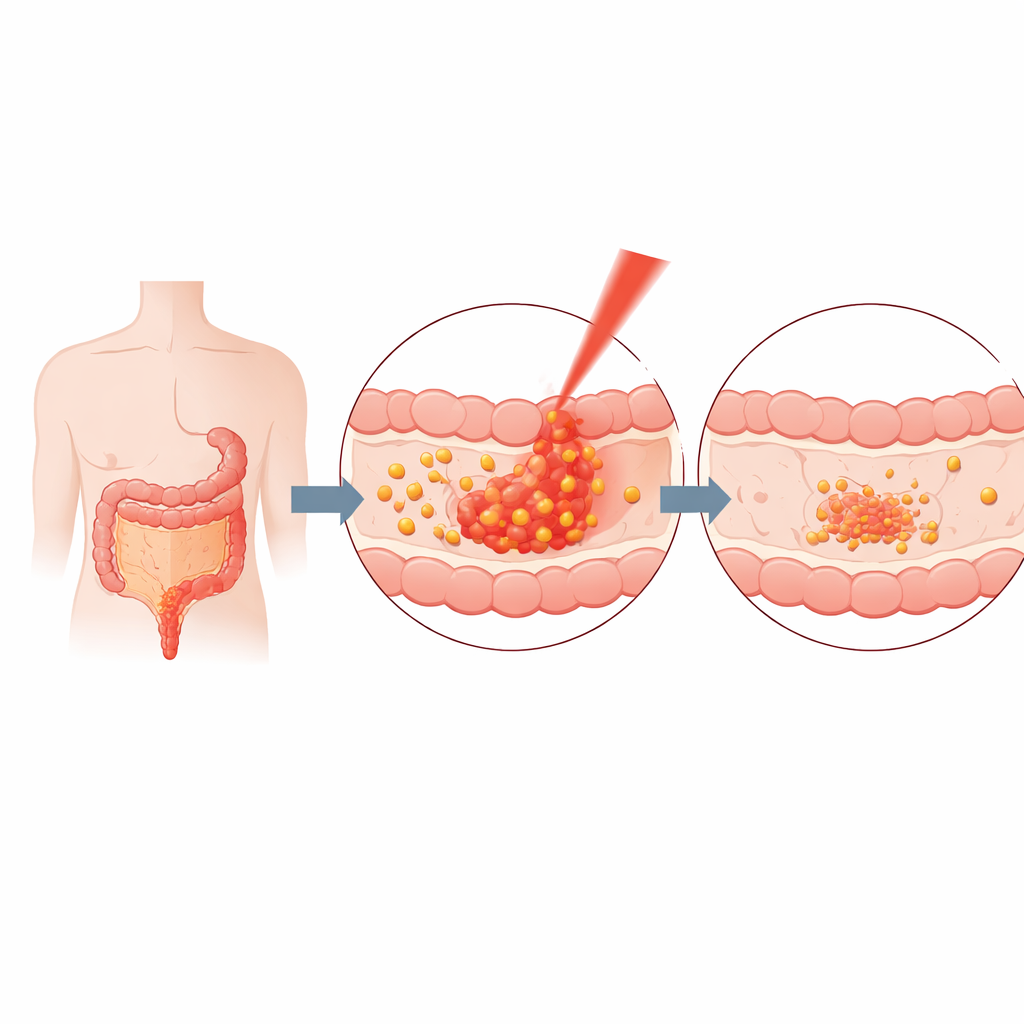
Использование мягкого тепла как выключателя вкл/выкл
Далее команда изучала, как ближний инфракрасный (БИК) свет может служить дистанционным управлением высвобождением лекарства. БИК‑свет, невидимый невооружённым глазом, проникает глубже в ткани, чем видимый свет, и уже применяется в некоторых медицинских устройствах. Когда куркумин‑желатиновые частицы облучали инфракрасной лампой, нагревая их до примерно 38 °C — немного выше нормальной температуры тела — частицы разбухали и начали быстрее выпускать куркумин. При таком мягком нагреве высвободилась около половины захваченного лекарства, а суммарный выход во времени оказался до одной трети быстрее, чем без облучения. Важно, что этот эффект достигается всего за 30 секунд освещения, демонстрируя быстрый температурочувствительный переключатель для включения высвобождения лекарства. 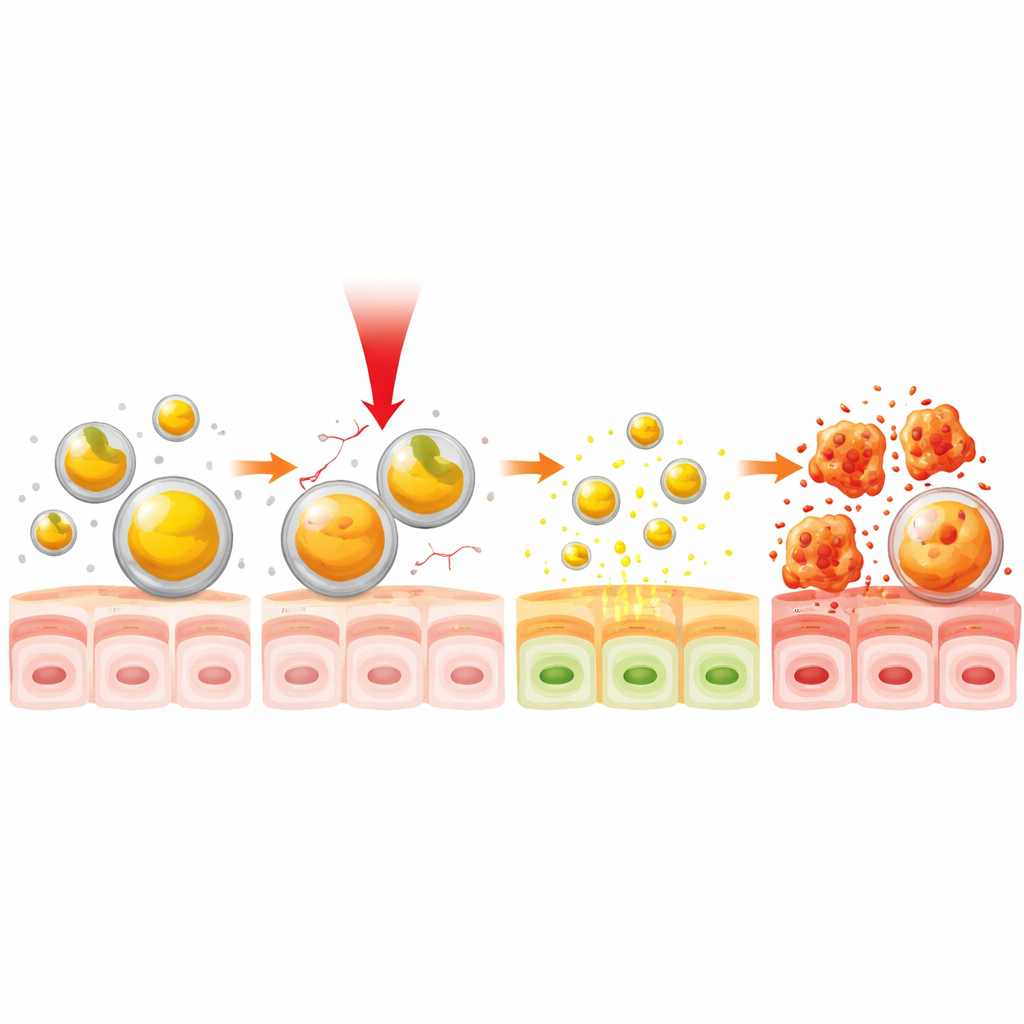
Испытание системы в 2D‑ и 3D‑моделях опухоли
Чтобы проверить, действительно ли система, активируемая светом, вредит раковым клеткам, исследователи протестировали её на двух линиях человеческих клеток колоректального рака и на здоровых клетках сосудистой стенки, выращенных в чашках. Они также создали более реалистичную трёхмерную модель, в которой раковые клетки толстой кишки росли вместе с эндотелиальными клетками, имитируя мини‑опухоль с её поддерживающими сосудами. Поскольку куркумин естественно флуоресцирует при определённом освещении, команда могла наблюдать, как наночастицы проникают в клетки и накапливаются в клеточном соке. При эквивалентной дозе куркумина 25 мкг/мл частицы значительно снижали выживаемость, подвижность и инвазивность раковых клеток, особенно в сочетании с БИК‑нагревом. В то же время здоровые клетки были значительно менее чувствительны при тех же или меньших дозах, что указывает на некоторую селективность в отношении опухолевой ткани.
Как частицы подталкивают раковые клетки к гибели
Помимо обычного подсчёта живых клеток, исследователи изучили, как лечение меняет поведение клеток. Раковые клетки, подвергшиеся действию активируемых БИК куркумин‑частиц, показывали классические признаки программируемой клеточной гибели (апоптоза): конденсацию ДНК, фрагментацию ядер, потерю нормального электропотенциала и уменьшение митохондрий. В тестах заживления ран и Transwell, измеряющих скорость распространения и инвазии клеток, частицы, активированные БИК, значительно замедляли миграцию и инвазию раковых клеток по сравнению с частицами без облучения. Эти изменения согласуются с известной способностью куркумина снижать вредные реактивные кислородные виды и ослаблять провоспалительные сигналы — пути, которые способствуют росту и распространению опухолей.
Что это может значить для будущей онкологической помощи
Проще говоря, работа превращает активный компонент куркумы в целевое «удалённо управляемое» противораковое средство. Спрятав куркумин внутри биодеградируемых желатиновых шариков и используя мягкий ближний инфракрасный нагрев как переключатель вкл/выкл, исследователи добились быстрого контролируемого высвобождения лекарства и сильного антиопухолевого эффекта в реалистичных лабораторных моделях, при этом в значительной мере щадя здоровые клетки. Хотя требуется ещё много испытаний на животных и в клинике, исследование указывает на путь к более точным, менее токсичным и потенциально более простым в производстве терапиям рака толстой кишки, открывая дорогу к «умным», управляемым светом методам на базе безопасных натуральных соединений.
Цитирование: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
Ключевые слова: колоректальный рак, куркумин, наночастицы, ближний инфракрасный свет, целевая доставка лекарств