Clear Sky Science · sv
Syntes och karaktärisering av NIR-känsliga curcumin‑gelatin‑nanopartiklar för målinriktad läkemedelsleverans i 3D‑koloncancer
Att förvandla ett kryddmått till en smart cancerbekämpare
Många känner till curcumin som den starkt gula föreningen i gurkmeja, ett vanligt kökssalt. Utöver sin kulinariska berömmelse kan curcumin bromsa tillväxten av cancerceller i laboratoriet. Problemet är att vår kropp inte tar upp det väl, och det bryts snabbt ned. Denna studie visar hur forskare förvandlade curcumin till en ”smart” behandling för koloncancer genom att paketera det i små gelatinpartiklar som släpper ut läkemedlet när de värms lätt med när‑infrarött ljus.
Varför kolonstumörer är svåra att behandla
Koloncancer är fortfarande en av de vanligaste och mest dödliga cancerformerna i världen. Traditionella behandlingar som kirurgi, kemoterapi och strålning kan rädda liv men skadar ofta frisk vävnad och kan misslyckas när tumörer blir resistenta. Därför söker forskare terapier som koncentrerar verkan inuti tumörer samtidigt som resten av kroppen skonas. Gruppen bakom denna artikel fokuserade på att bygga ett läkemedelssystem som reagerar på en extern utlösare—ljus—så att den mest intensiva effekten sker endast där det behövs, inne i eller nära tumören i kolon.
Design av små gelatinkärl
Forskarna byggde sitt leveranssystem av gelatin, ett välkänt livsmedelsoch medicinskt material som kroppen säkert kan bryta ner. De blandade löst gelatin och curcumin och använde sedan korta ultraljudspulser för att bilda nanopartiklar—sfärer tusentals gånger mindre än ett sandkorn. Genom att noggrant ställa in blandningstid och förhållandet curcumin till gelatin fick de stabila partiklar på cirka 20–40 nanometer i diameter som fångade in ungefär två tredjedelar av det tillgängliga curcuminet. Ett batteri av fysikaliska tester bekräftade partiklarnas storlek, struktur och stabilitet och antydde att curcumin hölls främst av svaga fysiska krafter snarare än permanenta kemiska bindningar, vilket gör det lättare att frigöra på begäran. 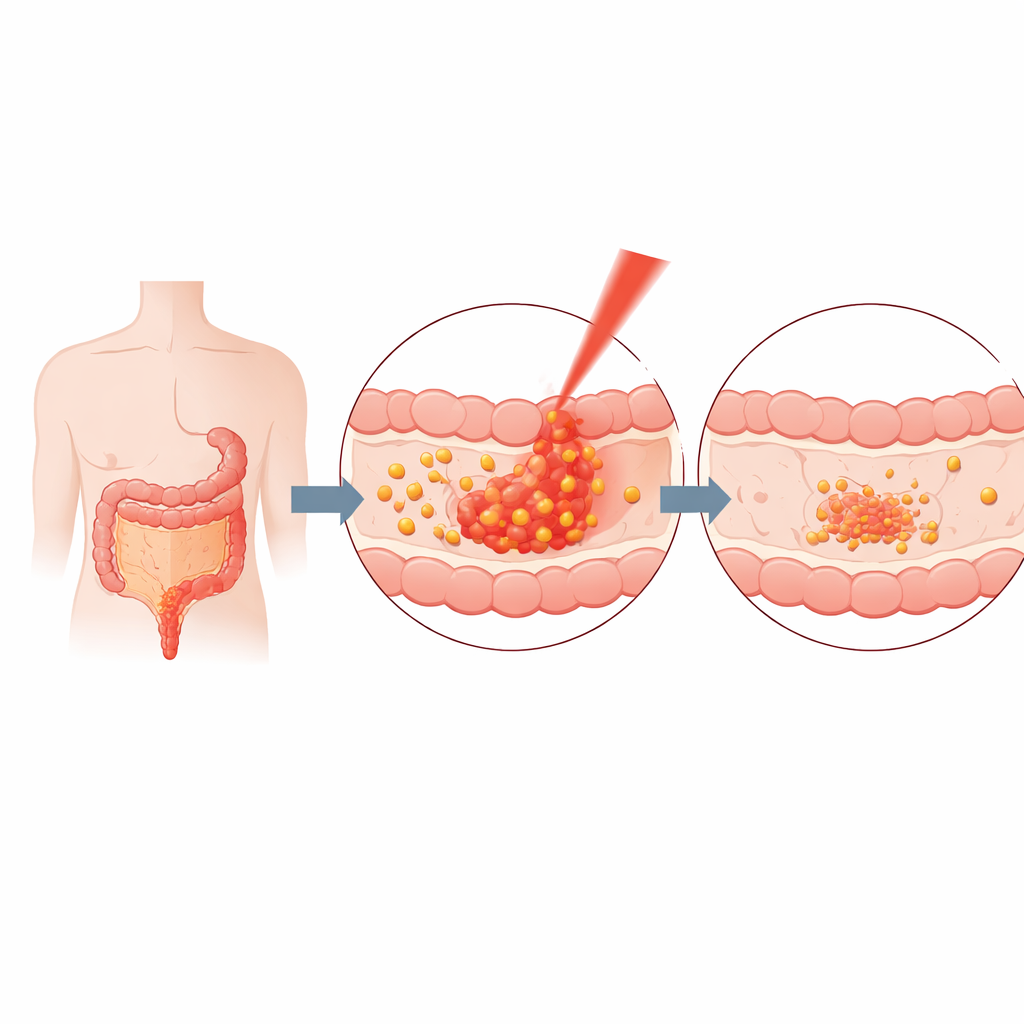
Att använda mild värme som en av/på‑knapp
Nästa steg var att undersöka hur när‑infrarött (NIR) ljus kunde fungera som fjärrkontroll för läkemedelsfrisättning. NIR‑ljus, som är osynligt för ögat, kan tränga djupare in i vävnad än synligt ljus och används redan i vissa medicinska enheter. När curcumin‑gelatinpartiklarna exponerades för en infraröd lampa som värmde dem till cirka 38 °C—bara något över normal kroppstemperatur—svällde de i storlek och började läcka curcumin snabbare. Vid denna milda temperatur frigjordes ungefär hälften av det bundna läkemedlet, och den totala frisättningen över tid var upp till en tredjedel snabbare än utan ljus. Viktigt är att denna effekt kunde uppnås på bara 30 sekunders belysning, vilket demonstrerar en snabb, temperatursensitiv strömbrytare för att slå på läkemedelsfrisättning. 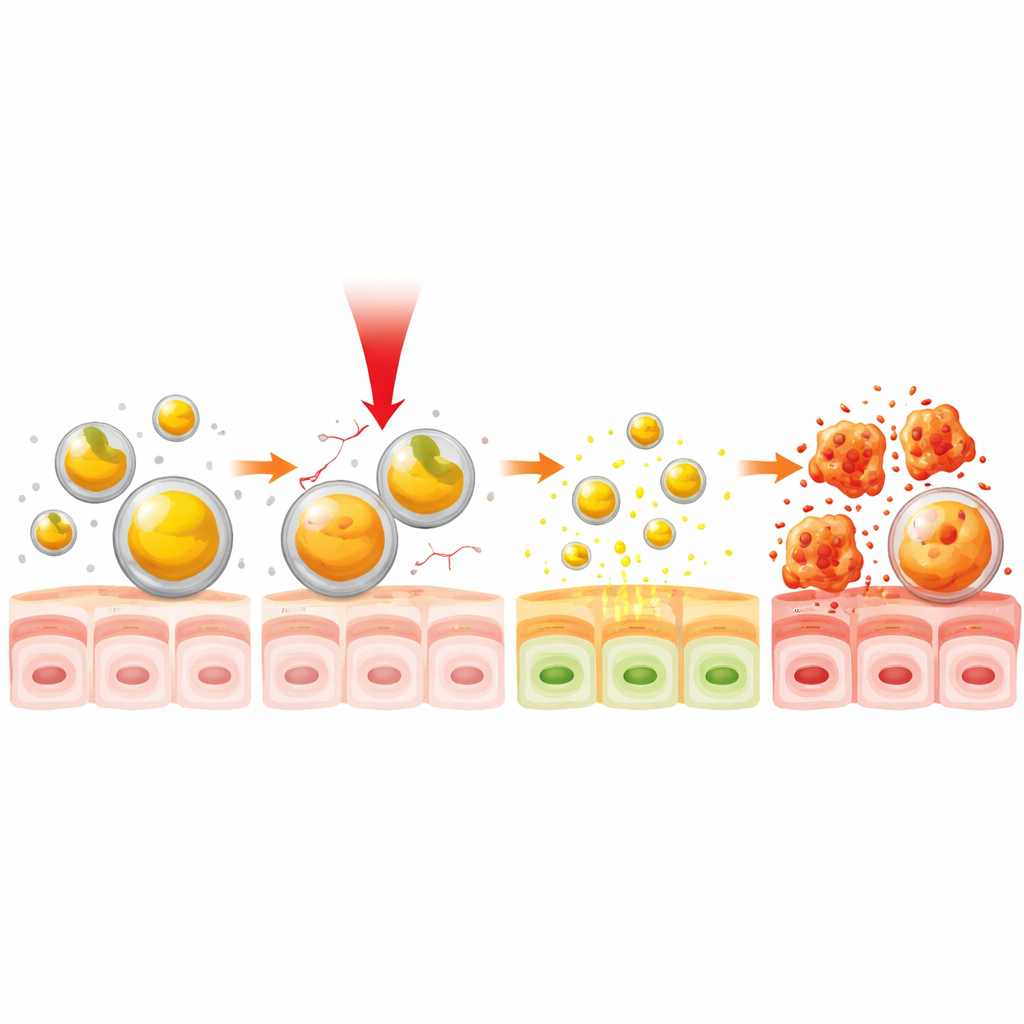
Systemet testas i 2D‑ och 3D‑tumörmodeller
För att se om detta ljusaktiverade system faktiskt skadade cancerceller testade forskarna det på två humana koloncancercellinjer och på friska blodkärlsceller odlade i skålar. De byggde också en mer realistisk tredimensionell modell där kolonceller växte tillsammans med endotelceller och efterliknade en mini‑tumör med sina stödjande blodkärl. Eftersom curcumin lyser naturligt under viss belysning kunde teamet följa hur nanopartiklarna gick in i cellerna och ansamlades i cellvätskan. Vid en curcumin‑ekvivalent dos på 25 mikrogram per milliliter minskade partiklarna signifikant cancercellernas överlevnad, rörelseförmåga och invasion, särskilt i kombination med NIR‑uppvärmning. I kontrast påverkades friska celler mycket mindre vid samma eller lägre doser, vilket tyder på en grad av selektivitet för tumörvävnad.
Hur partiklarna driver cancerceller mot död
Utöver att bara räkna levande celler undersökte forskarna hur behandlingen förändrade cellbeteendet. Cancerceller som exponerats för NIR‑aktiverade curcuminpartiklar visade klassiska tecken på kontrollerad celldöd, eller apoptos: deras DNA kondenserade, deras kärnor fragmenterades och deras energiproducerande mitokondrier förlorade sin normala elektriska potential och krympte. I sår‑helande och Transwell‑tester som mäter hur snabbt celler sprider sig och invaderar, bromsade NIR‑behandlade partiklar cancercellernas migration och invasion avsevärt mer än partiklar utan ljusexponering. Dessa förändringar är förenliga med curcuminets kända förmåga att minska skadliga reaktiva syreradikaler och dämpa inflammatoriska signaler, banor som hjälper tumörer att växa och sprida sig.
Vad detta kan betyda för framtidens cancervård
Enkelt uttryckt förvandlar detta arbete gurkmejans aktiva ingrediens till en målinriktad, ”fjärrstyrd” cancerbehandling. Genom att dölja curcumin i biologiskt nedbrytbara gelatinsfärer och använda mild när‑infraröd uppvärmning som en av/på‑knapp uppnådde forskarna snabb, kontrollerad läkemedelsfrisättning och starka antitumöreffekter i realistiska laboratoriemodeller, samtidigt som friska celler i stor utsträckning skons. Även om betydligt mer testning i djur och människor krävs, pekar studien på en väg mot koloncancerterapier som är mer precisa, mindre toxiska och potentiellt enklare att producera, och öppnar dörren för smartare, ljusstyrda behandlingar baserade på säkra, naturliga föreningar.
Citering: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
Nyckelord: koloncancer, curcumin, nanopartiklar, närinfrarött ljus, målinriktad läkemedelsleverans