Clear Sky Science · fr
Synthèse et caractérisation de nanoparticules curcumine‑gélatine sensibles au proche infrarouge pour une délivrance ciblée de médicaments dans un modèle 3D du cancer du côlon
Transformer une épice en un combattant intelligent du cancer
Beaucoup de gens connaissent la curcumine comme le composé jaune vif du curcuma, une épice courante. Au‑delà de sa renommée culinaire, la curcumine peut ralentir la croissance des cellules cancéreuses en laboratoire. Le problème est que notre organisme l’absorbe mal et qu’elle se dégrade rapidement. Cette étude montre comment des chercheurs ont transformé la curcumine en un traitement « intelligent » du cancer du côlon en l’encapsulant dans de minuscules particules de gélatine qui libèrent leur charge médicamenteuse lorsqu’on les chauffe légèrement avec de la lumière proche infrarouge.
Pourquoi les tumeurs du côlon sont difficiles à traiter
Le cancer du côlon reste l’un des cancers les plus fréquents et mortels dans le monde. Les traitements traditionnels comme la chirurgie, la chimiothérapie et la radiothérapie peuvent sauver des vies mais endommagent souvent les tissus sains et peuvent échouer lorsque les tumeurs deviennent résistantes. Les chercheurs cherchent donc des thérapies qui concentrent leur action au niveau des tumeurs tout en épargnant le reste de l’organisme. L’équipe à l’origine de cet article s’est concentrée sur la conception d’un système médicamenteux qui répond à un déclencheur externe — la lumière — de sorte que la majeure partie de l’effet se produise uniquement là où c’est nécessaire, à l’intérieur ou à proximité de la tumeur dans le côlon.
Conception de minuscules transporteurs en gélatine
Les scientifiques ont construit leur système d’administration à partir de gélatine, un matériau alimentaire et médical familier que le corps peut décomposer en toute sécurité. Ils ont mélangé de la gélatine dissoute et de la curcumine, puis utilisé de brèves impulsions d’ultrasons pour former des nanoparticules — des sphères des milliers de fois plus petites qu’un grain de sable. En réglant soigneusement le temps de mixage et le rapport curcumine/gélatine, ils ont obtenu des particules stables d’environ 20–40 nanomètres de diamètre qui ont piégé environ les deux tiers de la curcumine disponible. Une batterie de tests physiques a confirmé la taille, la structure et la stabilité des particules, et a suggéré que la curcumine était retenue principalement par des forces physiques faibles plutôt que par des liaisons chimiques permanentes, ce qui facilite sa libération à la demande. 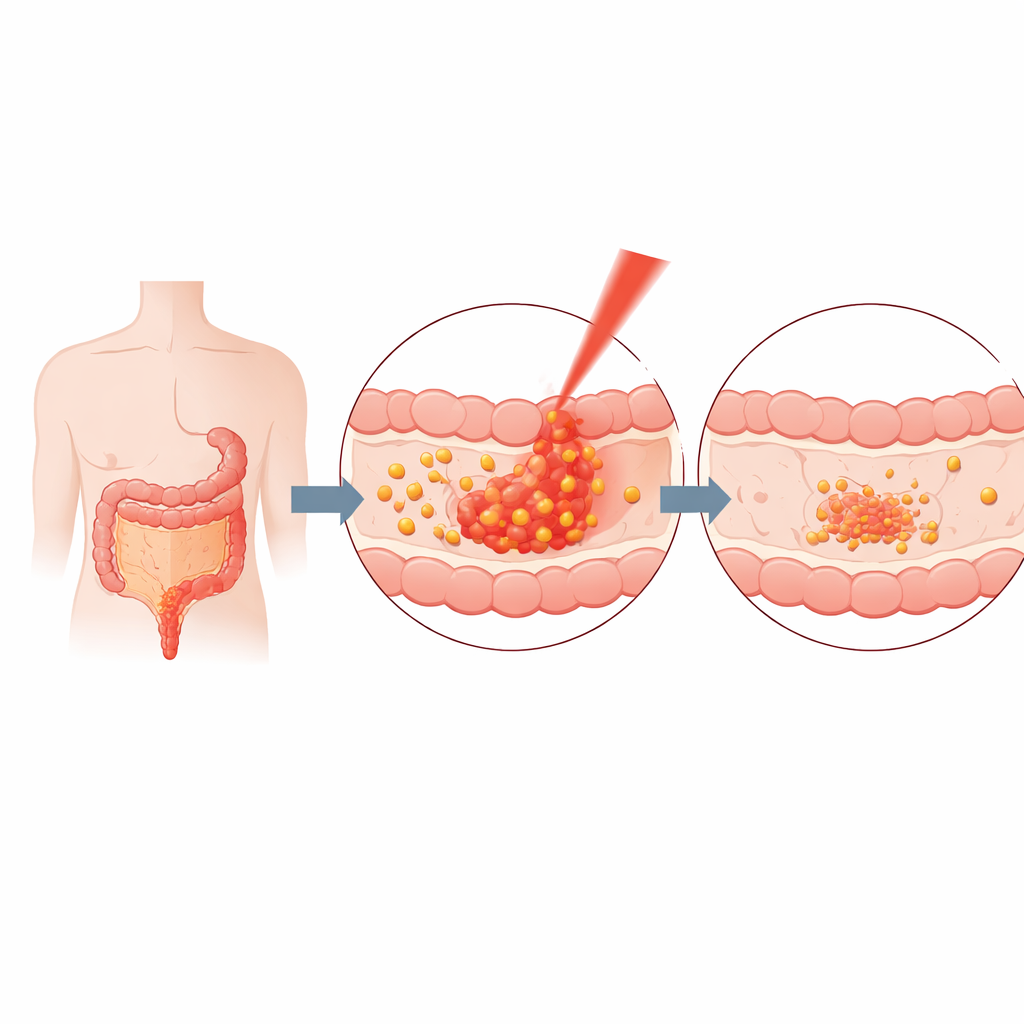
Utiliser la chaleur douce comme interrupteur marche‑arrêt
Ensuite, l’équipe a exploré comment la lumière proche infrarouge (PIR) pouvait servir de télécommande pour la libération du médicament. La lumière PIR, invisible à l’œil, peut pénétrer les tissus plus profondément que la lumière visible et est déjà utilisée dans certains dispositifs médicaux. Lorsque les particules curcumine‑gélatine ont été exposées à une lampe infrarouge les chauffant autour de 38 °C — juste un peu au‑dessus de la température corporelle normale — leur taille a gonflé et elles ont commencé à fuir la curcumine plus rapidement. À cette température modérée, environ la moitié du médicament piégé a été libérée, et la libération globale au fil du temps a été jusqu’à un tiers plus rapide qu’en l’absence de lumière. Fait important, cet effet pouvait être obtenu en seulement 30 secondes d’illumination, démontrant un interrupteur rapide et sensible à la température pour activer la libération du médicament. 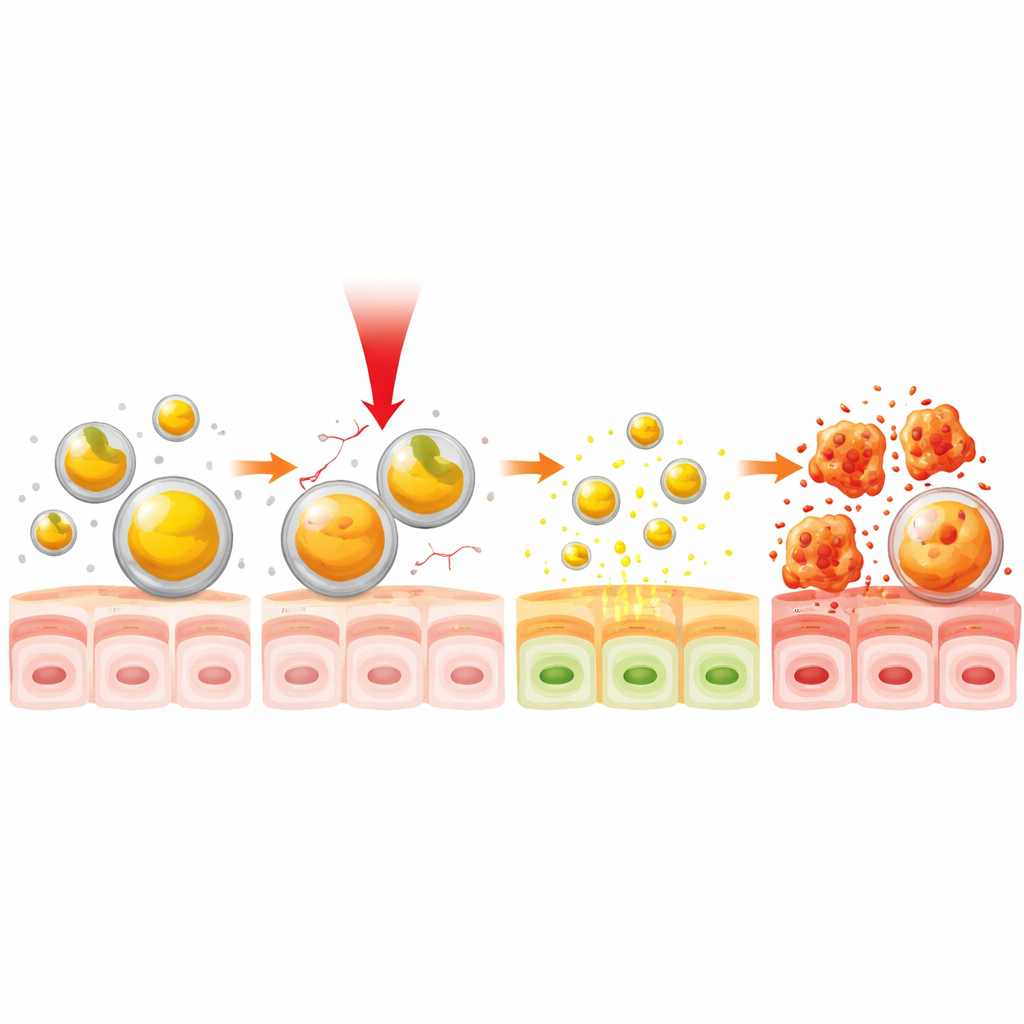
Évaluation du système dans des modèles tumoraux 2D et 3D
Pour vérifier si ce système activé par la lumière nuisait réellement aux cellules cancéreuses, les chercheurs l’ont testé sur deux lignées cellulaires humaines de cancer du côlon et sur des cellules endothéliales saines cultivées en culture. Ils ont aussi construit un modèle tridimensionnel plus réaliste dans lequel des cellules de cancer du côlon croissaient avec des cellules endothéliales, reproduisant une mini‑tumeur avec ses vaisseaux de soutien. Comme la curcumine émet naturellement de la fluorescence sous certaines lumières, l’équipe a pu observer les nanoparticules pénétrer dans les cellules et s’accumuler dans le cytoplasme. À une dose équivalente en curcumine de 25 microgrammes par millilitre, les particules ont réduit de façon significative la survie, la mobilité et l’invasion des cellules cancéreuses, en particulier lorsqu’elles étaient combinées au chauffage PIR. En revanche, les cellules saines ont été beaucoup moins affectées aux mêmes doses ou à des doses inférieures, ce qui suggère un certain degré de sélectivité pour le tissu tumoral.
Comment les particules poussent les cellules cancéreuses vers la mort
Au‑delà du simple comptage des cellules vivantes, les chercheurs ont examiné comment le traitement modifiait le comportement cellulaire. Les cellules cancéreuses exposées aux particules de curcumine activées par PIR présentaient des signes classiques d’apoptose, ou mort cellulaire programmée : leur ADN se condensait, leurs noyaux se fragmentaient, et leurs mitochondries productrices d’énergie perdaient leur potentiel électrique normal et se rétractaient. Dans des tests de cicatrisation et de Transwell mesurant la vitesse de propagation et d’invasion, les particules traitées par PIR ont considérablement ralenti la migration et l’invasion des cellules cancéreuses bien plus que les particules non éclairées. Ces changements sont cohérents avec la capacité connue de la curcumine à diminuer les molécules réactives de l’oxygène nocives et à atténuer les signaux inflammatoires, des voies qui aident les tumeurs à croître et à se propager.
Ce que cela pourrait signifier pour les soins du cancer à l’avenir
En termes simples, ce travail transforme le principe actif du curcuma en un traitement anticancéreux ciblé et « télécommandé ». En cachant la curcumine dans des sphères de gélatine biodégradables et en utilisant un réchauffement doux proche infrarouge comme interrupteur marche‑arrêt, les chercheurs ont obtenu une libération rapide et contrôlée du médicament et de puissants effets anti‑tumeur dans des modèles de laboratoire réalistes, tout en épargnant en grande partie les cellules saines. Bien que de nombreux tests supplémentaires chez l’animal et chez l’humain soient nécessaires, l’étude suggère une voie vers des thérapies du cancer du côlon plus précises, moins toxiques et potentiellement plus faciles à produire, ouvrant la porte à des traitements guidés par la lumière et basés sur des composés naturels sûrs.
Citation: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
Mots-clés: cancer du côlon, curcumine, nanoparticules, lumière proche infrarouge, délivrance ciblée de médicaments