Clear Sky Science · ja
3D大腸がんにおける標的薬物送達のための近赤外感受性クルクミン–ゼラチンナノ粒子の合成と特性評価
スパイスをスマートながん治療へ
多くの人がクルクミンを、台所にあるスパイスであるウコンの鮮やかな黄色成分として知っています。料理での知名度を超えて、クルクミンは実験室ではがん細胞の増殖を抑える働きを示します。しかし問題は、体内での吸収性が低く、速やかに分解されてしまう点です。本研究は、クルクミンを小さなゼラチン粒子に封入し、近赤外光で穏やかに加温することで薬剤を放出させる“スマート”治療法に変えた経緯を示しています。
大腸腫瘍が治療しにくい理由
大腸がんは依然として世界で最も一般的かつ致死的ながんの一つです。手術、化学療法、放射線療法といった従来の治療は命を救いますが、しばしば正常組織を傷つけ、腫瘍が耐性を獲得すると効果を失うことがあります。したがって研究者は、体の他部位をできるだけ傷つけず腫瘍内部に効果を集中させる治療法を模索しています。本稿の研究チームは、外部からのトリガー—光—に反応する薬物送達システムの構築に注力し、作用の大半が大腸内の腫瘍付近でのみ起こるように設計しました。
小さなゼラチン担体の設計
研究者らは、体内で安全に分解される馴染みのある食品・医療材料であるゼラチンを基に送達システムを構築しました。溶解したゼラチンとクルクミンを混合し、短い超音波パルスを用いてナノ粒子—砂粒よりも何千倍も小さな球状粒子—を形成しました。混合時間とクルクミン対ゼラチンの比率を慎重に調整することで、直径約20〜40ナノメートルの安定した粒子を得て、利用可能なクルクミンの約3分の2を封入しました。複数の物理的試験により粒子のサイズ、構造、安定性が確認され、クルクミンは主に永久的な化学結合ではなく弱い物理的相互作用で保持されていることが示唆され、必要時に放出しやすいことが示されました。 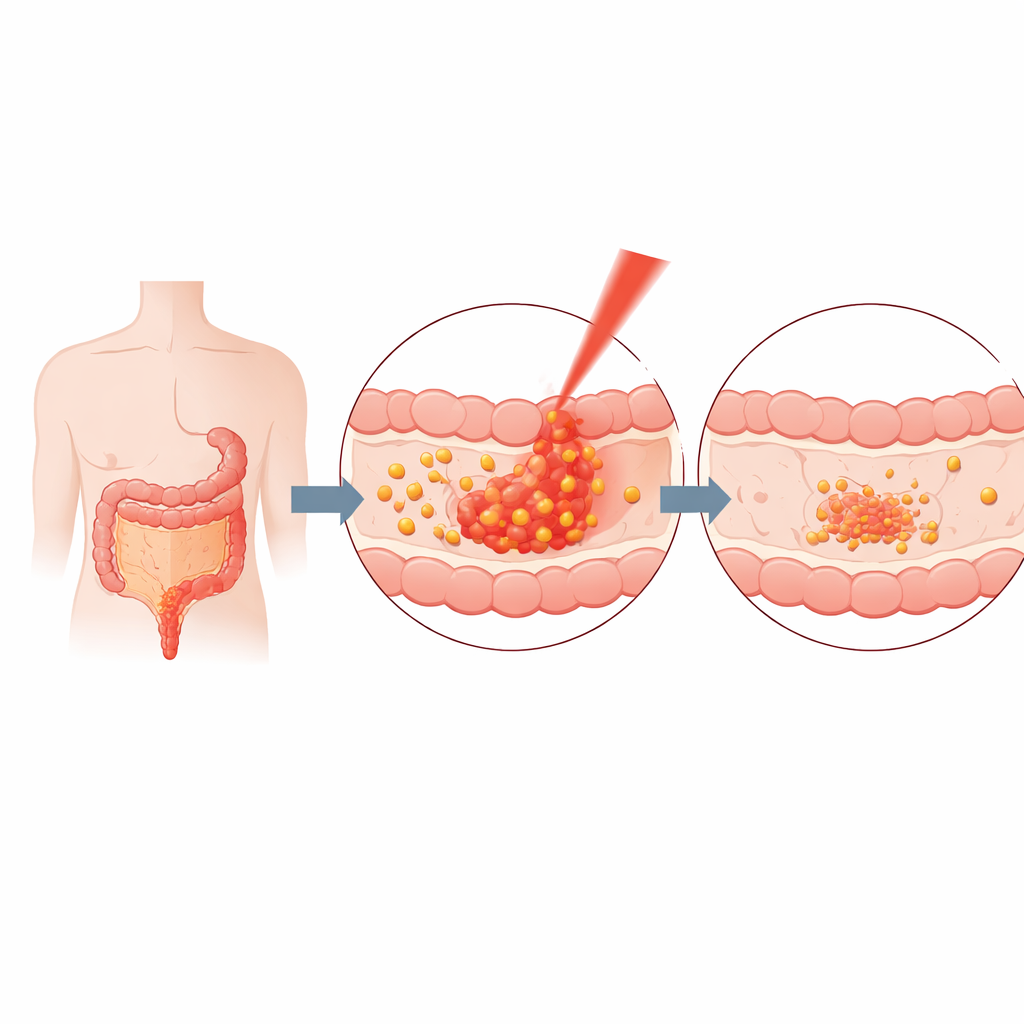
穏やかな加熱をオン/オフスイッチとして利用
次にチームは、近赤外(NIR)光が薬剤放出のリモートコントロールとして働くかを調べました。目に見えないNIR光は可視光より組織を深く透過でき、既にいくつかの医療機器で用いられています。クルクミン–ゼラチン粒子に赤外ランプで約38°C、すなわち通常の体温よりわずかに高い温度まで加温すると、粒子が膨潤してクルクミンの漏出が速くなることが分かりました。この穏やかな温度では、封入された薬の約半分が放出され、時間当たりの総放出速度は光なしの場合より最大で約3分の1速くなりました。重要なのは、この効果がわずか30秒の照射で達成でき、薬物放出をオンにする迅速な温度感受性スイッチを示した点です。 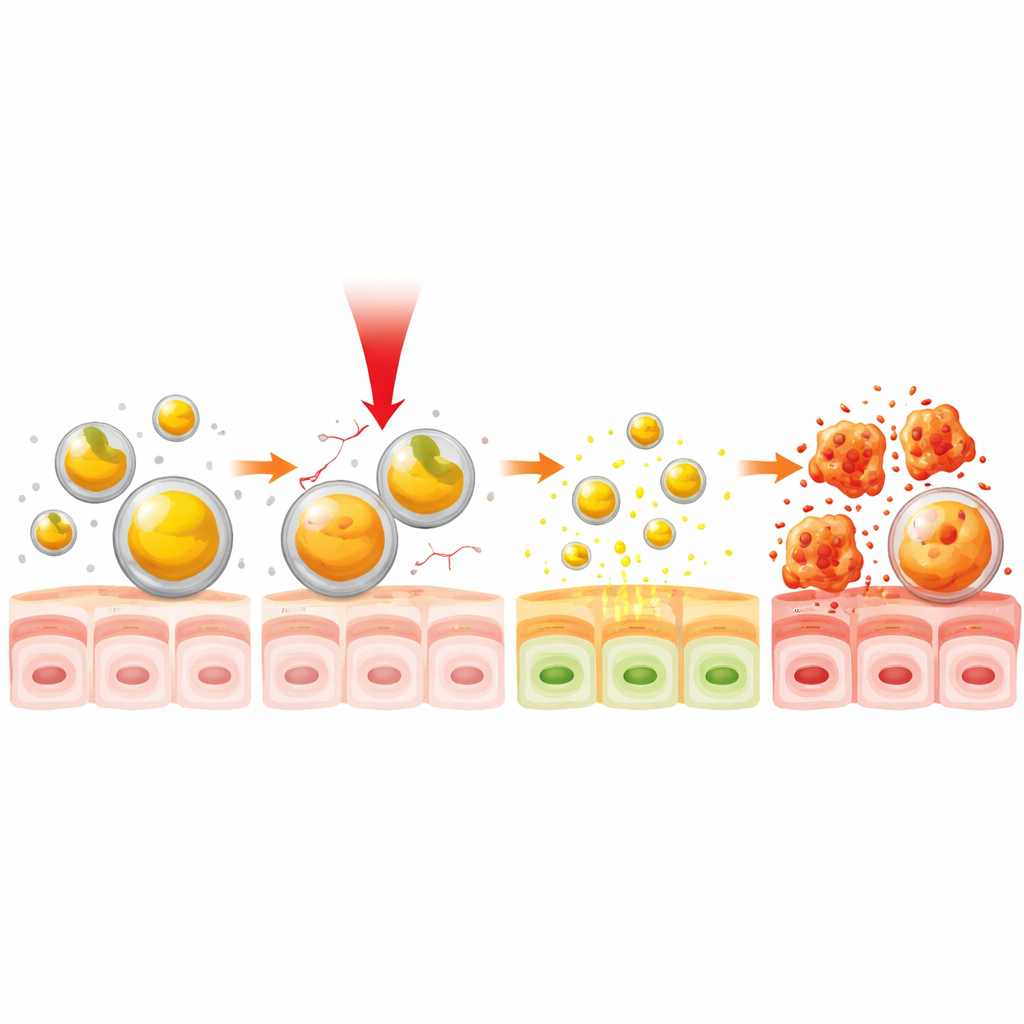
2Dおよび3D腫瘍モデルでの検証
この光活性化システムが実際にがん細胞を傷害するかを確かめるため、研究者らは2種類のヒト大腸がん細胞株と培養皿で育てた健康な血管内皮細胞に対して試験を行いました。さらに、大腸がん細胞が内皮細胞とともに成長する三次元のより現実的なモデルも構築し、血管を有する小さな腫瘍を模しました。クルクミンは特定の光で自然に蛍光を発するため、チームはナノ粒子が細胞内に取り込まれ細胞質に蓄積する過程を観察できました。クルクミン換算で25マイクログラム/ミリリットルの用量では、粒子は特にNIR加温と組み合わせた場合にがん細胞の生存、運動、侵襲を有意に減少させました。対照的に、同じまたはそれ以下の用量では健康な細胞への影響ははるかに小さく、腫瘍組織に対するある程度の選択性が示唆されました。
粒子ががん細胞を死へと導く仕組み
単に生存細胞数を数えるだけでなく、研究者らは治療が細胞の挙動をどのように変えるかを調べました。NIRで活性化されたクルクミン粒子にさらされたがん細胞は、プログラムされた細胞死(アポトーシス)の古典的な兆候を示しました:DNAの凝縮、核の断片化、エネルギー産生を担うミトコンドリアの膜電位の喪失と縮小です。細胞の広がりや侵襲速度を測る傷創治癒試験やトランスウェル試験では、NIR処理された粒子は光のない粒子よりもがん細胞の移動と侵襲をはるかに強く抑制しました。これらの変化は、クルクミンが有害な活性酸素種を低下させ、炎症性シグナルを鎮めるという既知の作用と整合し、腫瘍の成長と転移を助ける経路に影響を与えることを示しています。
将来のがん医療に与える意味
平たく言えば、本研究はウコンの有効成分を標的化された「遠隔制御可能な」がん治療へと変えます。生分解性のゼラチン球にクルクミンを包み込み、穏やかな近赤外加温をオン/オフスイッチとして用いることで、研究者らは迅速で制御された薬物放出と現実的な実験モデルでの強力な抗腫瘍効果を達成し、同時に健康な細胞への影響は大部分で抑えられました。さらに多くの動物実験や臨床試験が必要ですが、この研究は、より精密で毒性の低い、かつ製造が比較的簡便な大腸がん治療への道筋を示しており、安全な天然化合物に基づく光誘導型のスマート治療の可能性を開きます。
引用: Özerkan, D., Danışman-Kalındemirtaş, F. & Kariper, İ.A. Synthesis and characterization of NIR-sensitive curcumin-gelatin nanoparticles for targeted drug delivery in 3D colon cancer. Sci Rep 16, 12167 (2026). https://doi.org/10.1038/s41598-026-42199-3
キーワード: 大腸がん, クルクミン, ナノ粒子, 近赤外光, 標的薬物送達