Clear Sky Science · zh
通过理性设计κ-酪蛋白肽调节GSK-3β动力学以用于阿尔茨海默病治疗
奶源分子与记忆
阿尔茨海默病逐步夺走人们的记忆和独立性,目前的药物对大脑中引发疾病的根本损伤几乎无能为力。本研究探讨了一种出人意料却熟悉的治疗灵感来源:牛奶。作者们用先进的计算模拟重新设计了牛奶蛋白的一个微小片段,使其能够附着到与阿尔茨海默病相关的关键脑内酶上,可能抑制驱动疾病的一些有害过程。
误导大脑的那种酶
在阿尔茨海默病中,神经细胞受到缠结的tau纤维、黏性的淀粉样斑块以及神经连接失灵的损害。一个名为GSK-3β的酶在多方面助长了这些问题。它会在tau蛋白上添加化学标记,促进其凝聚成缠结;还影响淀粉样蛋白的形成,以及神经细胞的通信和对类胰岛素信号的应答。由于其核心作用,许多研究者将GSK-3β视为疾病进展的主控开关和新疗法的首要靶点。
为什么关注乳蛋白?
牛奶不仅含脂肪、糖和钙:它还含有可以被切割成短肽、并具有出乎意料强烈生物学作用的蛋白质。早期研究表明乳制品摄入可能对认知衰退有保护作用,特定来源于牛奶的肽能保护大脑、降低有害酶活性并在动物模型中改善记忆。酪蛋白是牛奶中的主要蛋白之一,包含多种亚型;其中κ-酪蛋白作为脑保护性片段的来源相对鲜为人知。作者们着手检视κ-酪蛋白的一小段是否可以被塑造成GSK-3β的高效抑制剂。
在计算机上设计更聪明的肽
研究团队首先预测了κ-酪蛋白的三维结构,并将其与GSK-3β进行对接,以寻找能嵌入酶中通常与能量分子结合的口袋的一段序列。他们发现了一个已有良好结合力的10个氨基酸片段。通过详细的能量计算,他们识别出该片段中四个对结合贡献较弱甚至不利的位置。随后,借助突变预测工具,他们系统地将这四个位置替换为可能增强相互作用的残基,构建了48个新的虚拟肽变体库。安全性筛查去除了被预测为有毒或致敏的候选者,剩下22个重新与GSK-3β进行对接。
筛选出最有希望的候选者
对接评分和相互作用图谱突出了四个表现突出的肽,命名为PEP8、PEP36、PEP40和PEP44。所有四者都共享两个关键变化:在一端附近将一个中性、疏油的残基替换为更具相互作用能力的残基,帮助它们更稳固地锚定在酶的口袋中。PEP8和PEP44还在另一个位置引入了带负电的残基,进一步增强了结合力。数百纳秒的计算模拟显示,当PEP8或PEP44结合时,酶的结构变得略微更紧凑且不那么灵活,尤其是在其天然底物通常位于的口袋周围。这些肽与酶形成的接触点比原始的牛奶片段更多,表明结合强度和选择性更高。能量分析确认PEP8和PEP44形成了最紧密的复合体,主要由短程引力和肽与酶之间的电性相互作用驱动。
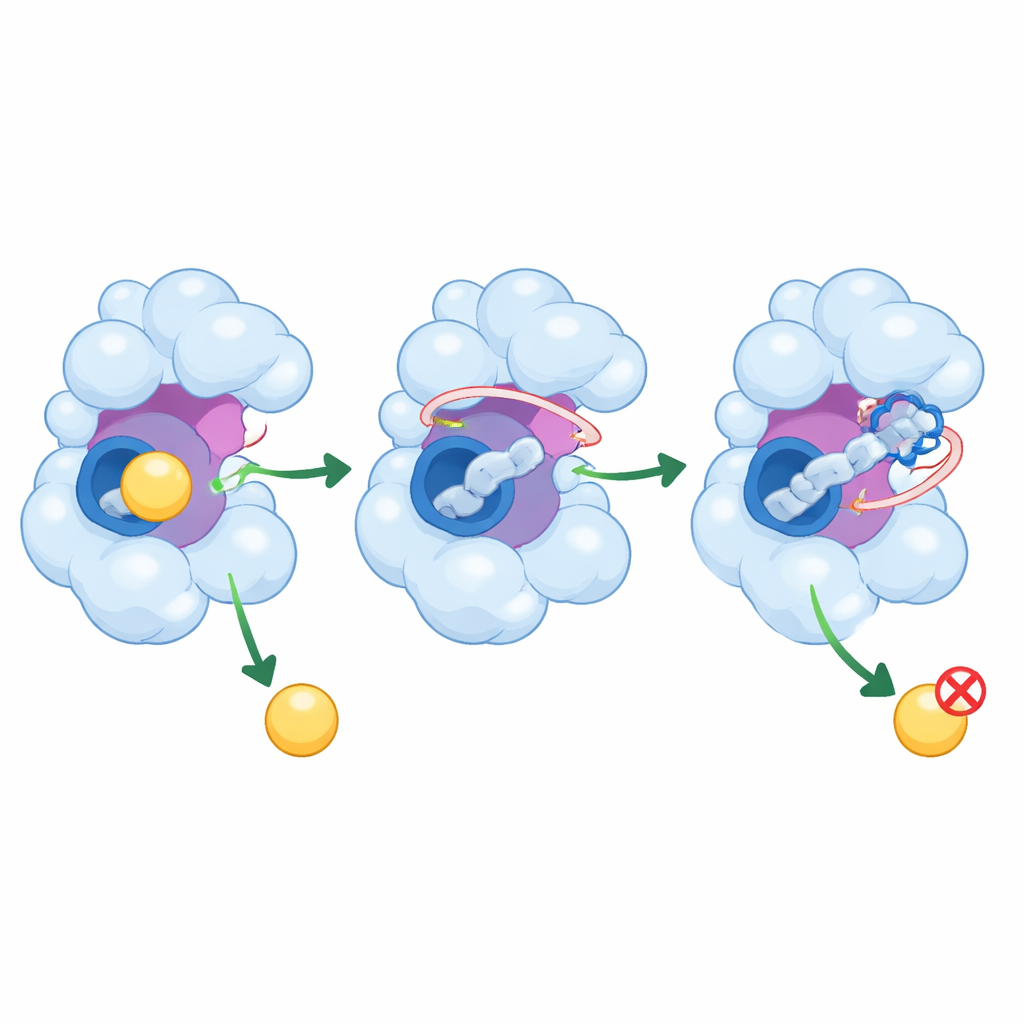
这些肽如何平抑过度活跃的酶
除了简单阻塞中央口袋外,PEP8和PEP44还延伸到GSK-3β的邻近区域,这些区域有助于控制其活性。它们与一段引导入侵分子的柔性环相互作用,而PEP44还与一个对酶催化至关重要的残基发生接触。模拟显示这些相互作用减少了蛋白关键部分的摆动,缩小了酶可采用构象的范围。随着活动部位部分被锁定且口袋更为拥挤,GSK-3β接纳其常见结合伙伴的能力下降,这可能转化为在细胞中产生较少有害的tau修饰和与淀粉样蛋白相关的变化。
这对未来疗法意味着什么
尽管这项工作完全在体外计算环境中完成——在计算机里而非活体大脑中——它为从天然食物蛋白到经精细调控的肽候选物铺就了一条明确路径,理论上可调低阿尔茨海默病的一个主要驱动因子。PEP8和PEP44作为最强的结合子尤为突出,它们以应妨害其有害作用的方式重塑酶的动力学。下一步需要实验室验证,以确认这些设计型牛奶片段能否到达大脑、在体内保持稳定并真正保护神经细胞。如果可以,它们有望成为一种受日常营养启发、温和且多功能的新型治疗手段的基础。
引用: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
关键词: 阿尔茨海默病, GSK-3β 抑制, 乳蛋白肽, κ-酪蛋白, 计算药物设计