Clear Sky Science · sv
Rationell design av κ-casein-peptider för att modulera GSK-3β-dynamik vid Alzheimers-terapi
Mjölkmolekyler och minne
Alzheimers sjukdom berövar människor gradvis deras minnen och självständighet, och dagens läkemedel gör lite för att stoppa den underliggande skadan i hjärnan. Denna studie utforskar en oväntat välbekant källa för nya behandlingsidéer: mjölk. Författarna använde avancerade datorsimuleringar för att omforma ett litet fragment av ett mjölkprotein så att det kan fästa vid ett centralt hjärnenzym kopplat till Alzheimer, och därigenom potentiellt dämpa några av de skadliga processer som driver sjukdomen.
Enzymet som vilseleder hjärnan
Vid Alzheimer skadas hjärnceller av trassliga tau-fibrer, klibbiga amyloidplack och sviktande förbindelser mellan neuroner. Ett enda enzym, kallat GSK-3β, bidrar till flera av dessa problem samtidigt. Det lägger kemiska markörer på tau-proteinet, vilket uppmuntrar det att klumpa ihop sig till trassel, och påverkar också hur amyloid bildas samt hur väl nervceller kommunicerar och svarar på insulinlika signaler. På grund av denna centrala roll ser många forskare GSK-3β som en huvudomkopplare för sjukdomsprogression och ett främsta mål för nya terapier.
Varför titta på mjölkproteiner?
Mjölk är mer än bara fett, socker och kalcium: det innehåller också proteiner som kan brytas ner till korta fragment, eller peptider, med förvånansvärt starka biologiska effekter. Tidigare arbete har antytt att mejerikonsumtion kan skydda mot kognitiv försämring, och att specifika mjölkderiverade peptider kan skydda hjärnan, minska skadlig enzymaktivitet och förbättra minnet i djurmodeller. Ett av mjölkens huvudproteiner, kasein, innehåller flera undertyper; bland dem har κ-casein varit relativt outforskad som källa till hjärnskyddande fragment. Författarna ville undersöka om en kort sträcka av κ-casein kunde formas till en effektiv blockare av GSK-3β.
Att designa smartare peptider på datorn
Teamet började med att förutsäga den tredimensionella strukturen av κ-casein och docka den mot GSK-3β för att hitta en del som ligger i enzymets ficka där energibärande molekyler normalt binder. De hittade ett segment på 10 aminosyror som redan visade hyggligt grepp. Genom detaljerade energiberäkningar identifierade de fyra positioner inom detta segment som bidrog svagt eller till och med ogynnsamt till bindningen. Med ett muteringsprediktionsverktyg bytte de systematiskt ut dessa fyra byggstenar mot alternativ som sannolikt skulle stärka interaktionen och byggde ett virtuellt bibliotek med 48 nya peptidvarianter. Säkerhetskontroller sorterade bort kandidater som förutspåddes vara toxiska eller allergena, vilket lämnade 22 som sedan dockades om mot GSK-3β.
Att smalna av de mest lovande kandidaterna
Dockningspoäng och interaktionskartor framhävde fyra framstående peptider, märkta PEP8, PEP36, PEP40 och PEP44. Alla fyra delade två nyckelförändringar som ersatte en neutral, oljig rest nära ena änden med en mer interaktiv rest, vilket hjälpte dem att förankras starkare i enzymets ficka. PEP8 och PEP44 gick längre och lade till en negativt laddad rest på en annan position, vilket ökade deras grepp. Datorsimuleringar körda över hundratals nanosekunder visade att när PEP8 eller PEP44 är bundna blir enzymets struktur något mer kompakt och mindre flexibel, särskilt runt fickan där dess naturliga mål normalt sitter. Dessa peptider skapade fler kontaktpunkter med enzymet än det ursprungliga mjölkfragmentet, vilket tyder på högre styrka och bättre selektivitet. Energianalyser bekräftade att PEP8 och PEP44 bildade de tightaste komplexen, drivet främst av kortdistansattraktioner och elektriska krafter mellan peptiden och enzymet.
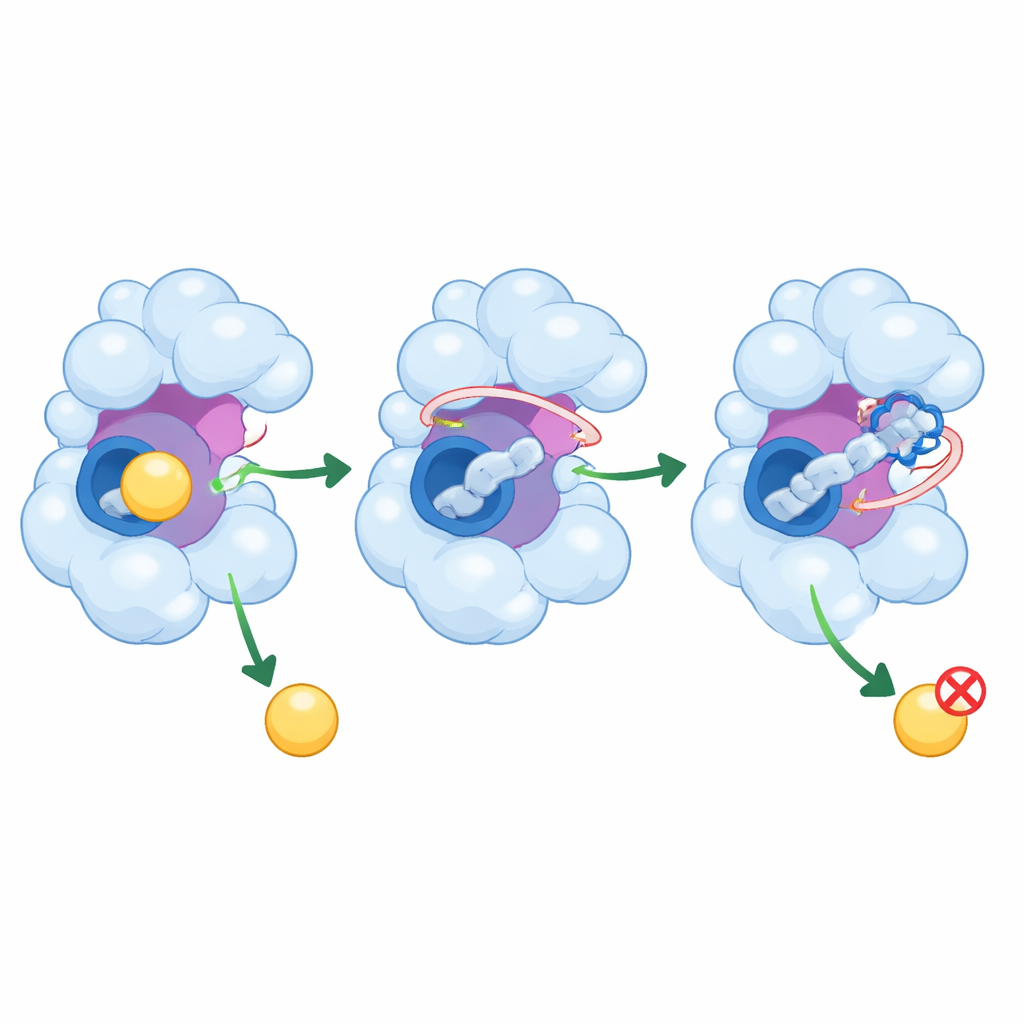
Hur dessa peptider kan dämpa ett löpskt enzym
Utöver att bara fylla den centrala fickan når PEP8 och PEP44 in i angränsande regioner av GSK-3β som hjälper till att kontrollera dess aktivitet. De interagerar med en flexibel loop som styr inkommande molekyler och, i fallet med PEP44, med en katalytisk rest som är avgörande för enzymets kemi. Simulationerna visar att dessa interaktioner minskar svängningarna i viktiga delar av proteinet och krymper spannet av former enzymet kan anta. Med sina rörliga delar delvis låsta och fickan mer trång, blir GSK-3β mindre kapabel att välkomna sina vanliga partners, vilket i verkliga celler kan översättas till minskad produktion av skadliga tau-modifikationer och amyloidrelaterade förändringar.
Vad detta kan innebära för framtida behandlingar
Även om detta arbete utfördes helt in silico — inne i datorer snarare än i levande hjärnor — kartlägger det en tydlig väg från ett naturligt födoprotein till noggrant avvägda peptidkandidater som i princip skulle kunna dämpa en huvudorsak till Alzheimers. PEP8 och PEP44 framstår som de starkaste bindarna, som omformar enzymets dynamik på sätt som bör hämma dess skadliga verksamhet. Nästa steg kräver laboratorietester för att bekräfta om dessa designade mjölkfragment kan nå hjärnan, förbli stabila i kroppen och verkligen skydda nervceller. Om så är fallet kan de utgöra grunden för en ny klass varsamt verkande, multitaskande behandlingar inspirerade av vardaglig kost.
Citering: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
Nyckelord: Alzheimers sjukdom, GSK-3β-hämning, mjölkpeptider, κ-casein, beräkningsbaserad läkemedelsdesign