Clear Sky Science · ar
التصميم العقلاني لببتيدات κ-كازين لتعديل ديناميكيات GSK-3β لعلاج مرض ألزهايمر
جزيئات الحليب والذاكرة
يسلب مرض ألزهايمر الناس ذكرياتهم واستقلاليتهم تدريجياً، والأدوية الحالية تفعل القليل لوقف التلف الأساسي في الدماغ. تستكشف هذه الدراسة مصدراً مألوفاً وغير متوقع لأفكار علاجية جديدة: الحليب. استخدم المؤلفون محاكاة حاسوبية متقدمة لإعادة تصميم مقطع صغير من بروتين الحليب بحيث يتمكن من الالتصاق بإنزيم دماغي رئيسي مرتبط بألزهايمر، مما قد يهدئ بعض العمليات الضارة التي تدفع المرض.
الإنزيم الذي يضلل الدماغ
في ألزهايمر، تلحق ألياف تاو المتشابكة والبلاكا اللزجة من الأميلويد وتفاقم الاتصالات بين الخلايا العصبية ضرراً بالخلايا الدماغية. إنزيم واحد يُدعى GSK-3β يساهم في دفع عدة من هذه المشاكل في آن واحد. يضيف علامات كيميائية على بروتين التاو، مما يشجعه على التكتل إلى تشابكات، كما يؤثر أيضاً في كيفية تكوّن الأميلويد وكذلك في كفاءة التواصل الخلوي العصبي واستجابة الخلايا لإشارات تشبه الإنسولين. بسبب هذا الدور المركزي، يرى العديد من الباحثين GSK-3β كمفتاح رئيسي لتقدم المرض وهدف رئيسي للعلاجات الجديدة.
لماذا النظر إلى بروتينات الحليب؟
الحليب أكثر من دهون وسكّر وكالسيوم: فهو يحتوي أيضاً على بروتينات يمكن تقسيمها إلى مقاطع قصيرة، أو ببتيدات، ذات تأثيرات بيولوجية قوية بصورة مدهشة. أشارت أعمال سابقة إلى أن تناول مشتقات الألبان قد يحمي من التدهور المعرفي، وأن ببتيدات محددة مشتقة من الحليب يمكن أن تحمي الدماغ، وتقلل نشاط إنزيمي ضار، وتحسّن الذاكرة في نماذج حيوانية. أحد البروتينات الرئيسية في الحليب، الكازين، يشمل أنماط فرعية متنوعة؛ ومن بينها κ-كازين الذي لم يُستكشف كثيراً كمصدر لمقاطع تحمي الدماغ. انطلق المؤلفون ليتحققوا مما إذا كان يمكن تشكيل مقطع قصير من κ-كازين إلى مانع قوي لـ GSK-3β.
تصميم ببتيدات أذكى على الحاسوب
بدأ الفريق بتوقع البنية ثلاثية الأبعاد لـ κ-كازين وربطها بإنزيم GSK-3β لاكتشاف جزء يستقر داخل جيب الإنزيم حيث ترتبط عادة الجزيئات الحاملة للطاقة. وجدوا مقطعاً مكوَّناً من 10 أحماض أمينية كان يمتلك بالفعل قبضة جيدة. باستخدام حسابات طاقة دقيقة، حدّدوا أربعة مواقع ضمن هذا المقطع تسهم ضعيفاً أو حتى سلبياً في الارتباط. ثم، بأداة لتوقع الطفرات، استبدلوا منهجياً هذه الوحدات الأربع ببدائل من المرجح أن تقوي التفاعل، مبنيين مكتبة افتراضية تضم 48 متغيراً جديداً للببتيد. أزالت فحوصات السلامة أي مرشحين متوقعين أن يكونوا سامة أو مسببة للحساسية، متبقية بـ22 أعيدت محاكاتها على GSK-3β.
تضييق الخيارات الواعدة
أشارت درجات الارتباط وخرائط التداخل إلى أربعة ببتيدات بارزة، مُعنونة PEP8 وPEP36 وPEP40 وPEP44. شاركت كلها تعديلين رئيسيين استبدلا بقاعدة متعادلة وزيتية بالقرب من أحد الطرفين بأخرى أكثر تفاعلية، مما ساعدها على التثبيت بقوة أكبر في جيب الإنزيم. تقدمت PEP8 وPEP44 أبعد من ذلك بإضافة بقاعدة سالبة الشحنة في موقع آخر، مما عزز قبضتهما. أظهرت محاكاة الحاسوب التي استمرت لمئات النانوثواني أنه عندما يرتبط PEP8 أو PEP44، تصبح بنية الإنزيم أكثر إحكاماً وأقل مرونة قليلاً، خاصة حول الجيب حيث تجلس أهدافه الطبيعية عادةً. شكلت هذه الببتيدات نقاط اتصال أكثر مع الإنزيم مقارنة بالمقطع الأصلي من الحليب، مما يشير إلى قوة وانتقائية أعلى. أكدت تحليلات الطاقة أن PEP8 وPEP44 شكلتا أكثر المركبات تماسكاً، مدفوعة بشكل رئيسي بالجاذبيات قصيرة المدى والقوى الكهربائية بين الببتيد والإنزيم.
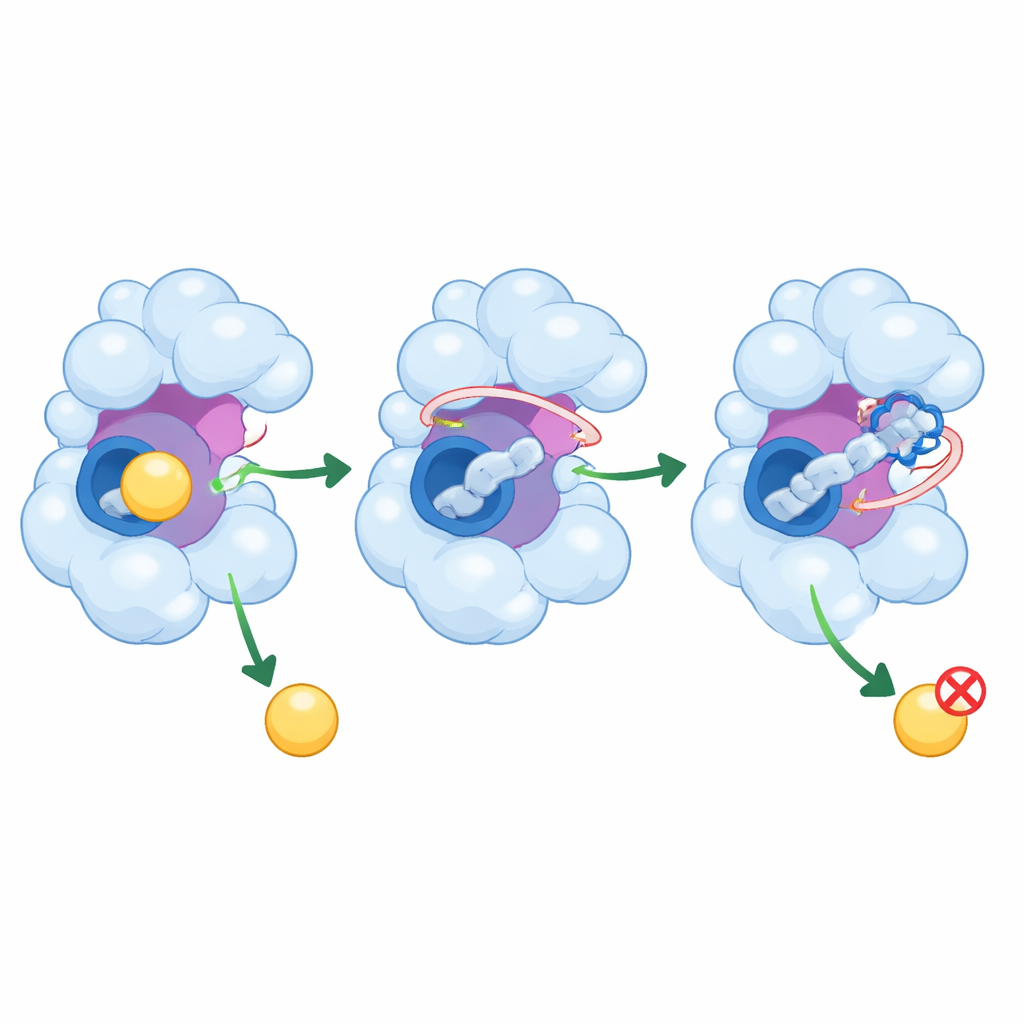
كيف قد تهدئ هذه الببتيدات إنزيماً خارقاً
خلافاً لكونها مجرد سد للجيب المركزي، يمتد PEP8 وPEP44 إلى مناطق مجاورة في GSK-3β تساهم في التحكم بنشاطه. تتفاعل مع حلقة مرنة توجه الجزيئات الداخلة ومع، في حالة PEP44، بقاعدة تَفَعِّلية حاسمة لكيمياء الإنزيم. تُظهر المحاكاة أن هذه التداخلات تقلل من اهتزاز الأجزاء المهمة من البروتين، مقلصة نطاق الأشكال التي يمكن للإنزيم تبنّيها. مع جزئياته المتحركة المقيدة جزئياً وجيبه المزحوم أكثر، يصبح GSK-3β أقل قدرة على استقبال شركائه المعتادين، وهو ما قد يترجم إلى تقليل إنتاج تعديلات التاو الضارة والتغيرات المتعلقة بالأميلويد في الخلايا الحية.
ما الذي قد يعنيه هذا لعلاجات المستقبل
رغم أن هذا العمل نُفِّذ كلياً محاسبينياً—داخل الحواسيب بدلاً من أدمغة حية—إلا أنه يوضح مساراً واضحاً من بروتين غذائي طبيعي إلى مرشحين ببتيديين مضبوطين بعناية يمكنهم، من حيث المبدأ، تخفيف نشاط محرك رئيسي للألزهايمر. تبرز PEP8 وPEP44 كأقوى الرابطين، حيث يعيدان تشكيل ديناميكيات الإنزيم بطرق من المفترض أن تعوق أفعاله الضارة. الخطوات التالية ستتطلب اختبارات مخبرية للتأكد مما إذا كانت هذه المقاطع المصممة من الحليب قادرة على الوصول إلى الدماغ، والبقاء مستقرة في الجسم، وحماية الخلايا العصبية فعلياً. إذا نجحت، فقد تشكل أساس فئة جديدة من العلاجات اللطيفة ومتعددة المهام المستوحاة من تغذية يومية.
الاستشهاد: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
الكلمات المفتاحية: داء ألزهايمر, تثبيط GSK-3β, ببتيدات الحليب, κ-كازين, تصميم دوائي حاسوبي