Clear Sky Science · nl
Rationeel ontwerp van κ-caseïnepeptiden om GSK-3β-dynamica te moduleren voor de behandeling van Alzheimer
Melkmoleculen en geheugen
De ziekte van Alzheimer berooft mensen geleidelijk van hun herinneringen en zelfstandigheid, en de huidige medicijnen doen weinig om de onderliggende schade in de hersenen te stoppen. Deze studie onderzoekt een onverwacht vertrouwde bron voor nieuwe behandelingsideeën: melk. De auteurs gebruikten geavanceerde computersimulaties om een klein fragment van een melkproteïne opnieuw te ontwerpen zodat het zich kan vasthechten aan een sleutelenzym in de hersenen dat met Alzheimer wordt geassocieerd, en mogelijk enkele van de schadelijke processen die de ziekte aandrijven kan kalmeren.
Het enzym dat de hersenen misleidt
Bij Alzheimer worden hersencellen aangetast door verwarde tauvezels, kleverige amyloïdeplakken en falende verbindingen tussen neuronen. Eén enkel enzym, genaamd GSK-3β, draagt tegelijk bij aan meerdere van deze problemen. Het voegt chemische tags toe aan het tau-eiwit, waarmee het aanzet tot klontering tot verdraaiingen, en het beïnvloedt ook hoe amyloïde wordt gevormd, evenals hoe goed zenuwcellen communiceren en reageren op insulineachtige signalen. Vanwege deze centrale rol zien veel onderzoekers GSK-3β als een hoofdschakelaar voor ziekteprogressie en een belangrijk doelwit voor nieuwe therapieën.
Waarom naar melkproteïnen kijken?
Melk is meer dan vet, suiker en calcium: het bevat ook eiwitten die kunnen worden opgesplitst in korte fragmenten, of peptiden, met verrassend sterke biologische effecten. Eerder onderzoek suggereerde dat zuivelconsumptie mogelijk beschermt tegen cognitieve achteruitgang, en dat specifieke uit melk afkomstige peptiden de hersenen kunnen beschermen, schadelijke enzymactiviteit kunnen verminderen en het geheugen in diermodellen kunnen verbeteren. Een van de belangrijkste melkeiwitten, caseïne, omvat verschillende subtypes; onder hen is κ-caseïne relatief onontgonnen als bron van hersenbeschermende fragmenten. De auteurs wilden nagaan of een korte reeks van κ-caseïne kon worden omgevormd tot een krachtige remmer van GSK-3β.
Slimmere peptiden ontwerpen op de computer
Het team begon met het voorspellen van de driedimensionale structuur van κ-caseïne en koppelde het aan GSK-3β om een gedeelte te vinden dat in het zakje van het enzym past waar normaal energiedragende moleculen binden. Ze vonden een segment van 10 aminozuren dat al een redelijke grip liet zien. Met behulp van gedetailleerde energieberekeningen identificeerden ze vier posities binnen dit segment die zwak of zelfs ongunstig bijdroegen aan de binding. Vervolgens wisselden ze met een mutatievoorspellingsinstrument systematisch deze vier bouwstenen voor alternatieven die waarschijnlijk de interactie zouden versterken, en bouwden zo een virtuele bibliotheek van 48 nieuwe peptidevarianten. Veiligheidscontroles verwijderden kandidaten die als toxisch of allergeen werden voorspeld, waardoor 22 overbleven die opnieuw op GSK-3β werden gedockt.
De meest veelbelovende kandidaten verfijnen
Dockingscores en interactiekaarten belichtten vier opvallende peptiden, aangeduid als PEP8, PEP36, PEP40 en PEP44. Alle vier deelden twee sleutelwijzigingen die een neutraal, olieachtig residu aan één uiteinde vervingen door een meer interactief residu, waardoor ze zich steviger in het enzymzakje verankerden. PEP8 en PEP44 gingen verder door op een andere positie een negatief geladen residu toe te voegen, wat hun grip versterkte. Computersimulaties die honderden nanoseconden duurden, toonden aan dat wanneer PEP8 of PEP44 gebonden is, de structuur van het enzym iets compacter en minder flexibel wordt, vooral rond het zakje waar de natuurlijke doelmoleculen gewoonlijk zitten. Deze peptiden maakten meer contactpunten met het enzym dan het oorspronkelijke melkfragment, wat wijst op grotere sterkte en betere selectiviteit. Energieberekeningen bevestigden dat PEP8 en PEP44 de meest sterke complexen vormden, voornamelijk gedreven door kortafstandsaantrekkingen en elektrische krachten tussen het peptide en het enzym.
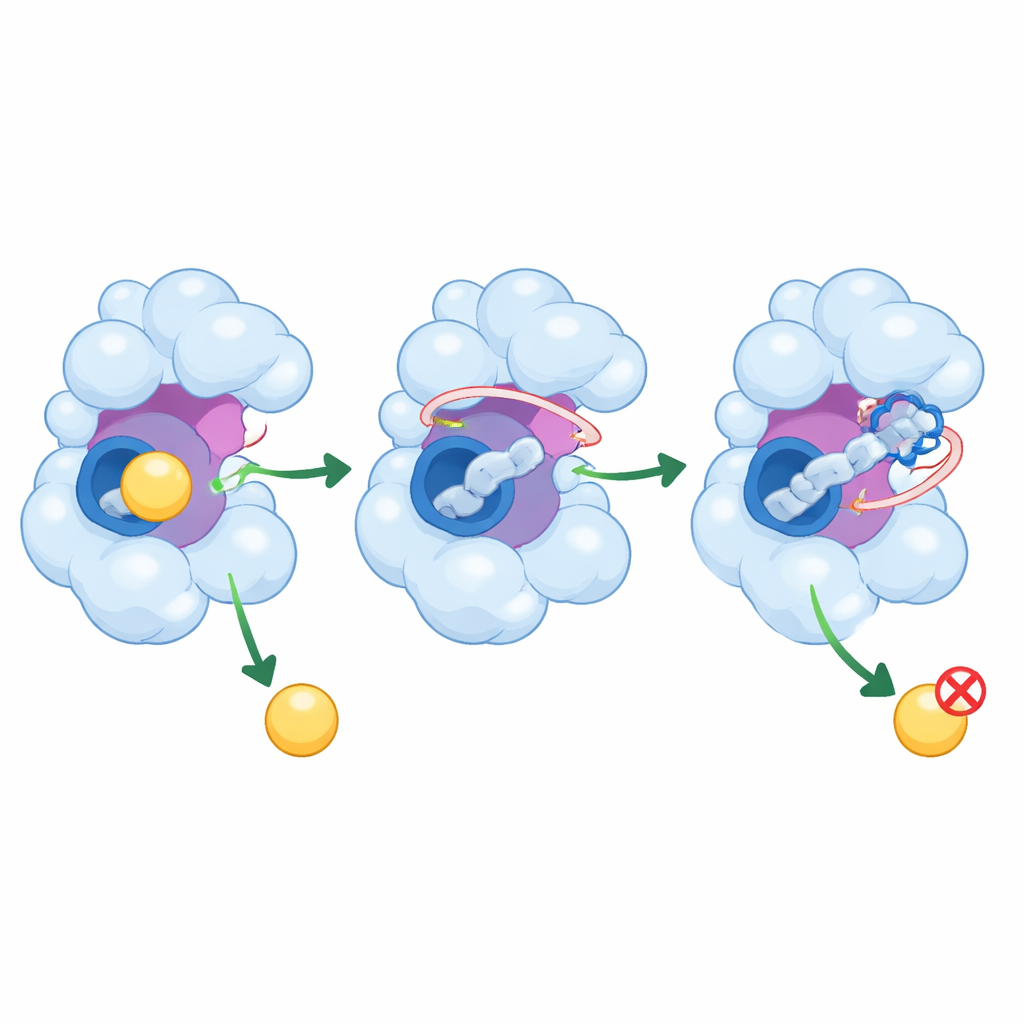
Hoe deze peptiden een uit de hand gelopen enzym kunnen kalmeren
Naast het simpelweg verstoppen van het centrale zakje reiken PEP8 en PEP44 in aangrenzende regio’s van GSK-3β die helpen de activiteit te regelen. Ze interageren met een flexibele lus die binnenkomende moleculen begeleidt en, in het geval van PEP44, met een katalytisch residu dat cruciaal is voor de chemie van het enzym. De simulaties laten zien dat deze interacties het wiebelen van belangrijke delen van het eiwit verminderen, waardoor het bereik van vormen dat het enzym kan aannemen kleiner wordt. Met bewegende delen die deels vastgezet zijn en een drukker zakje is GSK-3β minder in staat zijn gebruikelijke partners te verwelkomen, wat kan resulteren in verminderde productie van schadelijke tau-modificaties en amyloïdegerelateerde veranderingen in echte cellen.
Wat dit kan betekenen voor toekomstige behandelingen
Hoewel dit werk volledig in silico — binnen computers in plaats van in levende hersenen — is uitgevoerd, schetst het een helder traject van een natuurlijk voedingsproteïne naar zorgvuldig afgestemde peptidekandidaten die in principe een belangrijke Alzheimer-driver kunnen temperen. PEP8 en PEP44 springen eruit als de sterkste binders, die de dynamiek van het enzym zo hervormen dat diens schadelijke acties zouden moeten worden belemmerd. De volgende stappen vereisen laboratoriumtesten om te bevestigen of deze ontworpen melkfragmenten de hersenen kunnen bereiken, stabiel blijven in het lichaam en daadwerkelijk zenuwcellen beschermen. Als dat het geval is, zouden ze de basis kunnen vormen voor een nieuwe klasse zachte, multitaskende behandelingen geïnspireerd door alledaagse voeding.
Bronvermelding: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
Trefwoorden: Ziekte van Alzheimer, Remming van GSK-3β, melkpeptiden, κ-caseïne, computationeel geneesmiddelontwerp