Clear Sky Science · de
Rationales Design von κ‑Casein‑Peptiden zur Modulation der GSK‑3β‑Dynamik für die Alzheimer‑Therapie
Milchmoleküle und Gedächtnis
Die Alzheimer‑Krankheit raubt Menschen nach und nach ihre Erinnerungen und ihre Selbstständigkeit, und die heutigen Medikamente verhindern kaum den zugrundeliegenden Schaden im Gehirn. Diese Studie untersucht eine überraschend vertraute Quelle für neue Behandlungsideen: Milch. Die Autoren nutzten fortgeschrittene Computersimulationen, um ein winziges Fragment eines Milchproteins neu zu entwerfen, damit es an ein zentrales Hirnenzym bindet, das mit Alzheimer in Verbindung steht, und möglicherweise einige der schädlichen Prozesse dämpft, die die Krankheit vorantreiben.
Das Enzym, das das Gehirn fehlleitet
Bei Alzheimer werden Nervenzellen durch verknotete Tau‑Fasern, klebrige Amyloid‑Plaques und versagende Verbindungen zwischen Neuronen geschädigt. Ein einzelnes Enzym, genannt GSK‑3β, trägt auf mehrere Arten zu diesen Problemen bei. Es fügt dem Tau‑Protein chemische Markierungen hinzu, die seine Aggregation zu Fibrillen fördern, und beeinflusst außerdem die Amyloid‑Bildung sowie die Funktion neuronaler Kommunikation und insulinähnlicher Signalwege. Wegen dieser zentralen Rolle sehen viele Forscher GSK‑3β als Schlüsselschalter des Krankheitsverlaufs und als ein vorrangiges Ziel für neue Therapien.
Warum Milchproteine betrachten?
Milch ist mehr als Fett, Zucker und Kalzium: Sie enthält auch Proteine, die in kurze Fragmente, sogenannte Peptide, zerschnitten werden können und überraschend starke biologische Effekte besitzen. Frühere Arbeiten deuteten an, dass der Verzehr von Milch gegen kognitiven Abbau schützen könnte und dass spezifische, aus Milch stammende Peptide das Gehirn schützen, schädliche Enzymaktivitäten reduzieren und das Gedächtnis in Tiermodellen verbessern können. Eines der Hauptproteine der Milch, Casein, umfasst verschiedene Subtypen; darunter wurde κ‑Casein als Quelle gehirnschützender Fragmente bisher vergleichsweise wenig erforscht. Die Autoren wollten herausfinden, ob ein kurzer Abschnitt von κ‑Casein so gestaltet werden kann, dass er ein wirksamer Hemmer von GSK‑3β wird.
Intelligentere Peptide am Computer entwerfen
Das Team begann damit, die dreidimensionale Struktur von κ‑Casein vorherzusagen und sie gegen GSK‑3β zu docken, um einen Abschnitt zu finden, der sich in die Tasche des Enzyms einfügt, in der normalerweise energietragende Moleküle binden. Sie identifizierten ein Segment von zehn Aminosäuren, das bereits guten Halt zeigte. Mithilfe detaillierter Energieberechnungen lokalisierte man vier Positionen innerhalb dieses Segments, die nur schwach oder sogar ungünstig zur Bindung beitrugen. Dann wurden mit einem Mutations‑Vorhersagewerkzeug systematisch diese vier Bausteine gegen Alternativen ausgetauscht, die die Wechselwirkung wahrscheinlich stärken würden, und es entstand eine virtuelle Bibliothek von 48 neuen Peptidvarianten. Sicherheitsprüfungen schieden Kandidaten aus, die als toxisch oder allergen vorhergesagt wurden, sodass 22 übrig blieben, die anschließend erneut auf GSK‑3β gedockt wurden.
Die vielversprechendsten Kandidaten eingrenzen
Docking‑Werte und Interaktionskarten hoben vier herausragende Peptide hervor, bezeichnet als PEP8, PEP36, PEP40 und PEP44. Alle vier teilten zwei Schlüsseländerungen: Ein neutrales, hydrophobes Rest wurde nahe einem Ende durch einen interaktiveren Rest ersetzt, was half, sie fester in der Enzymtasche zu verankern. PEP8 und PEP44 gingen weiter und fügten an einer anderen Position eine negativ geladene Seitenkette hinzu, die ihren Halt weiter verstärkte. Computersimulationen über Hunderte von Nanosekunden zeigten, dass bei Bindung von PEP8 oder PEP44 die Enzymstruktur etwas kompakter und weniger flexibel wurde, besonders in der Region um die Tasche, in der normalerweise seine natürlichen Liganden sitzen. Diese Peptide bildeten mehr Kontaktpunkte mit dem Enzym als das ursprüngliche Milchfragment, was auf höhere Bindungsstärke und bessere Selektivität schließen lässt. Energieanalysen bestätigten, dass PEP8 und PEP44 die stabilsten Komplexe bildeten, hauptsächlich getrieben von kurzreichweitigen Anziehungen und elektrostatischen Kräften zwischen Peptid und Enzym.
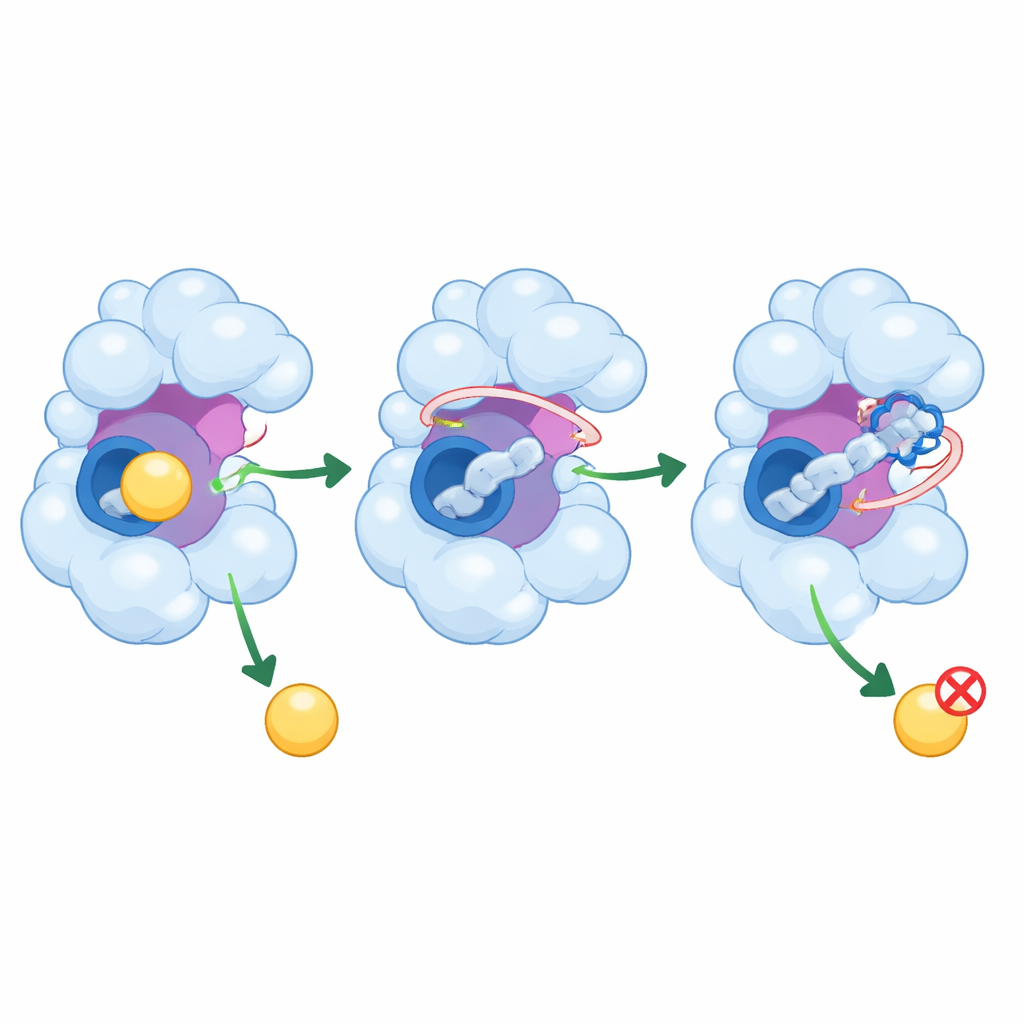
Wie diese Peptide ein entfesseltes Enzym beruhigen könnten
Über das bloße Verstopfen der zentralen Tasche hinaus reichen PEP8 und PEP44 in benachbarte Regionen von GSK‑3β, die dessen Aktivität mitkontrollieren. Sie interagieren mit einer flexiblen Schleife, die eintretende Moleküle leitet, und im Fall von PEP44 mit einer katalytisch wichtigen Aminosäure, die für die chemische Aktivität des Enzyms entscheidend ist. Die Simulationen zeigen, dass diese Wechselwirkungen das Zittern wichtiger Proteinbereiche reduzieren und die Bandbreite der möglichen Enzymkonformationen einschränken. Mit teilweise blockierten beweglichen Teilen und einer engeren Tasche ist GSK‑3β weniger fähig, seine üblichen Bindungspartner aufzunehmen, was in Zellen zu einer verminderten Produktion schädlicher Tau‑Modifikationen und amyloidbedingter Veränderungen führen könnte.
Was das für zukünftige Behandlungen bedeuten könnte
Auch wenn diese Arbeit vollständig in silico—also am Computer und nicht in lebenden Gehirnen—durchgeführt wurde, skizziert sie einen klaren Weg von einem natürlichen Lebensmittelprotein zu sorgfältig abgestimmten Peptidkandidaten, die prinzipiell einen wichtigen Alzheimer‑Treiber dämpfen könnten. PEP8 und PEP44 stechen als die stärksten Binder hervor, da sie die Dynamik des Enzyms so verändern, dass dessen schädliche Aktionen gehemmt werden sollten. Die nächsten Schritte erfordern Laboruntersuchungen, um zu bestätigen, ob diese konstruierten Milchfragmente das Gehirn erreichen, im Körper stabil bleiben und Nervenzellen tatsächlich schützen. Falls ja, könnten sie die Grundlage für eine neue Klasse schonender, multi‑wirksamer Behandlungen bilden, die von alltäglicher Ernährung inspiriert sind.
Zitation: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
Schlüsselwörter: Alzheimer‑Krankheit, GSK‑3β‑Hemmung, Milchpeptide, κ‑Casein, computergestützte Wirkstoffentwicklung