Clear Sky Science · it
Progettazione razionale di peptidi di κ-caseina per modulare la dinamica di GSK-3β nella terapia dell’Alzheimer
Molecole del latte e memoria
La malattia di Alzheimer spoglia lentamente le persone dei loro ricordi e della loro autonomia, e i farmaci attuali fanno poco per fermare il danno sottostante nel cervello. Questo studio esplora una fonte inaspettatamente familiare per nuove idee terapeutiche: il latte. Gli autori hanno utilizzato simulazioni computerizzate avanzate per riprogettare un piccolo frammento di una proteina del latte in modo che possa legarsi a un enzima cerebrale chiave associato all’Alzheimer, potenzialmente attenuando alcuni dei processi dannosi che guidano la malattia.
L’enzima che disorienta il cervello
Nell’Alzheimer le cellule cerebrali vengono danneggiate da fibre tau aggrovigliate, placche amiloidi appiccicose e dal cedimento delle connessioni tra i neuroni. Un singolo enzima, chiamato GSK-3β, contribuisce a più di questi problemi contemporaneamente. Aggiunge marcatori chimici alla proteina tau, favorendone l’aggregazione in grovigli, e influenza anche la formazione dell’amiloide, oltre a modulare la comunicazione neuronale e la risposta a segnali simili all’insulina. Per questo ruolo centrale, molti ricercatori vedono GSK-3β come un interruttore maestro della progressione della malattia e un bersaglio primario per nuove terapie.
Perché guardare alle proteine del latte?
Il latte non è soltanto grassi, zuccheri e calcio: contiene anche proteine che possono essere spezzate in brevi frammenti, o peptidi, con effetti biologici sorprendentemente potenti. Studi precedenti avevano suggerito che il consumo di latticini potesse proteggere dal declino cognitivo e che peptidi derivati dal latte potessero proteggere il cervello, ridurre l’attività di enzimi nocivi e migliorare la memoria in modelli animali. Una delle proteine principali del latte, la caseina, include diverse sottotipi; tra questi, la κ-caseina è stata relativamente poco esplorata come fonte di frammenti protettivi per il cervello. Gli autori si sono posti l’obiettivo di verificare se un breve tratto di κ-caseina potesse essere modellato in un efficace bloccante di GSK-3β.
Progettare peptidi più intelligenti al computer
Il team ha iniziato prevedendo la struttura tridimensionale della κ-caseina e l’ha fatta “docking” contro GSK-3β per individuare una porzione che si adattasse alla tasca dell’enzima dove normalmente si legano le molecole che trasportano energia. Hanno individuato un segmento di 10 aminoacidi che mostrava già una presa discreta. Utilizzando calcoli energetici dettagliati, hanno identificato quattro posizioni all’interno di questo segmento che contribuivano debolmente o addirittura in modo sfavorevole al legame. Poi, con uno strumento di predizione delle mutazioni, hanno sostituito sistematicamente questi quattro elementi con alternative probabilmente in grado di rafforzare l’interazione, costruendo una libreria virtuale di 48 nuove varianti peptidiche. Controlli di sicurezza hanno eliminato i candidati previsti come tossici o allergenici, lasciandone 22 che sono stati quindi ridedockati su GSK-3β.
Selezionare i candidati più promettenti
I punteggi di docking e le mappe di interazione hanno evidenziato quattro peptidi di spicco, etichettati PEP8, PEP36, PEP40 e PEP44. Tutti e quattro condividevano due cambiamenti chiave che sostituivano un residuo neutro, apolare vicino a un’estremità con uno più interattivo, aiutandoli ad ancorarsi con maggiore fermezza nella tasca dell’enzima. PEP8 e PEP44 sono andati oltre, aggiungendo un residuo carico negativamente in un’altra posizione, il che ha aumentato ulteriormente la loro presa. Simulazioni al computer eseguite per centinaia di nanosecondi hanno mostrato che quando PEP8 o PEP44 sono legati, la struttura dell’enzima diventa leggermente più compatta e meno flessibile, soprattutto attorno alla tasca dove si piazzerebbero i suoi bersagli naturali. Questi peptidi stabilivano più punti di contatto con l’enzima rispetto al frammento originario del latte, suggerendo maggiore forza e migliore selettività. Analisi energetiche hanno confermato che PEP8 e PEP44 formavano i complessi più stabili, guidati principalmente da attrazioni a corto raggio e forze elettriche tra il peptide e l’enzima.
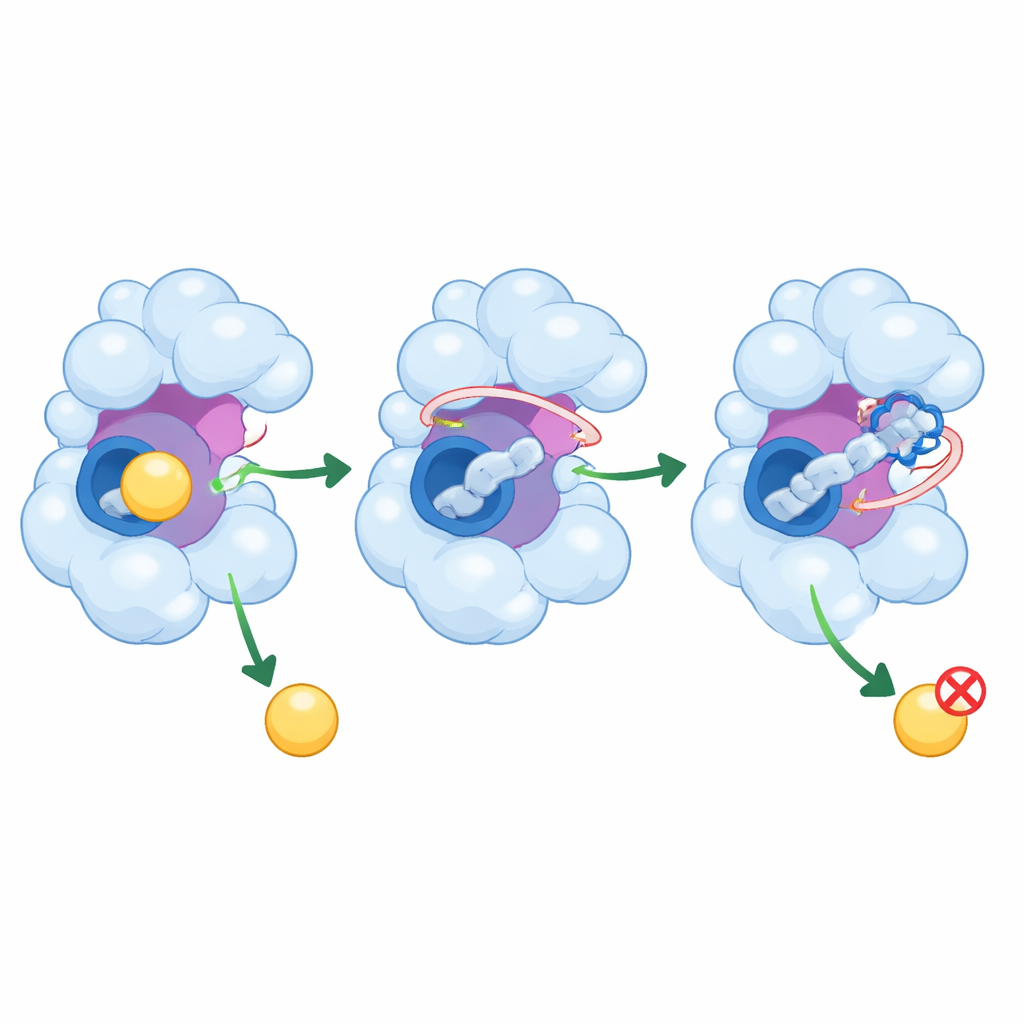
Come questi peptidi potrebbero calmare un enzima fuori controllo
Oltre a occupare la tasca centrale, PEP8 e PEP44 si estendono in regioni adiacenti di GSK-3β che contribuiscono a regolarne l’attività. Interagiscono con un loop flessibile che guida le molecole in arrivo e, nel caso di PEP44, con un residuo catalitico cruciale per la chimica dell’enzima. Le simulazioni mostrano che queste interazioni riducono le oscillazioni delle parti importanti della proteina, restringendo la gamma di conformazioni che l’enzima può assumere. Con i suoi elementi mobili in parte bloccati e la tasca più affollata, GSK-3β è meno in grado di accogliere i suoi partner abituali, il che potrebbe tradursi in una minore produzione delle modifiche dannose della tau e di cambiamenti legati all’amiloide nelle cellule reali.
Cosa potrebbe significare per i trattamenti futuri
Pur essendo stato condotto interamente in silico — nei computer piuttosto che in cervelli viventi — questo lavoro traccia un percorso chiaro da una proteina alimentare naturale a candidati peptidici accuratamente ottimizzati che potrebbero, in linea di principio, attenuare un importante fattore dell’Alzheimer. PEP8 e PEP44 emergono come i leganti più efficaci, rimodellando la dinamica dell’enzima in modi che dovrebbero ostacolarne le azioni dannose. I passaggi successivi richiederanno test di laboratorio per confermare se questi frammenti di latte progettati possono raggiungere il cervello, rimanere stabili nell’organismo e proteggere realmente le cellule nervose. Se ciò accadrà, potrebbero costituire la base di una nuova classe di trattamenti delicati e multitasking ispirati alla nutrizione quotidiana.
Citazione: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
Parole chiave: Malattia di Alzheimer, Inibizione di GSK-3β, peptidi del latte, κ-caseina, progettazione computazionale di farmaci