Clear Sky Science · fr
Conception rationnelle de peptides de κ‑caséine pour moduler la dynamique de GSK‑3β en vue d’une thérapie de la maladie d’Alzheimer
Molécules du lait et mémoire
La maladie d’Alzheimer prive progressivement les personnes de leurs souvenirs et de leur autonomie, et les traitements actuels font peu pour arrêter les dommages sous‑jacents dans le cerveau. Cette étude explore une source de traitements inattendue et familière : le lait. Les auteurs ont utilisé des simulations informatiques avancées pour redesigner un petit fragment d’une protéine du lait afin qu’il puisse se fixer sur une enzyme clé du cerveau liée à Alzheimer, apaisant potentiellement certains des processus néfastes qui alimentent la maladie.
L’enzyme qui mène le cerveau à l’erreur
Dans la maladie d’Alzheimer, les cellules cérébrales sont endommagées par des fibres de tau emmêlées, des plaques amyloïdes adhésives et des connexions neuronales défaillantes. Une seule enzyme, appelée GSK‑3β, contribue à plusieurs de ces problèmes à la fois. Elle ajoute des marques chimiques à la protéine tau, favorisant son agglutination en enchevêtrements, et influence aussi la formation de l’amyloïde ainsi que la communication des cellules nerveuses et leur réponse aux signaux de type insulinoïde. En raison de ce rôle central, de nombreux chercheurs considèrent GSK‑3β comme un commutateur maître de la progression de la maladie et une cible de choix pour de nouvelles thérapies.
Pourquoi s’intéresser aux protéines du lait ?
Le lait n’est pas seulement composé de lipides, de sucres et de calcium : il contient aussi des protéines qui peuvent être découpées en courts fragments, ou peptides, aux effets biologiques étonnamment puissants. Des travaux antérieurs ont suggéré qu’une consommation de produits laitiers pourrait protéger contre le déclin cognitif, et que des peptides dérivés du lait peuvent protéger le cerveau, réduire l’activité d’enzymes nuisibles et améliorer la mémoire dans des modèles animaux. L’une des principales protéines du lait, la caséine, comprend plusieurs sous‑types ; parmi eux, la κ‑caséine a été relativement peu explorée comme source de fragments protecteurs pour le cerveau. Les auteurs se sont demandé si un court segment de κ‑caséine pouvait être façonné en un bloqueur puissant de GSK‑3β.
Concevoir des peptides plus intelligents sur ordinateur
L’équipe a commencé par prédire la structure tridimensionnelle de la κ‑caséine et l’a mis en appariement (docké) contre GSK‑3β pour trouver une portion qui s’enfonce dans la poche de l’enzyme où se fixent normalement les molécules porteuses d’énergie. Ils ont identifié un segment de 10 acides aminés qui présentait déjà une tenue correcte. À l’aide de calculs énergétiques détaillés, ils ont repéré quatre positions au sein de ce segment qui contribuaient faiblement ou même défavorablement à la liaison. Puis, avec un outil de prédiction de mutations, ils ont systématiquement remplacé ces quatre éléments constitutifs par des alternatives susceptibles de renforcer l’interaction, construisant une bibliothèque virtuelle de 48 nouvelles variantes peptidiques. Des contrôles de sécurité ont éliminé les candidats prédits toxiques ou allergènes, ne conservant que 22 peptides qui ont ensuite été redockés sur GSK‑3β.
Restreindre les candidats les plus prometteurs
Les scores de docking et les cartes d’interaction ont mis en évidence quatre peptides remarquables, étiquetés PEP8, PEP36, PEP40 et PEP44. Les quatre partageaient deux modifications clés qui remplaçaient un résidu neutre, hydrophobe, près d’une extrémité par un résidu plus interagissant, les aidant à s’ancrer plus fermement dans la poche de l’enzyme. PEP8 et PEP44 ont été plus loin en ajoutant un résidu chargé négativement à une autre position, ce qui a renforcé leur tenue. Des simulations informatiques sur plusieurs centaines de nanosecondes ont montré que lorsque PEP8 ou PEP44 est lié, la structure de l’enzyme devient légèrement plus compacte et moins flexible, en particulier autour de la poche où se logent habituellement ses cibles naturelles. Ces peptides établissent plus de points de contact avec l’enzyme que le fragment initial du lait, suggérant une plus grande affinité et une meilleure sélectivité. Des analyses énergétiques ont confirmé que PEP8 et PEP44 formaient les complexes les plus serrés, principalement portés par des attractions à courte portée et des forces électrostatiques entre le peptide et l’enzyme.
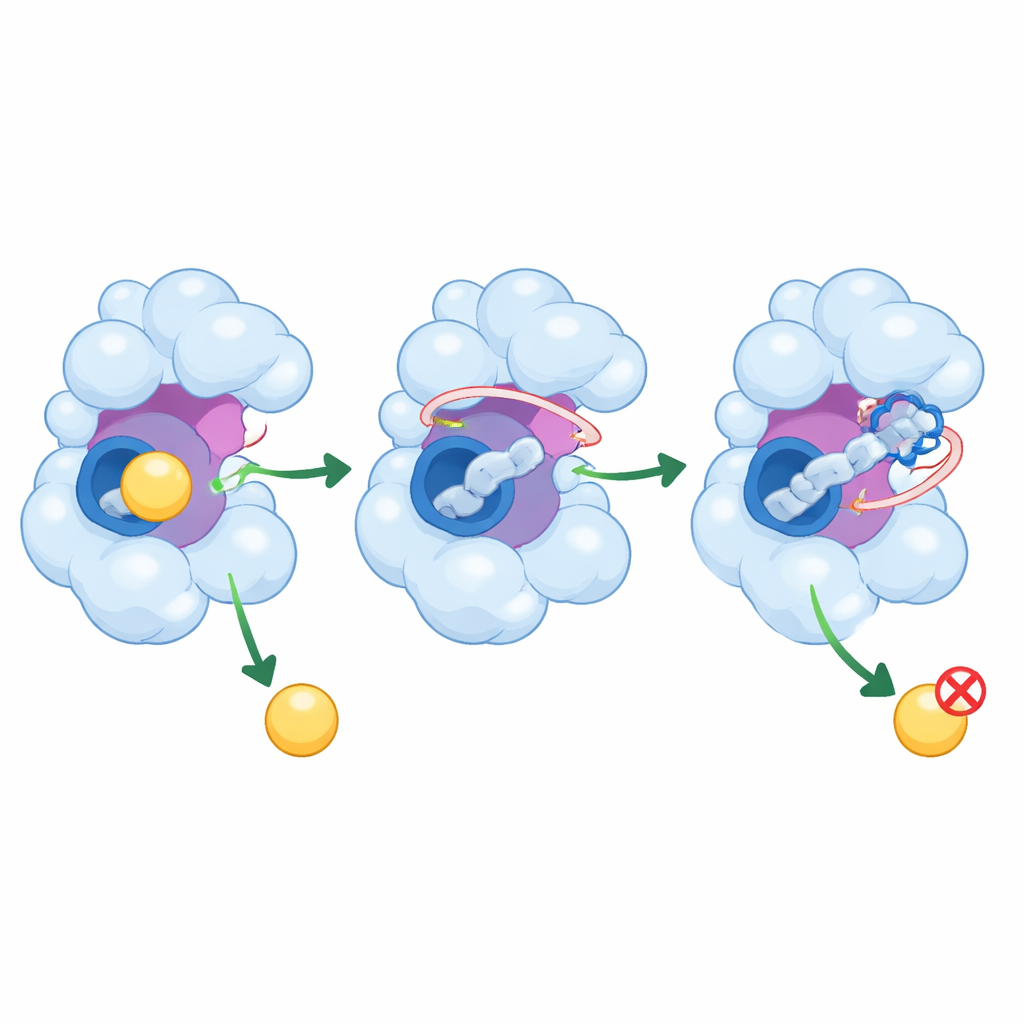
Comment ces peptides pourraient calmer une enzyme déréglée
Au‑delà de simplement obstruer la poche centrale, PEP8 et PEP44 s’étendent dans des régions voisines de GSK‑3β qui contribuent au contrôle de son activité. Ils interagissent avec une boucle flexible qui guide les molécules entrantes et, dans le cas de PEP44, avec un résidu catalytique crucial pour la chimie de l’enzyme. Les simulations montrent que ces interactions réduisent l’oscillation de parties importantes de la protéine, diminuant l’éventail de conformations que l’enzyme peut adopter. Ses éléments mobiles étant partiellement verrouillés et sa poche plus encombrée, GSK‑3β est moins apte à accueillir ses partenaires habituels, ce qui pourrait se traduire par une diminution de la production de modifications nocives de la tau et des changements liés à l’amyloïde dans des cellules réelles.
Ce que cela pourrait signifier pour les traitements futurs
Bien que ce travail ait été mené entièrement in silico — dans des ordinateurs plutôt que dans des cerveaux vivants — il trace une voie claire allant d’une protéine alimentaire naturelle à des candidats peptidiques finement ajustés qui pourraient, en principe, réduire l’activité d’un acteur majeur d’Alzheimer. PEP8 et PEP44 se distinguent comme les ligands les plus forts, remodelant la dynamique de l’enzyme de manière à gêner ses actions délétères. Les étapes suivantes nécessiteront des tests en laboratoire pour confirmer si ces fragments de lait conçus peuvent atteindre le cerveau, rester stables dans l’organisme et protéger réellement les cellules nerveuses. Si tel est le cas, ils pourraient servir de base à une nouvelle classe de traitements doux et multitâches, inspirés par la nutrition quotidienne.
Citation: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
Mots-clés: Maladie d’Alzheimer, Inhibition de GSK‑3β, peptides du lait, κ‑caséine, conception de médicaments assistée par ordinateur