Clear Sky Science · pl
Racjonalne projektowanie peptydów κ-kazeiny w celu modulacji dynamiki GSK-3β dla terapii choroby Alzheimera
Cząsteczki z mleka i pamięć
Choroba Alzheimera stopniowo pozbawia ludzi wspomnień i samodzielności, a dostępne dziś leki niewiele robią, by zatrzymać leżące u podstaw uszkodzenia mózgu. Niniejsze badanie sięga po nieoczekiwanie znajome źródło pomysłów terapeutycznych: mleko. Autorzy użyli zaawansowanych symulacji komputerowych, by przeprojektować niewielki fragment białka mlecznego tak, aby mógł przyczepiać się do kluczowego enzymu mózgowego związanego z Alzheimerem, potencjalnie łagodząc niektóre szkodliwe procesy napędzające chorobę.
Enzym, który wprowadza mózg w błąd
W chorobie Alzheimera komórki mózgowe są uszkadzane przez splecione włókna tau, lepkie blaszki amyloidowe i zawodzące połączenia między neuronami. Jeden enzym, nazywany GSK-3β, przyczynia się do kilku z tych problemów jednocześnie. Dodaje on chemiczne markery do białka tau, sprzyjając jego aglomeracji w splątki, wpływa też na formowanie amyloidu oraz na sprawność komunikacji komórek nerwowych i ich reakcję na sygnały podobne do insuliny. Z uwagi na tę centralną rolę wielu badaczy traktuje GSK-3β jako główny przełącznik postępu choroby i atrakcyjny cel nowych terapii.
Dlaczego patrzeć na białka mleka?
Mleko to nie tylko tłuszcz, cukier i wapń: zawiera też białka, które można rozciąć na krótkie fragmenty, czyli peptydy, wykazujące zaskakująco silne efekty biologiczne. Wcześniejsze badania sugerowały, że spożycie produktów mlecznych może chronić przed pogorszeniem funkcji poznawczych, a konkretne peptydy pochodzące z mleka potrafią chronić mózg, zmniejszać szkodliwą aktywność enzymów i poprawiać pamięć w modelach zwierzęcych. Jednym z głównych białek mleka jest kazeina, obejmująca różne podtypy; wśród nich κ-kazeina była stosunkowo mało zbadana jako źródło fragmentów chroniących mózg. Autorzy postawili pytanie, czy krótki odcinek κ-kazeiny można ukształtować w silny bloker GSK-3β.
Projektowanie „mądrzejszych” peptydów na komputerze
Zespół rozpoczął od przewidzenia trójwymiarowej struktury κ-kazeiny i dokowania jej do GSK-3β, by znaleźć fragment, który wsuwa się w kieszeń enzymu, gdzie zwykle wiążą się cząsteczki przenoszące energię. Znaleziono odcinek złożony z 10 aminokwasów, który już wykazywał przyzwoite uchwycenie. Przy użyciu szczegółowych obliczeń energetycznych zidentyfikowano cztery pozycje w tym segmencie, które przyczyniały się słabo lub wręcz niekorzystnie do wiązania. Następnie, przy użyciu narzędzia do przewidywania mutacji, systematycznie zamieniono te cztery elementy na alternatywy prawdopodobnie wzmacniające interakcję, tworząc wirtualną bibliotekę 48 nowych wariantów peptydów. Kontrole bezpieczeństwa wykluczyły kandydatów przewidywanych jako toksyczni lub alergenne, pozostawiając 22, które ponownie dokowano do GSK-3β.
Selekcja najbardziej obiecujących kandydatów
Wyniki dokowania i mapy interakcji wyodrębniły cztery wyróżniające się peptydy oznaczone jako PEP8, PEP36, PEP40 i PEP44. Wszystkie cztery miały dwie kluczowe zmiany polegające na zastąpieniu obojętnego, „oleistego” resztu w pobliżu jednego końca przez bardziej interaktywny, co pomagało im mocniej zakotwiczyć się w kieszeni enzymu. PEP8 i PEP44 posunęły się dalej, dodając ujemnie naładowany reszt na innej pozycji, co zwiększyło ich chwyt. Symulacje komputerowe prowadzone przez setki nanosekund pokazały, że gdy PEP8 lub PEP44 są związane, struktura enzymu staje się nieco bardziej kompaktowa i mniej elastyczna, szczególnie wokół kieszeni, gdzie zwykle znajdują się naturalne cele. Te peptydy nawiązywały więcej punktów kontaktu z enzymem niż oryginalny fragment mleczny, co sugeruje większą siłę i lepszą selektywność. Analizy energetyczne potwierdziły, że PEP8 i PEP44 tworzyły najściślejsze kompleksy, napędzane głównie przez oddziaływania bliskiego zasięgu i siły elektrostatyczne między peptydem a enzymem.
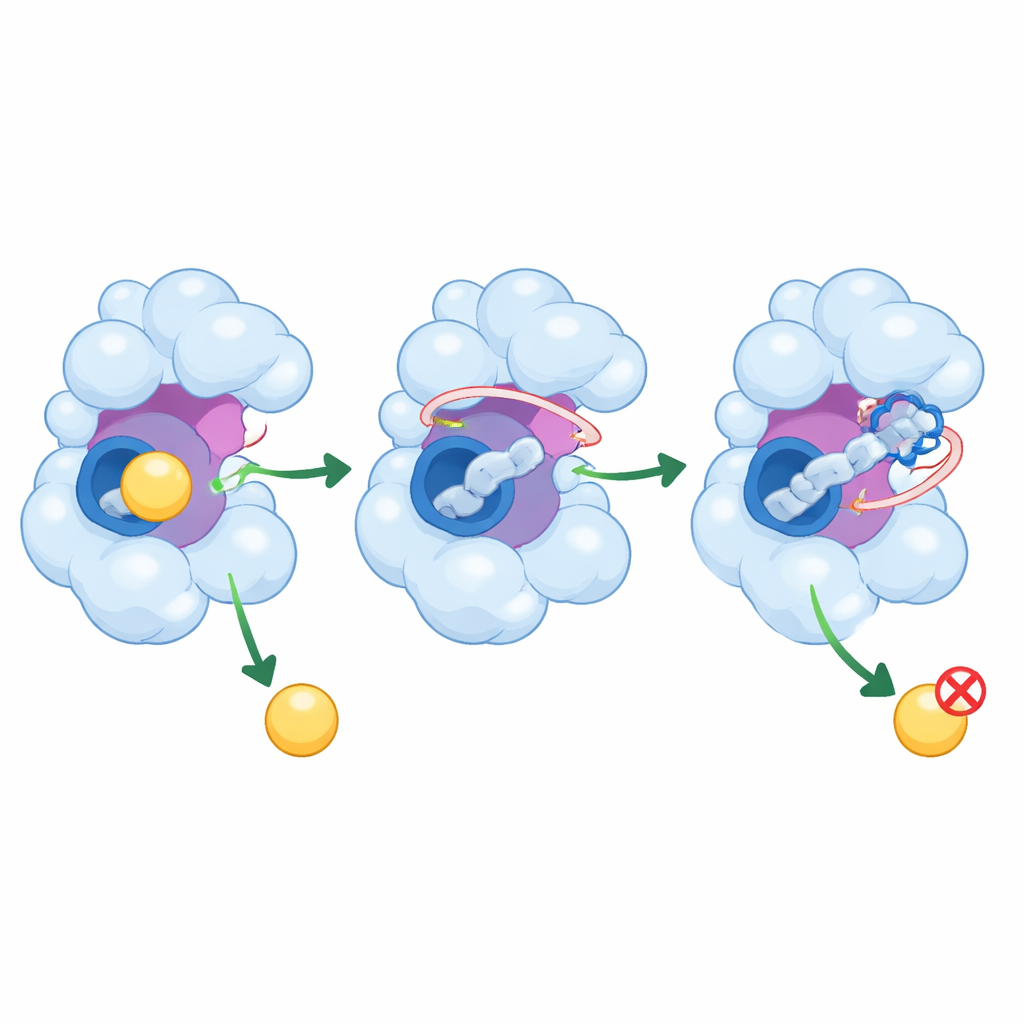
Jak te peptydy mogą uspokoić nadaktywny enzym
Ponad zwykłym zablokowaniem centralnej kieszeni, PEP8 i PEP44 wchodzą w sąsiednie rejony GSK-3β, które pomagają kontrolować jego aktywność. Oddziałują z elastyczną pętlą kierującą nadchodzące cząsteczki i, w przypadku PEP44, z resztą katalityczną kluczową dla chemii enzymu. Symulacje pokazują, że te interakcje ograniczają „pobudliwość” istotnych części białka, zawężając zakres kształtów, jakie enzym może przyjąć. Z poruszającymi się elementami częściowo zablokowanymi i bardziej zatłoczoną kieszenią, GSK-3β ma mniejszą zdolność do przyjmowania swoich zwykłych partnerów, co mogłoby przekładać się na zmniejszone powstawanie szkodliwych modyfikacji tau i zmian związanych z amyloidem w prawdziwych komórkach.
Co to może znaczyć dla przyszłych terapii
Choć praca ta została wykonana wyłącznie in silico — w komputerach, a nie w żywych mózgach — wytycza jasną ścieżkę od naturalnego białka spożywczego do starannie dopracowanych kandydatów peptydowych, które w zasadzie mogłyby przygasić ważny czynnik napędzający Alzheimera. PEP8 i PEP44 wyróżniają się jako najsilniejsze ligandy, przekształcając dynamikę enzymu w sposób, który powinien utrudniać jego szkodliwe działanie. Kolejne kroki wymagają badań laboratoryjnych, by potwierdzić, czy te zaprojektowane fragmenty mleka mogą dotrzeć do mózgu, pozostać stabilne w organizmie i rzeczywiście chronić komórki nerwowe. Jeśli tak, mogłyby stać się podstawą nowej klasy łagodnych, wielofunkcyjnych terapii inspirowanych codzienną dietą.
Cytowanie: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
Słowa kluczowe: choroba Alzheimera, inhibicja GSK-3β, peptydy mleczne, κ-kazeina, komputerowe projektowanie leków