Clear Sky Science · es
Diseño racional de péptidos de κ-caseína para modular la dinámica de GSK-3β en la terapia del Alzheimer
Moléculas de la leche y memoria
La enfermedad de Alzheimer va despojando lentamente a las personas de sus recuerdos e independencia, y los fármacos actuales hacen poco para detener el daño subyacente en el cerebro. Este estudio explora una fuente inesperadamente familiar para nuevas ideas terapéuticas: la leche. Los autores emplearon simulaciones computacionales avanzadas para rediseñar un pequeño fragmento de una proteína de la leche de modo que pueda unirse a una enzima cerebral clave vinculada al Alzheimer, potencialmente atenuando algunos de los procesos dañinos que impulsan la enfermedad.
La enzima que desorienta al cerebro
En el Alzheimer, las células cerebrales se dañan por fibras tau enredadas, placas amiloides pegajosas y conexiones neuronales que fallan. Una sola enzima, llamada GSK-3β, contribuye a varios de estos problemas a la vez. Añade marcas químicas a la proteína tau, fomentando que se agrupe en ovillos, y también influye en cómo se forma el amiloide, así como en la comunicación neuronal y la respuesta a señales tipo insulina. Debido a este papel central, muchos investigadores consideran a GSK-3β como un interruptor maestro de la progresión de la enfermedad y un objetivo principal para nuevas terapias.
¿Por qué estudiar proteínas de la leche?
La leche es más que grasa, azúcar y calcio: también contiene proteínas que pueden fragmentarse en péptidos cortos con efectos biológicos sorprendentemente potentes. Trabajos previos sugerían que el consumo de lácteos podría proteger frente al deterioro cognitivo, y que péptidos derivados de la leche pueden proteger el cerebro, reducir la actividad de enzimas perjudiciales y mejorar la memoria en modelos animales. Una de las principales proteínas de la leche, la caseína, incluye varios subtipos; entre ellos, la κ-caseína ha sido relativamente poco explorada como fuente de fragmentos neuroprotectores. Los autores se propusieron evaluar si un tramo corto de κ-caseína podía conformarse en un bloqueador potente de GSK-3β.
Diseñar péptidos más inteligentes en un ordenador
El equipo comenzó prediciendo la estructura tridimensional de la κ-caseína y acoplándola a GSK-3β para encontrar una porción que encaje en el bolsillo de la enzima donde normalmente se unen las moléculas portadoras de energía. Encontraron un segmento de 10 aminoácidos que ya mostraba bastante agarre. Usando cálculos energéticos detallados, identificaron cuatro posiciones dentro de ese segmento que contribuían débilmente o incluso de forma desfavorable a la unión. Luego, con una herramienta de predicción de mutaciones, intercambiaron sistemáticamente esos cuatro bloques por alternativas con probabilidad de reforzar la interacción, construyendo una biblioteca virtual de 48 variantes peptídicas nuevas. Controles de seguridad eliminaron candidatos predichos como tóxicos o alergénicos, quedando 22 que se volvieron a acoplar a GSK-3β.
Reduciendo el campo a los candidatos más prometedores
Las puntuaciones de acoplamiento y los mapas de interacción destacaron cuatro péptidos sobresalientes, etiquetados PEP8, PEP36, PEP40 y PEP44. Los cuatro compartían dos cambios clave que reemplazaron un residuo neutro y apolar cerca de un extremo por otro más interactivo, ayudándoles a anclarse con mayor firmeza en el bolsillo de la enzima. PEP8 y PEP44 fueron más allá, añadiendo un residuo con carga negativa en otra posición, lo que reforzó su agarre. Simulaciones computacionales realizadas durante cientos de nanosegundos mostraron que, cuando PEP8 o PEP44 están unidos, la estructura de la enzima se vuelve ligeramente más compacta y menos flexible, especialmente alrededor del bolsillo donde suelen situarse sus objetivos naturales. Estos péptidos establecieron más puntos de contacto con la enzima que el fragmento original de la leche, lo que sugiere mayor afinidad y mejor selectividad. Los análisis energéticos confirmaron que PEP8 y PEP44 formaron los complejos más estrechos, impulsados principalmente por atracciones a corta distancia y fuerzas eléctricas entre el péptido y la enzima.
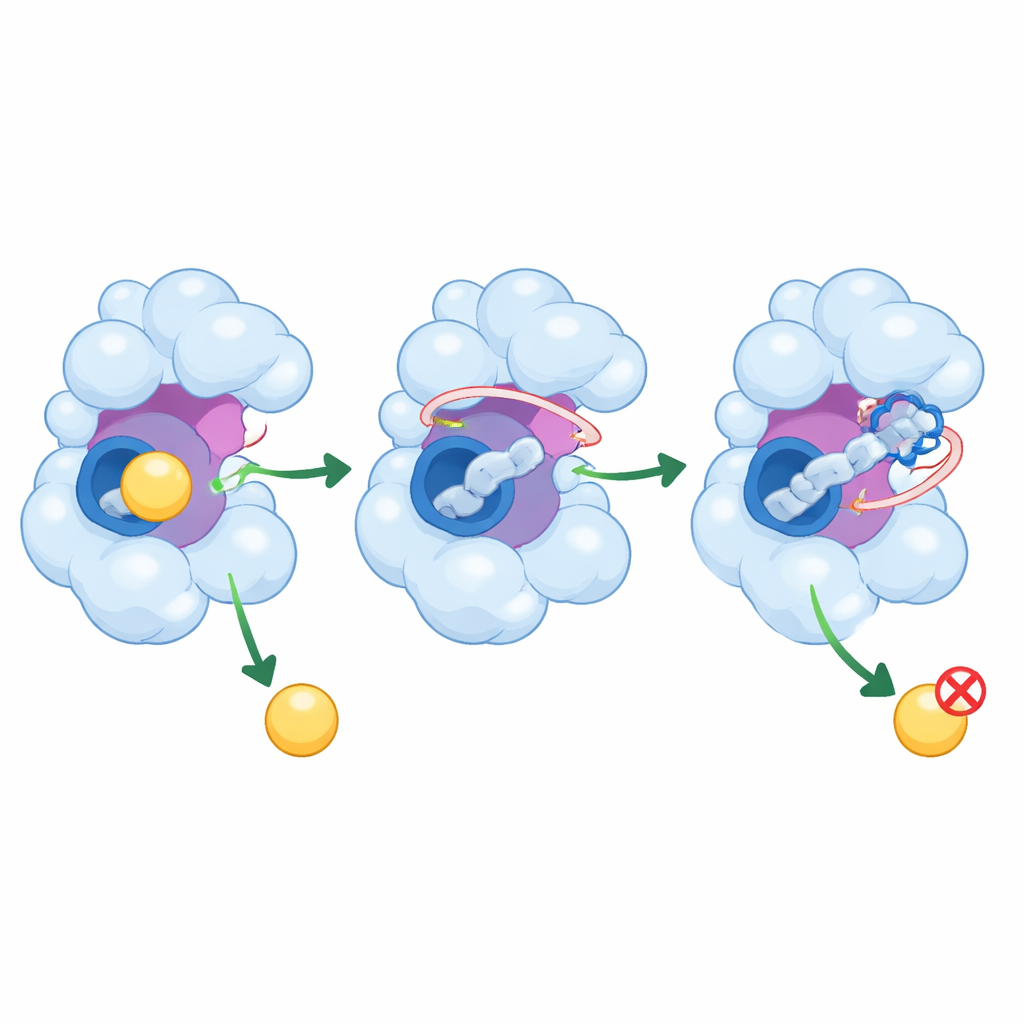
Cómo estos péptidos podrían calmar una enzima desbocada
Más allá de simplemente bloquear el bolsillo central, PEP8 y PEP44 alcanzan regiones vecinas de GSK-3β que ayudan a controlar su actividad. Interactúan con un lazo flexible que guía a las moléculas entrantes y, en el caso de PEP44, con un residuo catalítico crucial para la química de la enzima. Las simulaciones muestran que estas interacciones reducen el vaivén de partes importantes de la proteína, estrechando el rango de conformaciones que la enzima puede adoptar. Con sus piezas móviles parcialmente inmovilizadas y su bolsillo más congestionado, GSK-3β tiene menos capacidad para acoger a sus socios habituales, lo que podría traducirse en una disminución de la producción de modificaciones dañinas de tau y en cambios relacionados con el amiloide en células reales.
Qué podría significar esto para tratamientos futuros
Aunque este trabajo se realizó íntegramente in silico —dentro de ordenadores en lugar de en cerebros vivos— traza una ruta clara desde una proteína alimentaria natural hasta candidatos peptídicos afinados que, en principio, podrían moderar un impulsor importante del Alzheimer. PEP8 y PEP44 destacan como los ligandos más fuertes, remodelando la dinámica de la enzima de maneras que deberían obstaculizar sus acciones dañinas. Los siguientes pasos requerirán pruebas de laboratorio para confirmar si estos fragmentos lácteos diseñados pueden alcanzar el cerebro, permanecer estables en el organismo y realmente proteger a las neuronas. Si lo consiguen, podrían constituir la base de una nueva clase de tratamientos suaves y multitarea inspirados en la nutrición cotidiana.
Cita: Moghaddam, N., Ramazani, A. & Zarei, A. Rational design of k-casein peptides to modulate GSK-3B dynamics for Alzheimer’s therapy. Sci Rep 16, 12768 (2026). https://doi.org/10.1038/s41598-026-42103-z
Palabras clave: Enfermedad de Alzheimer, Inhibición de GSK-3β, péptidos de la leche, κ-caseína, diseño computacional de fármacos