Clear Sky Science · zh
涂有壳聚糖外壳的磁性分子印迹聚合物以增强可控药物释放
这对未来癌症治疗为何重要
抗癌药物可以挽救生命,但在到达靶点的过程中常常也会损伤健康细胞,导致严重副作用并限制患者可安全接受的药物剂量。本研究探索了一种微小的“智能”载体,用于白血病药物伊马替尼,该载体可被磁场引导并仅在酸性、类似肿瘤的环境中完全开启。目标简单而有力:更精确地将更多药物送达所需位置,延缓数天释放,并尽可能保护身体其他部位不受影响。
构建微小的定向药囊
研究者设计了一种多层纳米级胶囊——其尺寸比红细胞小数百倍——中心为磁性核。在该核周围添加了一层薄的二氧化硅壳以增强稳定性,然后用一种特殊的聚合物层围绕伊马替尼分子进行成型,类似为钥匙做专门的钥匙孔。这一步的“分子印迹”会留下微观空腔,能够强烈且选择性地捕获伊马替尼。最后,在装载药物后,他们用来自甲壳类天然物质的生物聚合物壳聚糖包裹整个结构,形成柔软的外衣。结果是得到一种可以被外部磁场牵引且对特定药物具有内在亲和力的磁性载药颗粒。
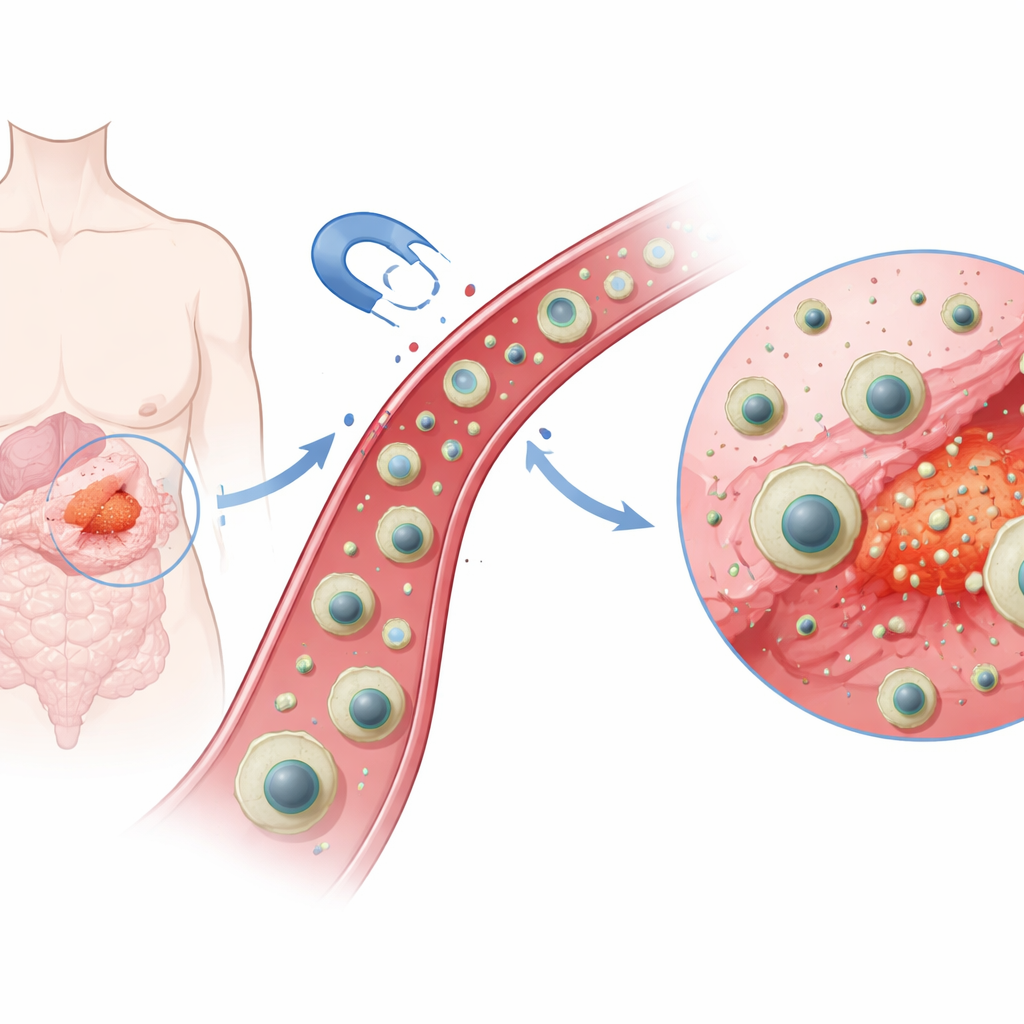
对体内化学环境的智能响应
肿瘤的一个显著特征是其周围环境通常比正常组织更酸性。团队利用了这一差异,选择壳聚糖作为外壳,因为其化学基团会随pH变化改变带电性。在健康组织附近的近中性条件(约pH 7.4)下,壳聚糖外壳保持相对致密、通透性较低,大部分药物被锁在内部。在更酸性的环境中(约pH 5.5,类似肿瘤小室和细胞回收中心),外壳的氨基会被质子化,带正电并相互排斥,从而使外壳膨胀变松,打开供药物分子逸出的通道。
对载体的性能测试
为检验设计效果,科学家们精确测量了颗粒的装药量及在不同条件下的释放速度。得益于印迹的内层,胶囊表现出高装载能力:大约三分之二的质量可为药物,并且它们对伊马替尼的结合远强于两种结构相关的类似抗癌药物。在模拟体液中,未包覆的颗粒释放货载较快,尤其在酸性溶液中。加入壳聚糖外壳后,释放显著变慢且呈强烈的pH依赖性。在四天内,中性pH下仅约四分之一的药物释放出来,而在酸性条件下大约有四分之三被释放,表明这些颗粒在正常组织中大多处于封闭状态,但在类似肿瘤的环境中则更容易打开。
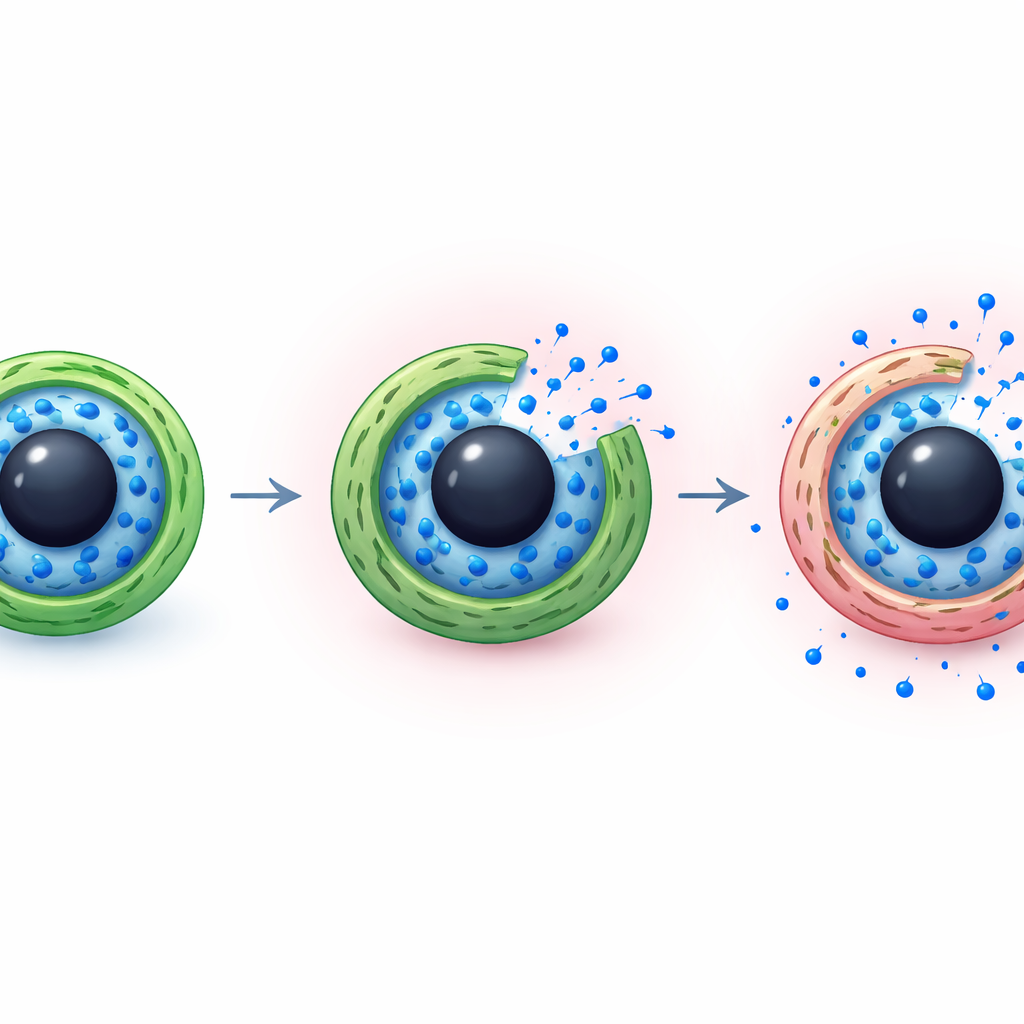
药物随时间渗出的机制
团队还分析了从物理层面上药物如何离开胶囊。通过将测得的释放曲线与药学中常用的数学模型比较,他们发现数据最好地符合这样一种图景:简单扩散与聚合物层的缓慢弛豫共同作用。在中性条件下,致密的壳聚糖涂层增加了阻力,使伊马替尼分子缓慢逸出;在酸性条件下,膨胀的外壳和印迹层内键合的减弱使水更易进入、药物更易移动,从而加速释放但并未演变成无法控制的突释。这一组合在循环过程中稳固地保留药物,同时在到达靶点后又允许其释放,提供了平衡。
更安全地攻击癌细胞
对人类白血病细胞和正常血液免疫细胞的体外实验展示了这种精细控制为何重要。游离伊马替尼对癌细胞和健康细胞都快速具有毒性。相比之下,载药颗粒对正常细胞温和得多,即便在更高剂量和更长暴露时间下仍如此,同时在药物逐步释放时仍能有效杀灭白血病细胞。尤其是壳聚糖包覆的版本,对癌细胞表现出更明显的时间依赖性效应,而绝大多数正常细胞存活,提示其在疗效与副作用之间的分离优于游离药物。
这对患者可能意味着什么
总体而言,这项工作展示了一个概念验证:一种可磁性引导的微小胶囊,能够识别特定抗癌药物、携带大量药物,并在肿瘤中比在健康组织中释放更多。尽管这些实验是在试管和细胞培养中完成,而非在患者身上,但它们指向未来治疗的可能性——医生或可用磁场将此类颗粒引向肿瘤,依靠肿瘤本身的酸性化学环境触发释放,从而减少常随化疗出现的附带损害。
引用: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
关键词: 靶向药物递送, 纳米颗粒, pH响应载体, 伊马替尼, 磁性聚合物