Clear Sky Science · pl
Magnetyczny molekularnie wyciskany polimer pokryty powłoką chitozanu dla usprawnionego kontrolowanego uwalniania leku
Dlaczego to ma znaczenie dla przyszłych terapii przeciwnowotworowych
Leki przeciwnowotworowe mogą ratować życie, ale często uszkadzają też zdrowe komórki, powodując poważne skutki uboczne i ograniczając dawki, jakie pacjenci mogą bezpiecznie otrzymać. W tym badaniu zbadano niezwykle mały, „inteligentny” nośnik dla leku przeciw białaczce — imatinibu — który można kierować za pomocą magnesów i który w pełni otwiera się tylko w kwaśnym, przypominającym guz środowisku. Cel jest prosty, lecz istotny: dostarczyć więcej leku precyzyjnie tam, gdzie jest potrzebny, uwalniać go stopniowo przez dni i jak najbardziej oszczędzić resztę organizmu.
Budowa maleńkiej, kierowanej kapsułki leku
Naukowcy zaprojektowali wielowarstwową kapsułkę o rozmiarach nano — setki razy mniejszą od czerwonej krwinki — z magnetycznym rdzeniem w centrum. Wokół tego rdzenia dodali cienką powłokę krzemionkową dla stabilności, a następnie specjalną warstwę polimeru odtworzoną wokół cząsteczek imatinibu niczym dopasowane gniazdo do klucza. Etap „molekularnego wyciskania” pozostawia mikroskopijne kieszonki, które silnie i selektywnie wiążą imatinib. Na koniec, po załadowaniu leku, całą strukturę otulono miękką zewnętrzną powłoką z chitozanu — biopolimeru spokrewnionego z naturalnymi materiałami występującymi u skorupiaków. Efekt to magnetyczna cząstka wypełniona lekiem, którą można przyciągnąć zewnętrznym magnesem i która ma wbudowaną preferencję względem konkretnego leku.
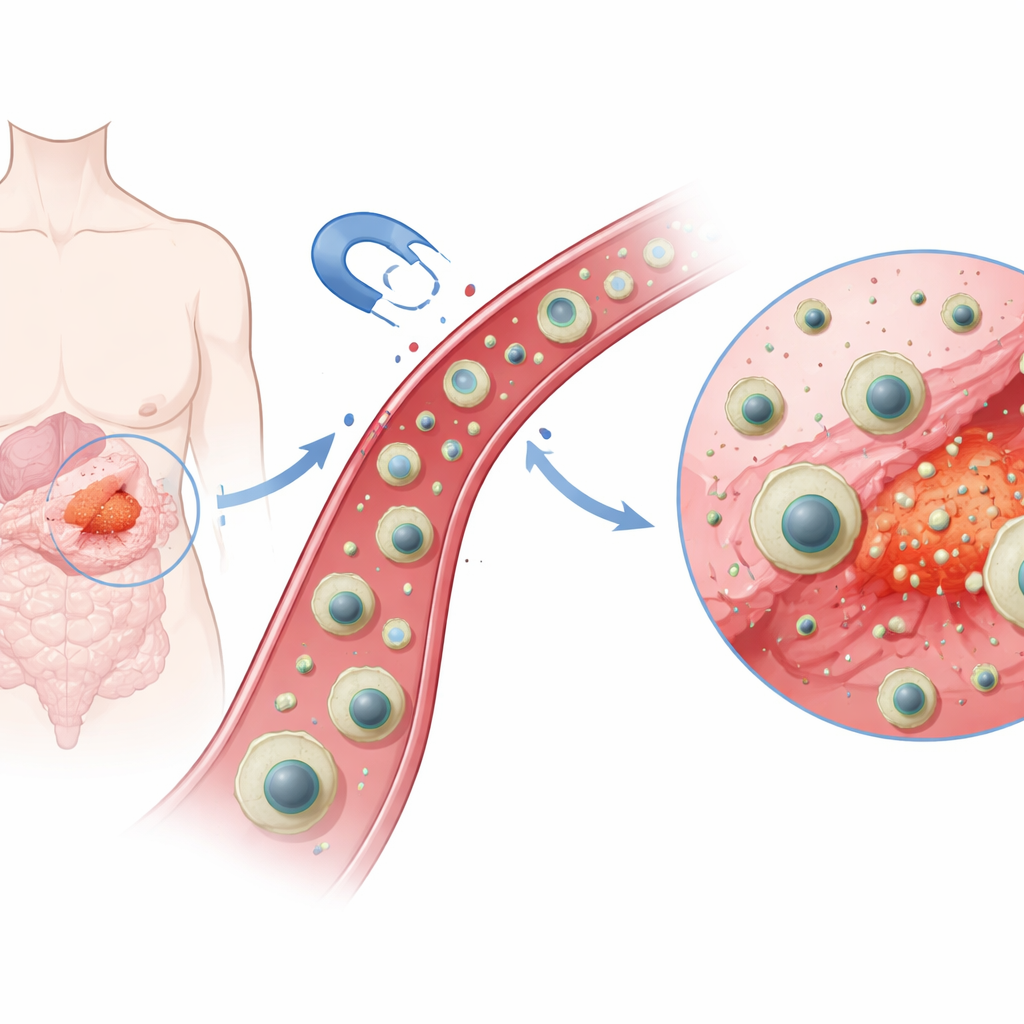
Inteligentna reakcja na chemię organizmu
Jedną z najbardziej charakterystycznych cech guzów jest to, że ich otoczenie jest zwykle bardziej kwaśne niż tkanki zdrowe. Zespół wykorzystał tę różnicę, wybierając chitozan na powłokę zewnętrzną, ponieważ jego grupy chemiczne zmieniają ładunek w zależności od pH. W warunkach bliskich obojętnym, charakterystycznych dla zdrowych tkanek (około pH 7,4), powłoka chitozanowa pozostaje stosunkowo zwarta i mniej przepuszczalna, utrzymując większość leku wewnątrz. W kwaśniejszym środowisku (około pH 5,5, podobnym do przedziałów w guzach i centrów recyklingu komórkowego) grupy aminowe powłoki przyjmują protony, stają się naładowane dodatnio i odpychają się nawzajem. Powoduje to pęcznienie i rozluźnienie powłoki, otwierając ścieżki, przez które cząsteczki leku mogą się wydostawać.
Testowanie nośnika
Aby sprawdzić skuteczność konstrukcji, naukowcy dokładnie zmierzyli, ile imatinibu cząstki są w stanie pomieścić i jak szybko ulega on wymywaniu w różnych warunkach. Dzięki wyciskanemu wewnętrznemu warstwie kapsułki wykazały wysoką pojemność ładunkową: około dwóch trzecich ich masy mogło stanowić lek, a imatinib wiązał się znacznie silniej niż dwa podobne leki przeciwnowotworowe o pokrewnych strukturach. Umieszczone w płynach imitujących warunki ustrojowe, niepowlekane cząstki uwalniały zawartość stosunkowo szybko, szczególnie w roztworach kwaśnych. Dodanie powłoki z chitozanu spowolniło ten proces i sprawiło, że uwalnianie stało się silnie zależne od pH. W ciągu czterech dni jedynie około jednej czwartej leku wydostało się przy neutralnym pH, podczas gdy w warunkach kwaśnych uwolnione zostało około trzech czwartych, co wskazuje, że cząstki pozostają w większości zamknięte w normalnych tkankach, lecz znacznie bardziej otwierają się w środowiskach przypominających guz.
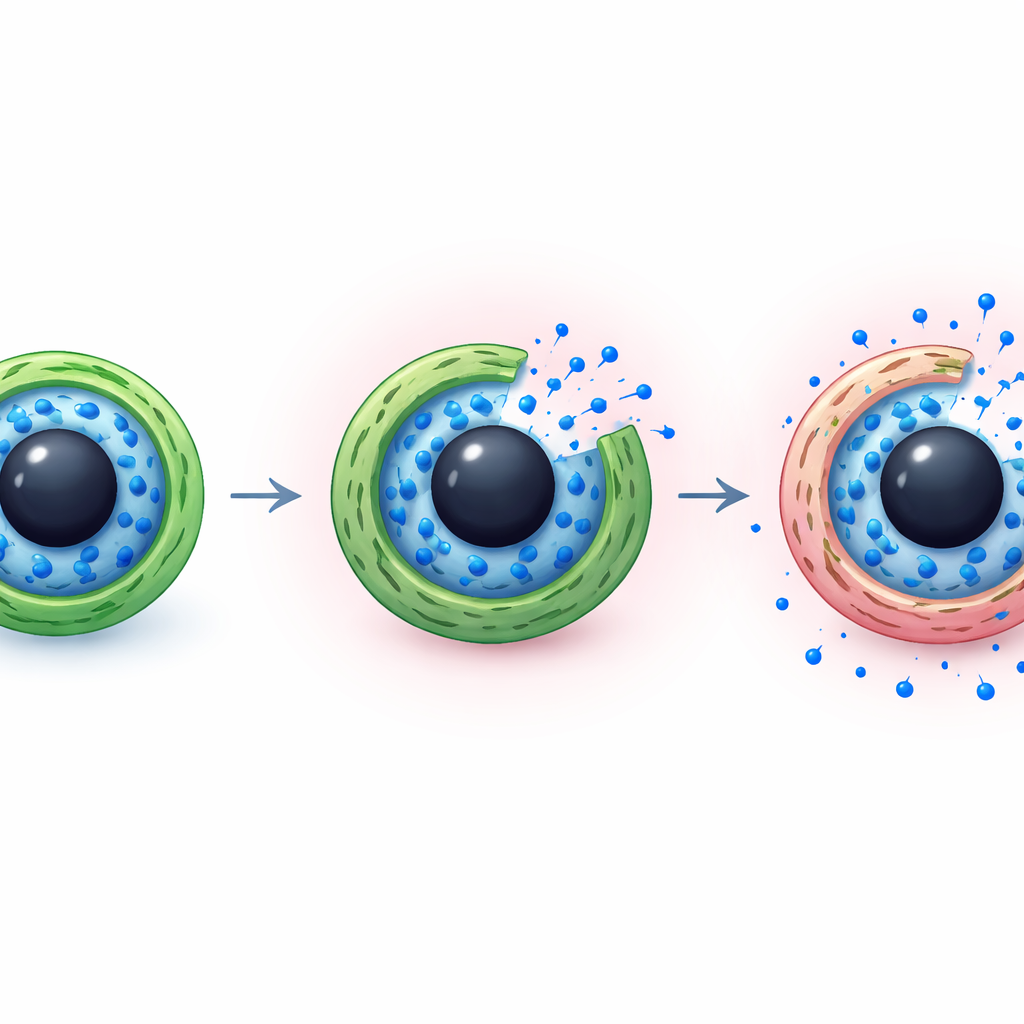
Jak lek przesącza się z upływem czasu
Zespół przeanalizował także, w kategoriach fizycznych, w jaki sposób lek opuszcza kapsułki. Porównując zmierzone krzywe uwalniania ze standardowymi modelami matematycznymi stosowanymi w naukach farmaceutycznych, stwierdzili, że dane najlepiej pasują do obrazu, w którym zarówno prosta dyfuzja, jak i powolna relaksacja warstw polimerowych działają wspólnie. W warunkach obojętnych ciasna powłoka z chitozanu dodaje opór, więc cząsteczki imatinibu wędrują na zewnątrz powoli. W warunkach kwaśnych spęczniała powłoka i osłabione wiązania wewnątrz wyciskanej warstwy ułatwiają napływ wody i ruch leku, przyspieszając uwalnianie bez przemiany w niekontrolowany wyrzut. To połączenie oferuje równowagę między bezpiecznym utrzymaniem leku podczas krążenia a umożliwieniem jego uwolnienia po dotarciu do celu.
Bardziej bezpieczne atakowanie komórek nowotworowych
Testy laboratoryjne na ludzkich komórkach białaczki i na normalnych komórkach odpornościowych krwi pokazały, dlaczego tak precyzyjna kontrola ma znaczenie. Wolny imatinib był szybko toksyczny zarówno dla komórek nowotworowych, jak i zdrowych. W przeciwieństwie do tego, cząstki załadowane lekiem były znacznie łagodniejsze dla komórek normalnych, nawet przy wyższych dawkach i dłuższym czasie ekspozycji, jednocześnie skutecznie zabijając komórki białaczki w miarę stopniowego uwalniania leku. W szczególności wersja pokryta chitozanem wykazała silniejsze efekty zależne od czasu wobec komórek nowotworowych przy jednoczesnym utrzymaniu większości komórek normalnych przy życiu, co sugeruje lepsze rozdzielenie korzyści i skutków ubocznych niż w przypadku wolnego leku.
Co to może oznaczać dla pacjentów
Podsumowując, praca dostarcza dowodu koncepcji dla maleńkiej, magnetycznie kierowalnej kapsułki, która rozpoznaje konkretny lek przeciwnowotworowy, przenosi jego dużą ilość i uwalnia go bardziej w guzach niż w zdrowych tkankach. Chociaż eksperymenty przeprowadzono w probówkach i hodowlach komórkowych, a nie u pacjentów, wskazują one drogę ku przyszłym terapiom, w których lekarze mogliby kierować takie cząstki w stronę guza za pomocą magnesów, polegać na kwaśnej chemii samego guza, by wywołać uwalnianie, i zmniejszyć szkody uboczne towarzyszące często chemioterapii.
Cytowanie: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
Słowa kluczowe: celowane dostarczanie leków, nanocząstki, nośniki reagujące na pH, imatinib, polimery magnetyczne