Clear Sky Science · ar
بوليمر بطبعة جزيئية مغناطيسي مغطى بغلاف شيتوزان لتحرير دواء محكوم معزز
لماذا يهم هذا لعلاجات السرطان المستقبلية
أدوية السرطان قد تنقذ الحياة، لكنها غالبًا ما تضر الخلايا السليمة على طول الطريق، محدثة آثارًا جانبية خطيرة ومقيدة لكمية الدواء التي يمكن أن يتلقاها المريض بأمان. تستكشف هذه الدراسة ناقلًا صغيرًا وذكيًا لدواء اللوكيميا إيماتينيب يمكن توجيهه بواسطة المغناطيس ويفتح بالكامل فقط في بيئات حمضية تشبه الورم. الهدف بسيط لكنه قوي: إرسال المزيد من الدواء بدقة إلى المكان المطلوب، إطلاقه ببطء على مدى أيام، وحماية بقية الجسم قدر الإمكان.
بناء كبسولة دوائية موجهة صغيرة
صمّم الباحثون كبسولة متعددة الطبقات بحجم نانوي — أصغر بمئات المرات من خلية دم حمراء — تحتوي على نواة مغناطيسية في المركز. حول هذه النواة أضافوا غلافًا رقيقًا من السيليكا للاستقرار، ثم طبقة بوليمرية خاصة مُشكَلة حول جزيئات الإيماتينيب مثل فتحة مخصصة لمفتاح. تترك خطوة «الطبع الجزيئي» وراءها تجاويف مجهرية تحبس الإيماتينيب بقوة وبانتقائية. أخيرًا، بعد تحميل الدواء، غلّفوا البنية كلها بطبقة خارجية ناعمة مصنوعة من الشيتوزان، وهو بوليمر حيوي ذو صلة بمواد طبيعية موجودة في القشريات. النتيجة جسيم مغناطيسي محمّل بالدواء يمكن سحبه بمغناطيس خارجي وله تفضيل مدمج لدواء محدد واحد.
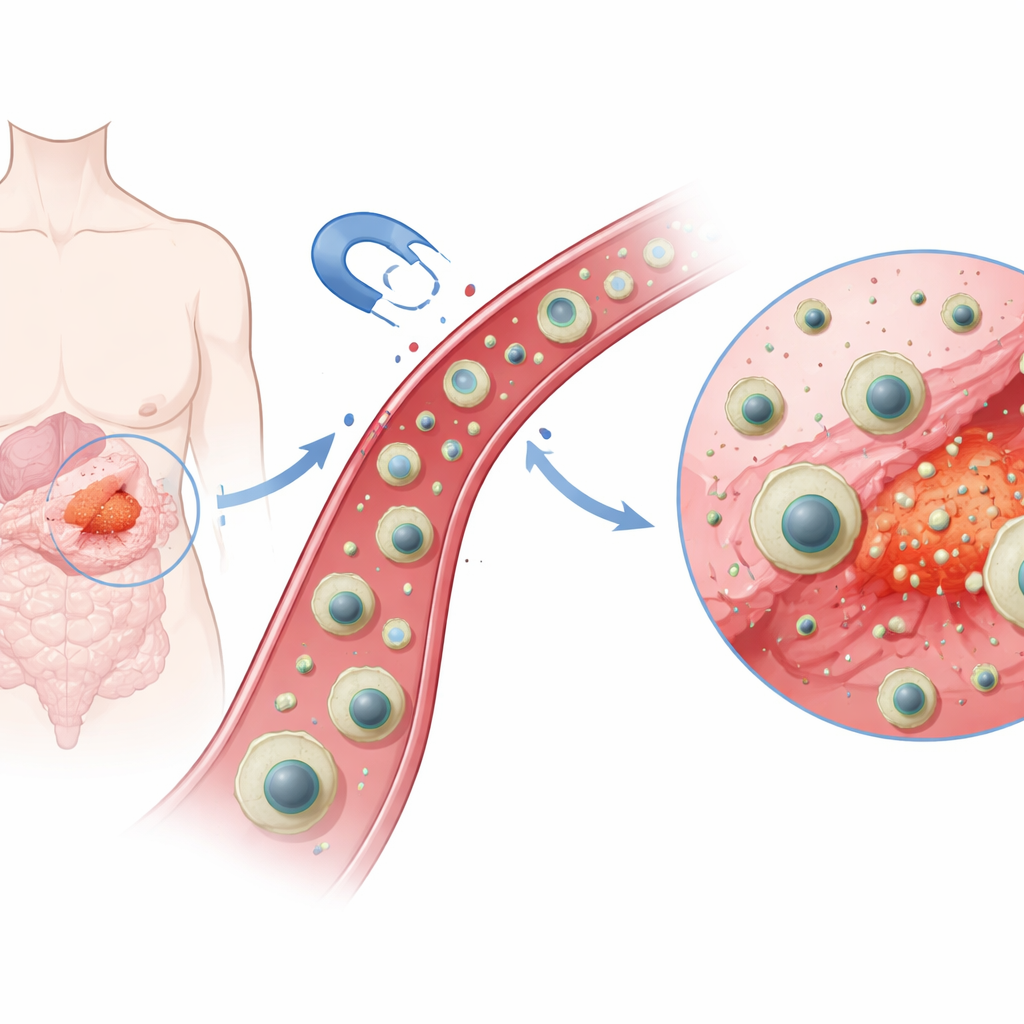
استجابة ذكية لكيمياء الجسم
إحدى أبرز خصائص الأورام أن محيطها يميل لأن يكون أكثر حمضية من الأنسجة الطبيعية. استغل الفريق هذا الفرق باختيار الشيتوزان كالقشر الخارجي، لأن مجموعاته الكيميائية تغير شحنتها حسب الحموضة. في ظروف قريبة من الحياد في الأنسجة السليمة (حوالي الرقم الهيدروجيني 7.4)، يبقى غلاف الشيتوزان مضغوطًا وأقل نفاذية، محتفظًا بمعظم الدواء بالداخل. في بيئة أكثر حمضية (حوالي الرقم الهيدروجيني 5.5، مشابهة لأقسام الأورام ومراكز إعادة تدوير الخلايا)، تكتسب مجموعات الأمين في الغلاف بروتونات، فتُصبح موجبة الشحنة وتتنافر مع بعضها البعض. يؤدي ذلك إلى انتفاخ الغلاف وتراخيه، ويفتح مسارات لتسرب جزيئات الدواء.
اختبار الناقل عمليًا
لمعرفة مدى فعالية التصميم، قاس العلماء بعناية مقدار الإيماتينيب الذي يمكن للجسيمات حمله ومدى سرعة تسربه تحت ظروف مختلفة. بفضل الطبقة الداخلية المطبوعة، أظهرت الكبسولات قدرة تحميل عالية: نحو ثلثي كتلتها كان يمكن أن يكون دواء، وكانت تربط الإيماتينيب بقوة أكبر بكثير من دوائين سرطانيين آخرين ذوي تراكيب قريبة. عند وضعها في سوائل تحاكي الجسم، أطلقت الجسيمات غير المغلَّفة حمولتها بسرعة نسبية، خاصة في محاليل حمضية. إضافة غلاف الشيتوزان أبطأ العملية وجعل الإطلاق معتمدًا بشكل قوي على الحموضة. على مدى أربعة أيام، تسرب حوالي ربع الدواء فقط عند الرقم الهيدروجيني المحايد، بينما تم إطلاق نحو ثلاثة أرباعه في ظروف حمضية، مما يشير إلى أن الجسيمات تبقى مغلقة إلى حد كبير في الأنسجة الطبيعية لكنها تفتح أكثر في بيئات تشبه الأورام.
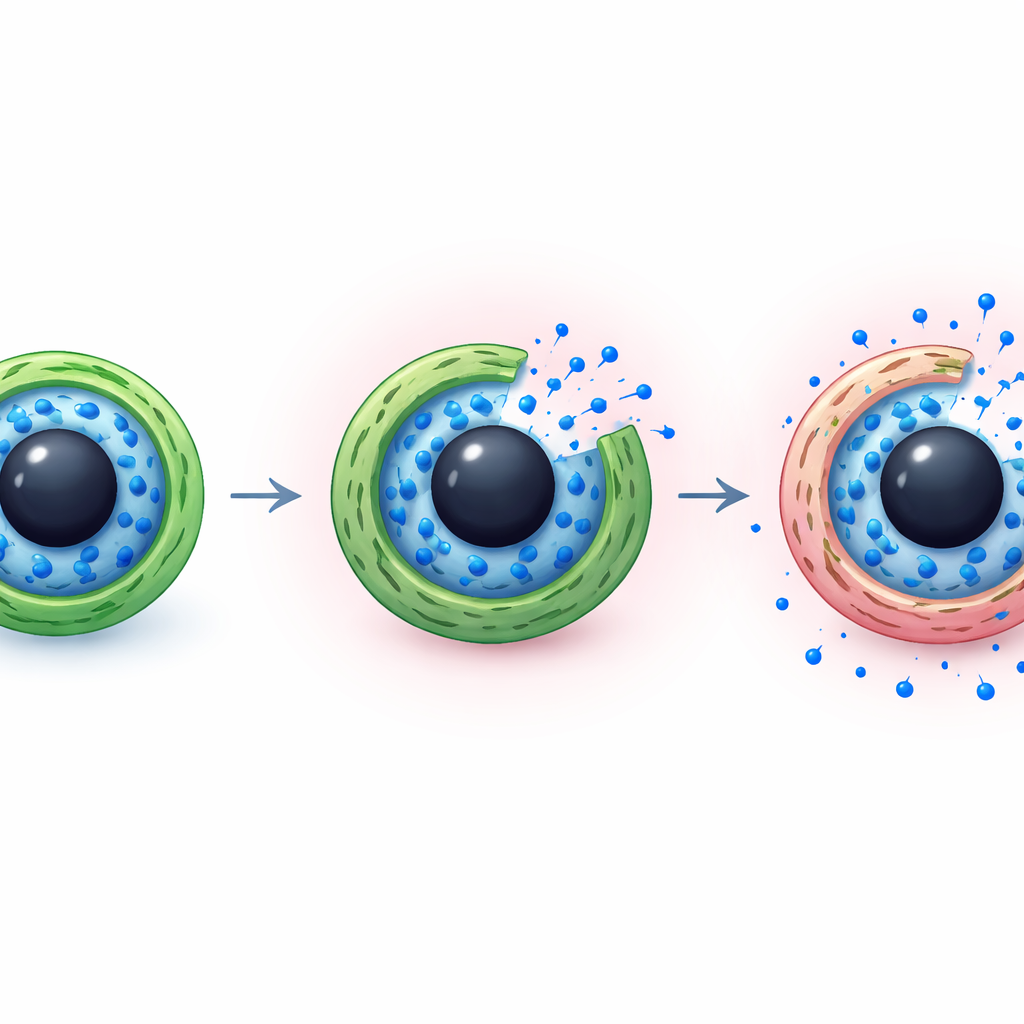
كيف يتسرب الدواء مع مرور الوقت
حلل الفريق أيضًا كيف يترك الدواء الكبسولات من الناحية الفيزيائية. بالمقارنة بين منحنيات الإطلاق المقاسة والنماذج الرياضية القياسية المستخدمة في علوم الصيدلة، وجدوا أن البيانات تتطابق أفضل مع صورة يعمل فيها كل من الانتشار البسيط والاسترخاء البطيء لطبقات البوليمر معًا. في الظروف المحايدة، يضيف غلاف الشيتوزان الضيق مقاومة، فتتحرك جزيئات الإيماتينيب ببطء نحو الخارج. في الظروف الحمضية، يجعل الغلاف المنتفخ والروابط الأضعف داخل الطبقة المطبوعة دخول الماء أسهل وحركة الدواء أسهل، مما يسرع الإطلاق دون أن يتحول إلى انفجار غير متحكم فيه. يقدم هذا المزيج توازنًا بين حفظ الدواء آمنًا أثناء الدوران في الجسم والسماح له بالخروج بمجرد وصوله إلى الهدف.
هجوم أكثر أمانًا على خلايا السرطان
أظهرت الاختبارات المخبرية على خلايا ليمفوما بشرية وخلايا مناعية دموية طبيعية سبب أهمية هذه السيطرة المتيقنة. كان الإيماتينيب الحر سامًا بسرعة لكل من الخلايا السرطانية والسليمة. بالمقابل، كانت الجسيمات المحمّلة بالدواء ألطف بكثير على الخلايا الطبيعية، حتى بجرعات أعلى وتعرض لفترات أطول، ومع ذلك قضت بفعالية على خلايا اللوكيميا مع إطلاق تدريجي للدواء. أظهرت النسخة المطلية بالشيتوزان على وجه الخصوص تأثيرات أقوى تعتمد على الزمن على الخلايا السرطانية بينما تُبقي معظم الخلايا الطبيعية على قيد الحياة، مما يشير إلى فصل أفضل بين الفائدة والآثار الجانبية مقارنة بالدواء الحر.
ماذا قد يعني هذا للمرضى
بشكل عام، يقدم العمل إثبات مفهوم لكبسولة صغيرة قابلة للتوجيه مغناطيسيًا تتعرف على دواء سرطاني محدد، وتحمل كمية كبيرة منه، وتفرجه أكثر في الأورام منه في الأنسجة السليمة. وعلى الرغم من أن هذه التجارب أُجريت في أنابيب اختبار وزراعات خلوية وليس في المرضى، فإنها تشير إلى علاجات مستقبلية قد يوجّه فيها الأطباء مثل هذه الجسيمات نحو الورم بالمغناطيس، ويعتمدون على كيمياء الحمضية في الورم لتحفيز الإفراج، مما يقلل من الضرر الجانبي الذي يصاحب العلاج الكيميائي في كثير من الأحيان.
الاستشهاد: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
الكلمات المفتاحية: توصيل الدواء المستهدف, جسيمات نانوية, حاملات حساسة لدرجة الحموضة, إيماتينيب, بوليمرات مغناطيسية