Clear Sky Science · he
פולימר מוטבע מולקולארית מגנטי מצופה בקליפת כיטוזן לשחרור מבוקר משופר של תרופה
מדוע זה משנה לטיפולים העתידיים בסרטן
תרופות לסרטן יכולות להציל חיים, אך לעיתים קרובות הן פוגעות גם בתאים בריאים, מה שמוביל לתופעות לוואי קשות ומגביל את כמות התרופה שניתן לתת בבטחה. המחקר הזה חוקר נשא זעיר וחכם לתרופת הלוקמיה אימטיניב, שניתן להניע בעזרת מגנטים וששפתוחו מוגבר רק בסביבות חומציות הדומות לגידול. המטרה פשוטה אך עוצמתית: להוביל יותר תרופה בדיוק היכן שהיא נדרשת, לשחררה בהדרגה על פני ימים, ולפגוע כמה שפחות בשאר הגוף.
בניית קפסולת רפואה מונחית זעירה
החוקרים תכננו קפסולה מולטישכבתית בגודל ננו — קטנה במאות פעמים מתא דם אדום — עם ליבה מגנטית במרכז. סביב ליבה זו הוסיפו מעטפת דקה של סיליקה ליציבות, ולאחריה שכבת פולימר מיוחדת שנוצרה תוך שימוש במולקולות אימטיניב כ"תבנית"—כמו חור מנעול שמותאם למפתח. שלב ה"הטבעה מולקולארית" הזה משאיר חללים מיקרוסקופיים שמלכדים אימטיניב בצורה חזקה וסלקטיבית. לבסוף, לאחר טעינת התרופה, עטפו את כל המבנה במעטה חיצוני רך עשוי כיטוזן, ביופולימר הקרוב לחומרים טבעיים הנמצאים בקליפת רכיכות. התוצאה היא חלקיק מגנטי מלא תרופה שניתן למשוך בעזרת מגנט חיצוני ובעל העדפה מובנית לתרופה מסוימת אחת.
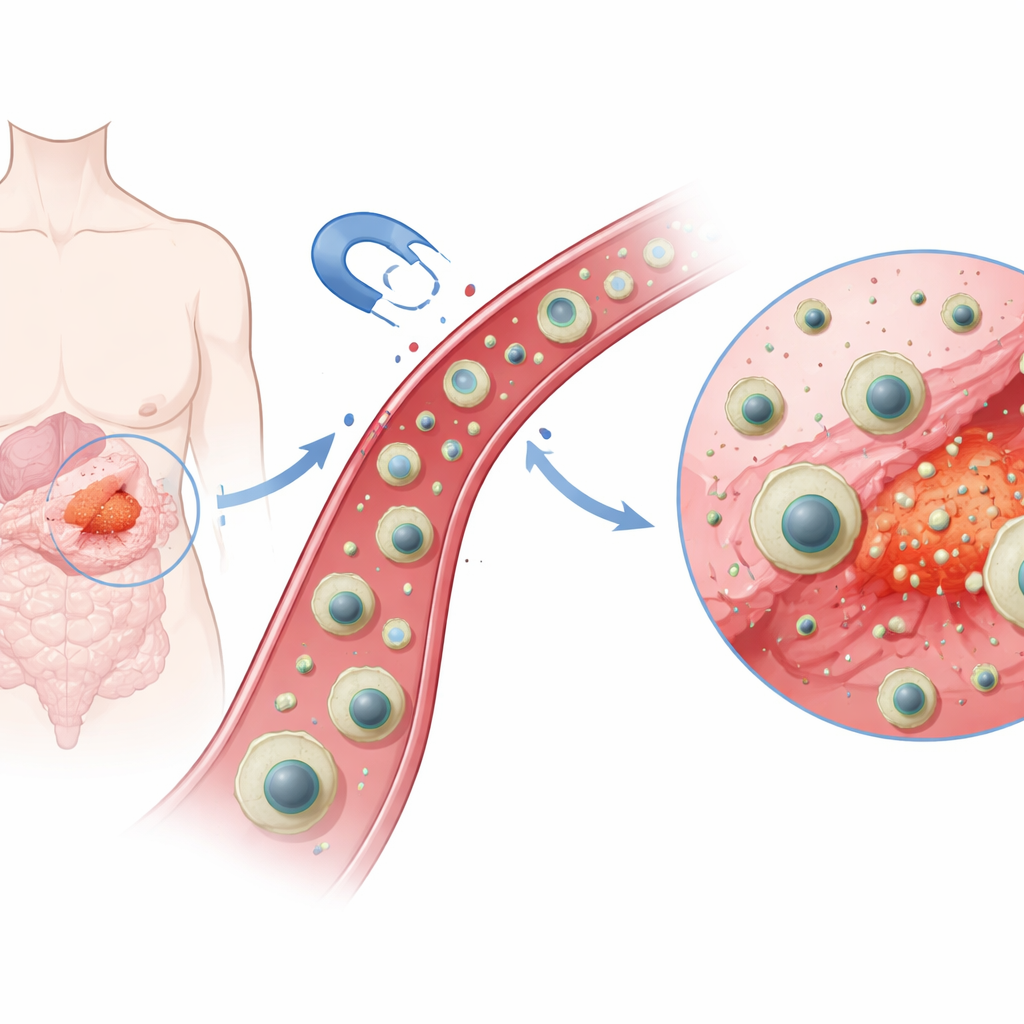
תגובה חכמה לכימיה של הגוף
אחת התכונות הבולטות של גידולים היא שסביבתן נוטה להיות חומצית יותר מרקמות נורמליות. הקבוצה ניצלה הבדל זה בבחירת הכיטוזן כקליפה החיצונית, משום שקבוצות הכימיות שלו משנות מטען בהתאם ל-pH. בתנאים נייטרליים-קרובים של רקמות בריאות (בערך pH 7.4), קליפת הכיטוזן נשארת דחוסה ופחות חדירה, ושומרת רוב התרופה בפנים. בסביבה חומצית יותר (בערך pH 5.5, דומה למחיצות גידול ומרכזי מיחזור תאיים), קבוצות האמינו של הכיטוזן קולטות פרוטונים, נהפכות חיוביות ומדחות זו את זו. זה גורם לכך שהקליפה מתנפחת ומתירלית, ויוצרת דרכי יציאה למולקולות התרופה.
בדיקת הנשא בפעולה
כדי לבחון עד כמה העיצוב עבד, המדענים מדדו בקפידה כמה אימטיניב החלקיקים יכולים להכיל וכמה מהר הוא דולף בחשיפות שונות. בזכות השכבה המוטבעת הפנימית, הקפסולות הראו קיבולת טעינה גבוהה: כשלושה-רבעים ממשקלן יכלו להיות תרופה, והן קשורות לאימטיניב בחוזקה רבה יותר מאשר לשתי תרופות סרטן דומות במבנה. כאשר הושמו בנוזלים המדמים את גופו של אדם, החלקיקים ללא הציפוי שחררו את המטען שלהם יחסית מהר, במיוחד בתמיסות חומציות. הוספת קליפת הכיטוזן האטה את כל התהליך ועשתה את השחרור תלוי pH באופן חזק. במהלך ארבעה ימים, רק כ־רבע מהתרופה יצאה ב-pH נייטרלי, בעוד שכ־שלושה-רבעים שוחררו בתנאים חומציים, מה שמעיד שהחלקיקים נשארים במצב סגור ברוב רקמות הגוף אך נפתחים יותר בסביבות הדומות לגידול.
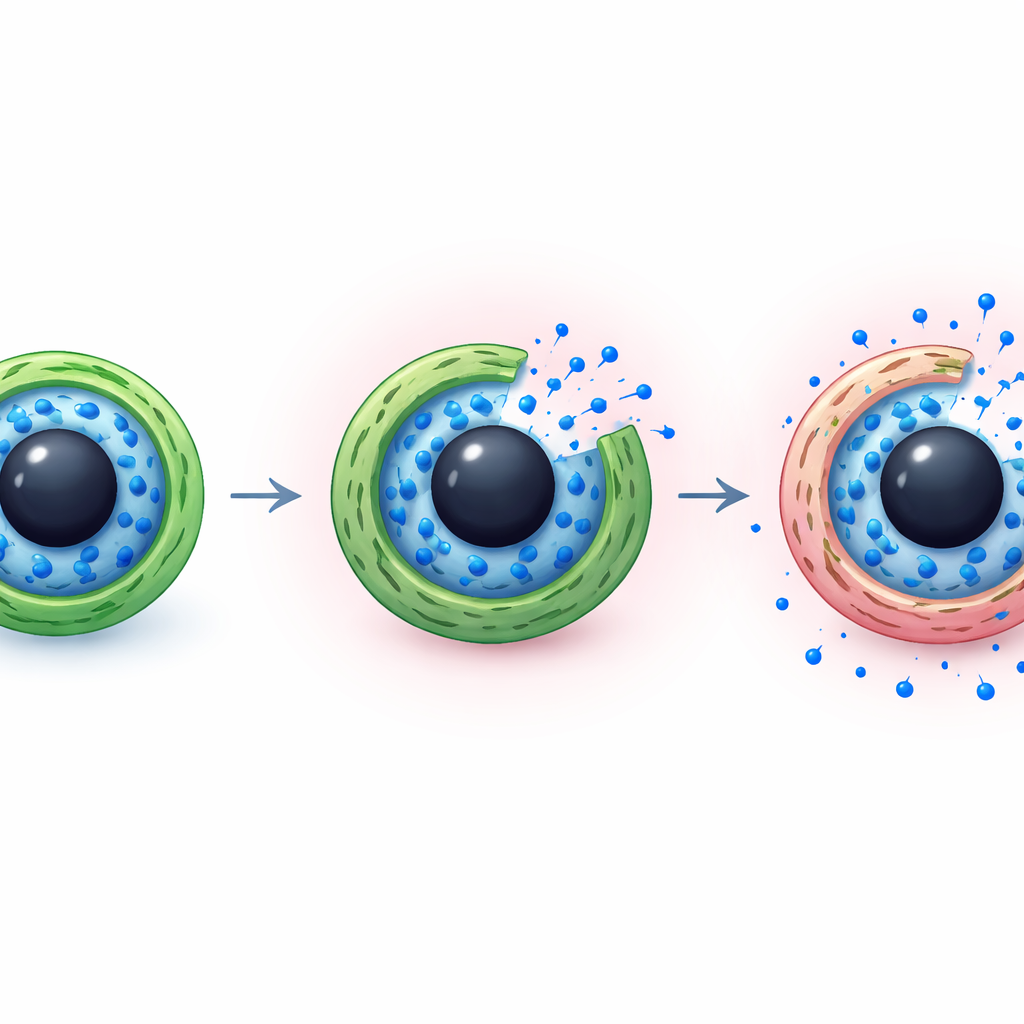
כיצד התרופה מחלחלת החוצה לאורך הזמן
הצוות גם ניתח כיצד, במונחים פיזיקליים, התרופה עוזבת את הקפסולות. בהשוואת עקומות השחרור הנמדדות למודלים מתמטיים סטנדרטיים בשימוש במדעי הפרמצבטיקה, נמצא שהנתונים מתאימים ביותר לתמונה שבה הן דיפוזיה פשוטה והן הרפיית פולימר איטית פועלות יחד. בתנאים נייטרליים הציפוי הצפוף של הכיטוזן מוסיף התנגדות, ולכן מולקולות האימטיניב נודדות החוצה באיטיות. בתנאים חומציים הקליפה המתנפחת וההחלשות של הקשירה בתוך השכבה המוטבעת מאפשרות למים לחדור ולתרופה לזוז בקלות רבה יותר, מה שמאיץ את השחרור מבלי להפוך אותו לפיצוץ בלתי נשלט. צירוף זה מציע איזון בין החזקת התרופה בבטחה במהלך ההסתובבות בדם לבין מתן אפשרות לשחרור ברגע שהחלקיקים הגיעו ליעד שלהם.
תקיפה בטוחה יותר של תאי סרטן
ניסויים במעבדה על תאי לוקמיה אנושיים ותאי דם חיסוניים רגילים הראו מדוע שליטה מדויקת כזו חשובה. אימטיניב חופשי היה רעיל במהירות הן לתאים סרטניים והן לתאים בריאים. לעומת זאת, החלקיקים המוטענים בתרופה היו הרבה יותר עדינים כלפי התאים הנורמליים, גם במינונים גבוהים ובחשיפות ארוכות יותר, ועדיין הרגו תאי לוקמיה ביעילות כשהתרופה שוחררה בהדרגה. הגרסה המצופה בכיטוזן במיוחד הראתה השפעות תלויות זמן חזקות יותר על תאים סרטניים בעוד שרוב התאים הנורמליים נותרו חיים, דבר המצביע על הפרדה טובה יותר בין תועלת ותופעות לוואי מאשר בתרופה החופשית.
מה יכול הדבר להציע לחולים
בסך הכל העבודה מהווה הוכחת קונספט לקפסולה זעירה שניתנת להנעה מגנטית, שמזהה תרופה סרטנית מסוימת, סוחבת כמות גדולה ממנה ומשחררת אותה יותר בגידולים מאשר ברקמות הבריאות. אמנם הניסויים הללו נעשו בצינורות ניסוי ובתרביות תאים ולא בחולים, הם מצביעים לכיוון טיפולים עתידיים שבהם רופאים עשויים להכוון חלקיקים כאלה אל הגידול בעזרת מגנטים, להסתמך על הכימיה החומצית של הגידול כזרז לשחרור, ולהפחית את הנזק הצדדי שאופייני לכימותרפיה.
ציטוט: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
מילות מפתח: העברת תרופות ממוקדת, ננוהחלקיקים, נשאים רגישי-pH, אימטיניב, פולימרים מגנטיים