Clear Sky Science · de
Magnetischer molekular-imprägnierter Polymerkern mit Chitosanhülle zur verbesserten kontrollierten Arzneistofffreisetzung
Warum das für künftige Krebstherapien wichtig ist
Krebsmedikamente können Leben retten, schädigen aber oft auch gesunde Zellen und verursachen dadurch schwere Nebenwirkungen, die die maximal verabreichbare Dosis begrenzen. Diese Studie untersucht einen winzigen, intelligenten Träger für das Leukämie‑Medikament Imatinib, der sich mit Magneten steuern lässt und sich nur in sauren, tumorähnlichen Umgebungen vollständig öffnet. Das Ziel ist einfach, aber wirkungsvoll: mehr Wirkstoff gezielt dorthin bringen, wo er gebraucht wird, ihn über Tage langsam freisetzen und den Rest des Körpers möglichst schonen.
Bau einer winzigen, gesteuerten Medikamentenkapsel
Die Forschenden entwarfen eine mehrschichtige, nanoskalige Kapsel—hunderte Male kleiner als eine rote Blutzelle—mit einem magnetischen Kern im Zentrum. Um diesen Kern legten sie eine dünne Silikatschicht zur Stabilisierung und anschließend eine spezielle Polymerschicht, die um Imatinib‑Moleküle herum geformt wurde wie ein maßgeschneidertes Schlüsselloch um einen Schlüssel. Dieser Schritt der „molekularen Imprägnierung“ hinterlässt mikroskopische Hohlräume, die Imatinib stark und selektiv binden. Nach dem Beladen mit dem Wirkstoff umhüllten sie die Struktur schließlich mit einer weichen Außenhülle aus Chitosan, einem Biopolymer, das mit natürlichen Stoffen aus Schalentieren verwandt ist. Das Ergebnis ist ein magnetisches, medikamentenbefülltes Partikel, das sich von einem externen Magneten anziehen lässt und von Haus aus eine Vorliebe für genau diesen Wirkstoff zeigt.
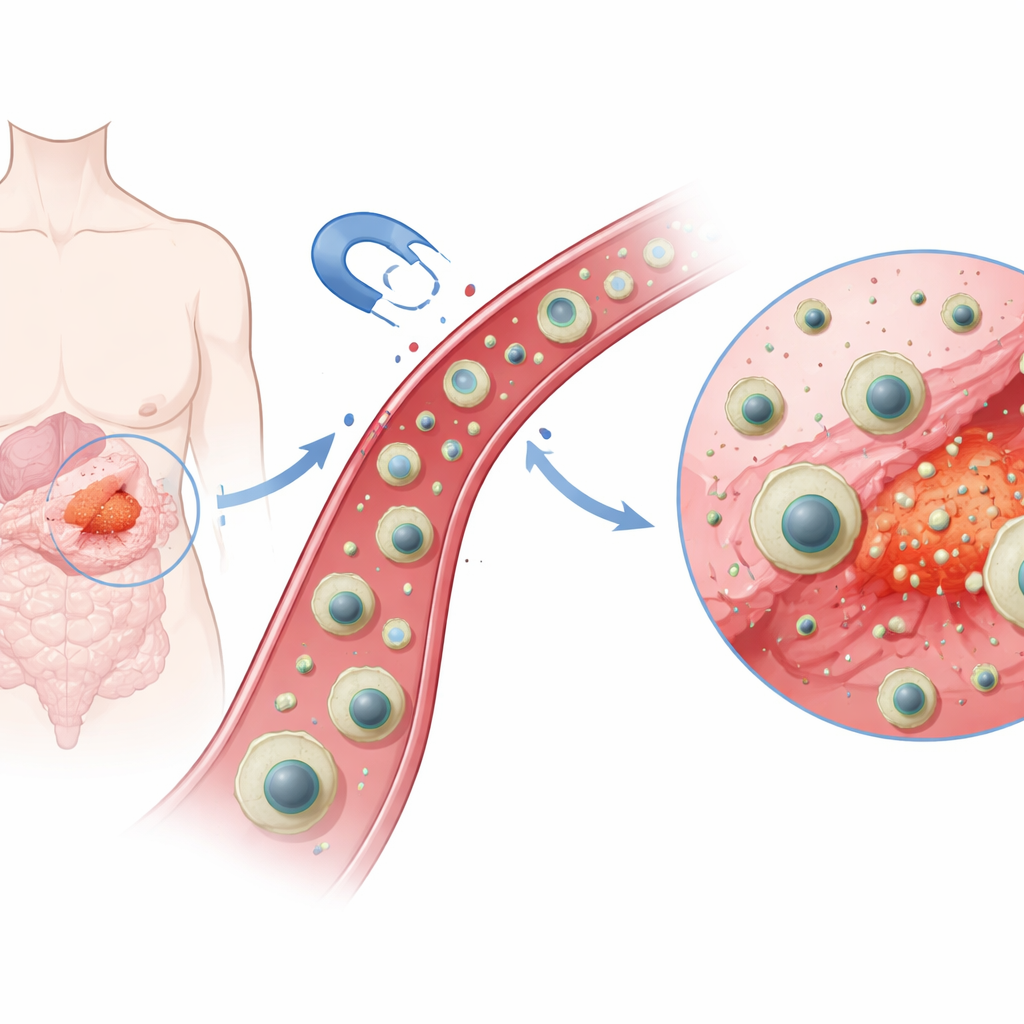
Intelligente Reaktion auf die Körperchemie
Eines der markantesten Merkmale von Tumoren ist, dass ihre Umgebung im Vergleich zu normalem Gewebe tendenziell saurer ist. Das Team nutzte diesen Unterschied, indem es Chitosan als Außenhülle wählte, weil dessen chemische Gruppen ihre Ladung in Abhängigkeit vom pH‑Wert ändern. Unter den nahezu neutralen Bedingungen gesunden Gewebes (um pH 7,4) bleibt die Chitosanhülle relativ kompakt und weniger durchlässig, sodass der Großteil des Wirkstoffs eingeschlossen bleibt. In einer sauren Umgebung (etwa pH 5,5, ähnlich wie in Tumorkompartimenten und zellulären Recyclingzentren) nehmen die Aminogruppen der Hülle Protonen auf, werden positiv geladen und stoßen sich gegenseitig ab. Dadurch quillt die Hülle auf und lockert sich, sodass Wege für die Wirkstoffmoleküle frei werden.
Prüfung des Trägers
Um die Leistungsfähigkeit ihres Designs zu testen, bestimmten die Wissenschaftler präzise, wie viel Imatinib die Partikel aufnehmen konnten und wie schnell es unter verschiedenen Bedingungen freigesetzt wurde. Dank der imprägnierten inneren Schicht zeigten die Kapseln eine hohe Beladungskapazität: etwa zwei Drittel ihrer Masse konnten Wirkstoff sein, und sie banden Imatinib deutlich stärker als zwei ähnliche Krebsmedikamente mit verwandten Strukturen. In körperähnlichen Flüssigkeiten setzten die unbeschichteten Partikel ihren Inhalt relativ schnell frei, besonders in sauren Lösungen. Die Zugabe der Chitosanhülle verlangsamte die Freisetzung und machte sie stark pH‑abhängig. Über vier Tage entwich bei neutralem pH nur etwa ein Viertel des Wirkstoffs, während unter sauren Bedingungen ungefährt drei Viertel freigesetzt wurden — ein Hinweis darauf, dass die Partikel in normalem Gewebe größtenteils geschlossen bleiben, sich in tumorähnlicher Umgebung jedoch deutlich mehr öffnen.
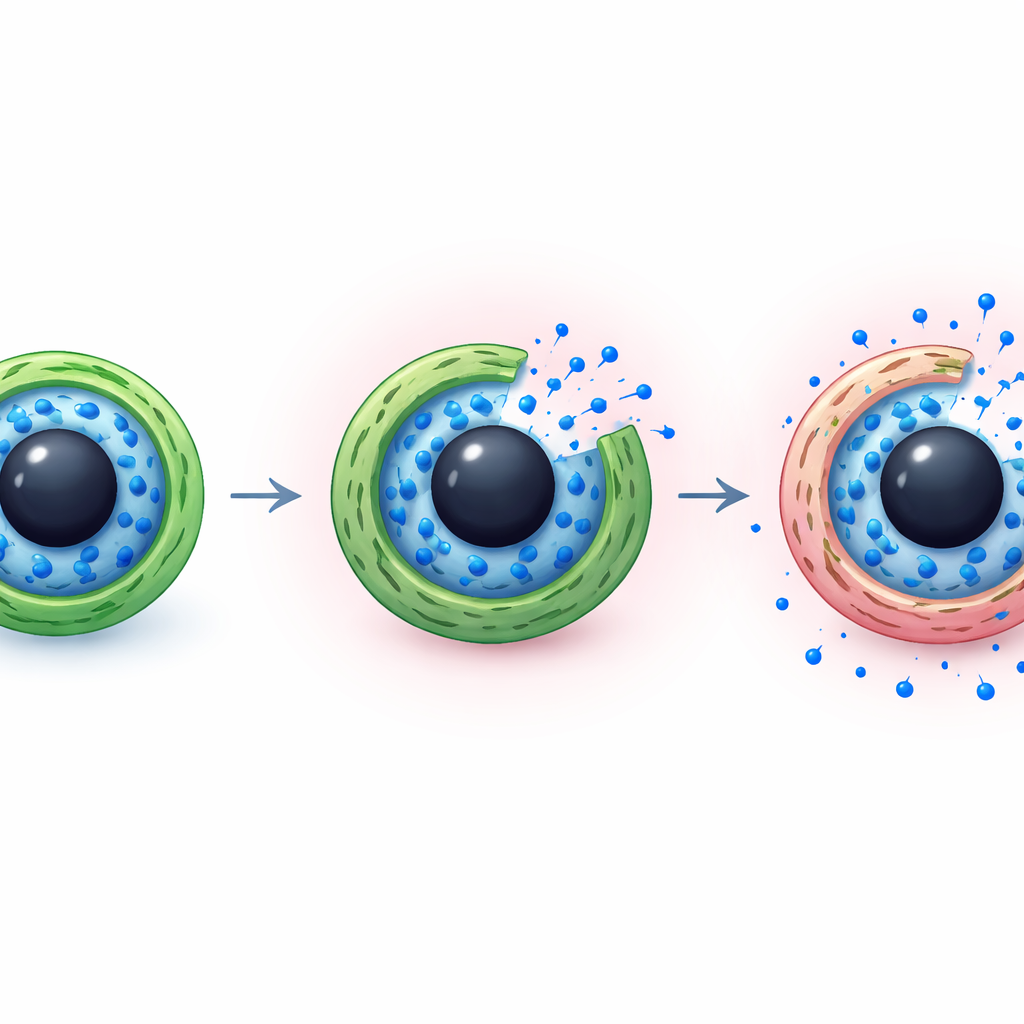
Wie der Wirkstoff im Zeitverlauf entweicht
Die Forschenden analysierten außerdem physikalisch, wie der Wirkstoff die Kapseln verlässt. Durch den Vergleich der gemessenen Freisetzungskurven mit gängigen mathematischen Modellen der pharmazeutischen Wissenschaft fanden sie, dass die Daten am besten zu einem Szenario passen, in dem sowohl einfache Diffusion als auch langsame Relaxation der Polymerschichten zusammenwirken. Bei neutralen Bedingungen fügt die dichte Chitosanbeschichtung Widerstand hinzu, sodass Imatinib‑Moleküle nur langsam entweichen. In saurer Umgebung erleichtern die gequollene Hülle und die geschwächten Bindungen in der imprägnierten Schicht das Eindringen von Wasser und die Bewegung des Wirkstoffs, was die Freisetzung beschleunigt, ohne sie in einen unkontrollierten Schub zu verwandeln. Diese Kombination bietet ein Gleichgewicht zwischen sicherer Bindung des Medikaments während der Zirkulation und seiner Freigabe, sobald es am Ziel angekommen ist.
Sichererer Angriff auf Krebszellen
Laborversuche an menschlichen Leukämiezellen und normalen Blut‑Immunzellen zeigten, warum eine so feine Steuerung wichtig ist. Freies Imatinib war rasch toxisch für sowohl Krebs‑ als auch gesunde Zellen. Im Gegensatz dazu wirkten die mit Wirkstoff beladenen Partikel auf normale Zellen deutlich schonender, selbst bei höheren Dosen und längerer Exposition, töteten dabei jedoch Leukämiezellen effizient, während der Wirkstoff schrittweise freigesetzt wurde. Die chitosanbeschichtete Variante zeigte dabei besonders ausgeprägte zeitabhängige Effekte auf Krebszellen bei gleichzeitigem Erhalt der meisten normalen Zellen, was auf eine bessere Trennung von Nutzen und Nebenwirkungen im Vergleich zum freien Wirkstoff hindeutet.
Was das für Patienten bedeuten könnte
Insgesamt liefert die Arbeit einen Proof of Concept für eine winzige, magnetisch steuerbare Kapsel, die einen spezifischen Krebswirkstoff erkennt, große Mengen davon transportiert und in Tumoren stärker freisetzt als in gesundem Gewebe. Obwohl diese Experimente in Reagenzgläsern und Zellkulturen und nicht am Patienten durchgeführt wurden, weisen sie in Richtung künftiger Therapien, bei denen Ärztinnen und Ärzte solche Partikel mit Magneten in Richtung Tumor lenken, auf die saure Chemie des Tumors zur Auslösung der Freisetzung vertrauen und so die Kollateralschäden verringern könnten, die Chemotherapien häufig begleiten.
Zitation: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
Schlüsselwörter: zielgerichtete Wirkstofffreisetzung, Nanopartikel, pH‑reaktive Trägersysteme, Imatinib, magnetische Polymere