Clear Sky Science · tr
İyileştirilmiş kontrollü ilaç salımı için kitin kabuklu manyetik moleküler baskılı polimer
Geleceğin kanser tedavileri için neden önemli
Kanser ilaçları hayat kurtarabilir, ancak çoğunlukla sağlıklı hücrelere de zarar vererek ciddi yan etkilere ve hastaların güvenli alabilecekleri ilaç miktarının sınırlanmasına yol açar. Bu çalışma, manyetik alanlarla yönlendirilebilen ve yalnızca tümör benzeri asidik ortamlarda tamamen açılan lösemi ilacı imatinib için küçük, akıllı bir taşıyıcıyı araştırıyor. Amaç basit ama güçlü: ilacı tam ihtiyaç duyulan yere tam isabetle göndermek, günler boyunca yavaşça salmak ve vücudun geri kalanını olabildiğince korumak.
Mini kılavuzlu ilaç kapsülü inşa etmek
Araştırıcılar, merkezinde manyetik bir çekirdeğe sahip çok katmanlı nano boyutlu bir kapsül tasarladı—kırmızı kan hücresinden yüzlerce kez daha küçük. Bu çekirdeğin etrafına kararlılık için ince bir silika kabuk eklediler, ardından imatinib molekülleri etrafında kalıp gibi şekillenen özel bir polimer tabakası uyguladılar. Bu “moleküler baskılama” adımı, imatinibi güçlü ve seçici olarak bağlayan mikroskobik boşluklar bırakır. Son olarak, ilacı yükledikten sonra tüm yapıyı kabuklu deniz ürünlerinde bulunan doğal maddelere ilişkili bir biyopolimer olan kitin bazlı yumuşak bir dış katmanla sardılar. Ortaya çıkan, harici bir mıknatısla çekilebilen ve belirli bir ilaca karşı doğal bir tercihi olan manyetik, ilaç dolu bir parçacıktır.
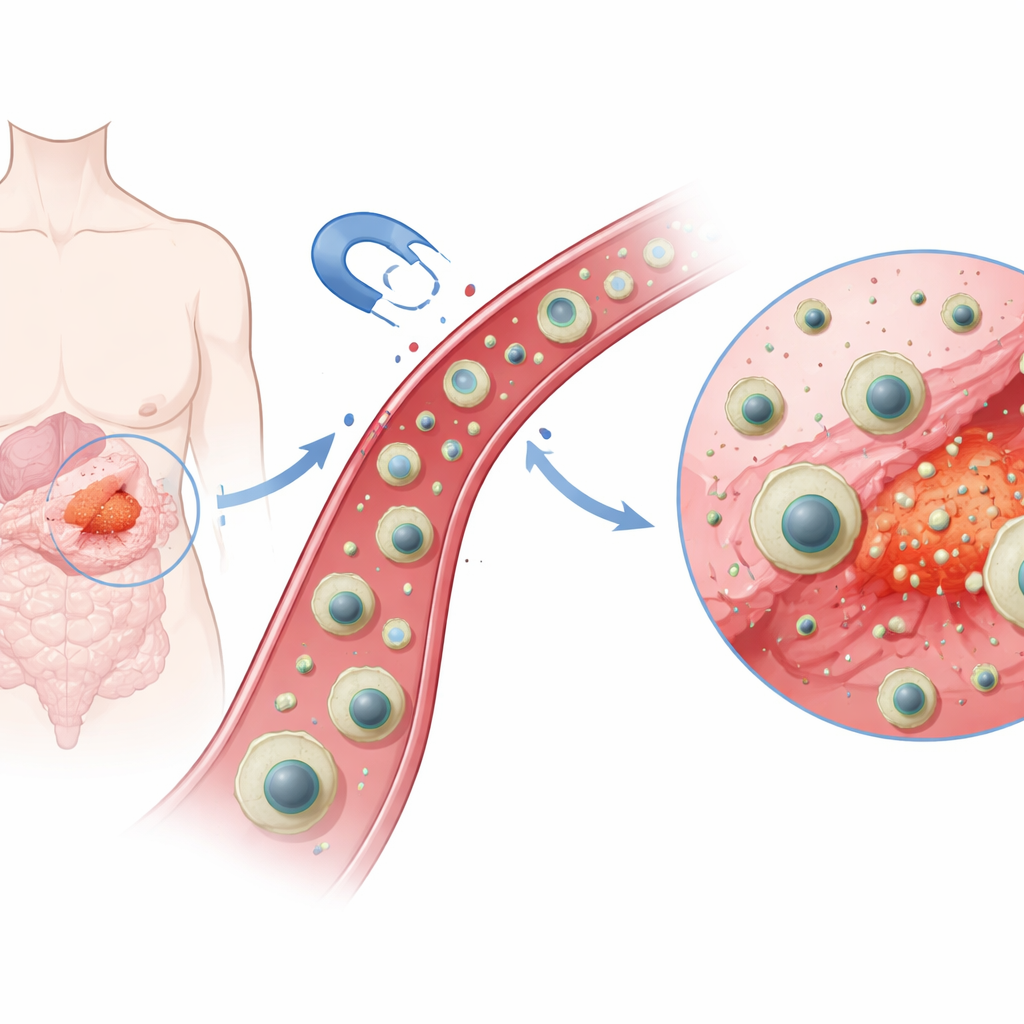
Vücudun kimyasına akıllı tepki
Tümörlerin en çarpıcı özelliklerinden biri, çevrelerinin normal dokulardan daha asidik olma eğilimidir. Ekip, dış kabuk olarak kitini seçerek bu farkı kullandı; çünkü kitinin kimyasal grupları pH'ya bağlı olarak yük değiştirir. Sağlıklı dokuların yakın-nötr koşullarında (yaklaşık pH 7.4) kitin kabuk nispeten sıkı ve daha az geçirgendir, böylece ilacın çoğunu içeride tutar. Daha asidik bir ortamda (yaklaşık pH 5.5, tümör bölmeleri ve hücre geri dönüşüm merkezlerine benzer), kabuğun amino grupları proton alır, pozitif yüklenir ve birbirini iter. Bu, kabuğun şişmesine ve gevşemesine neden olarak ilaç moleküllerinin kaçması için yollar açar.
Taşıyıcıyı teste sokmak
Tasarımın ne kadar iyi çalıştığını görmek için bilim insanları parçacıkların ne kadar imatinib tutabildiğini ve farklı koşullar altında ne kadar hızlı sızdırdıklarını dikkatle ölçtü. Baskılanmış iç katman sayesinde kapsüller yüksek bir yükleme kapasitesi gösterdi: kütlelerinin yaklaşık üçte ikisi ilaç olabiliyordu ve imatinibi ilgili yapıdaki iki benzer kanser ilacından çok daha güçlü bağladılar. Vücutı taklit eden sıvılara konulduğunda kaplanmamış parçacıklar yüklerini göreceli olarak hızlı serbest bıraktı, özellikle asidik çözeltilerde. Kitin kabuğun eklenmesi her şeyi yavaşlattı ve salımı güçlü biçimde pH bağımlı hale getirdi. Dört gün boyunca nötr pH'da ilacın sadece yaklaşık dörtte biri kaçarken, asidik koşullarda yaklaşık dörtte üçünün salınması, parçacıkların normal dokularda çoğunlukla kapalı kaldığını ancak tümör benzeri ortamlarda çok daha fazla açıldıklarını gösterdi.
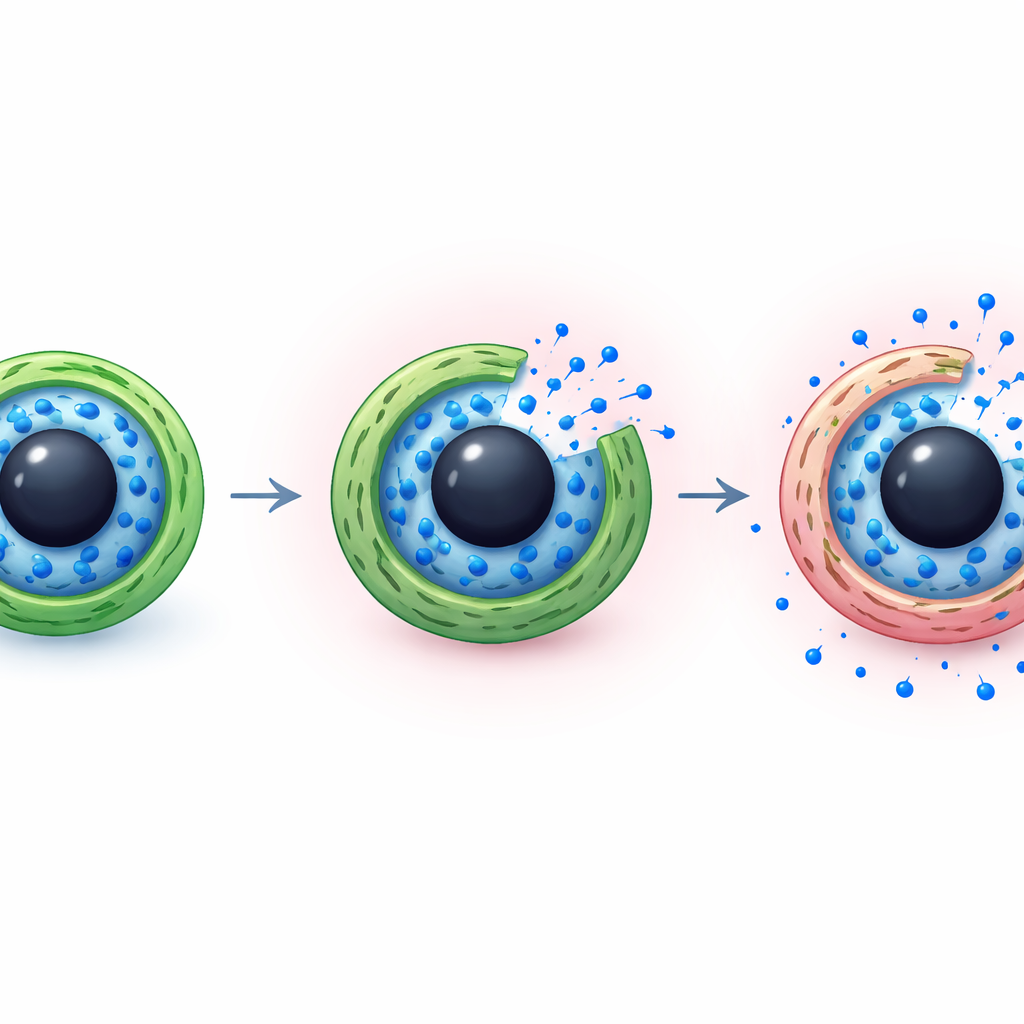
İlacın zaman içinde sızması nasıl gerçekleşiyor
Ekip ayrıca ilacın kapsüllerden fiziksel olarak nasıl çıktığını analiz etti. Ölçülen salım eğrilerini farmasötik bilimde kullanılan standart matematiksel modellerle karşılaştırarak, verilerin en iyi şekilde hem basit difüzyonun hem de polimer katmanlarının yavaş gevşemesinin birlikte çalıştığı bir tabloyla uyum gösterdiğini buldular. Nötr koşullarda sıkı kitin kaplama direnç ekleyerek imatinib moleküllerinin yavaşça dışarı akmasına neden oluyor. Asidik koşullarda ise şişmiş kabuk ve baskılanmış iç tabakadaki zayıflayan bağlanma, suyun içeri girmesini ve ilacın hareket etmesini kolaylaştırarak salımı hızlandırıyor ama kontrolsüz bir patlama haline getirmiyor. Bu kombinasyon, dolaşım sırasında ilacı güvenli şekilde tutmak ile hedefe ulaştığında kaçmasına izin vermek arasında bir denge sunuyor.
Kanser hücrelerine daha güvenli saldırı
İnsan lösemi hücreleri ve normal kan bağışıklık hücreleri üzerinde yapılan laboratuvar testleri, böyle hassas kontrolün neden önemli olduğunu gösterdi. Serbest imatinib hem kanserli hem de sağlıklı hücrelere hızla toksikti. Buna karşılık, ilaç yüklü partiküller normal hücrelere karşı çok daha nazikti; daha yüksek dozlarda ve daha uzun maruziyet sürelerinde bile, ilaç yavaşça salındıkça lösemi hücrelerini etkili şekilde öldürdüler. Özellikle kitin kaplı versiyon, kanser hücreleri üzerinde zamanla artan güçlü etkiler gösterirken çoğu normal hücreyi hayatta bıraktı; bu da serbest ilaca göre fayda ve yan etkiler arasında daha iyi bir ayrım olduğunu düşündürüyor.
Bu hastalar için ne anlama gelebilir
Toplamda, çalışma belirli bir kanser ilacını tanıyan, onu büyük miktarda taşıyan ve sağlıklı dokulardan çok tümörlerde daha fazla salan manyetik olarak yönlendirilebilen küçük bir kapsül için bir kavram kanıtı sunuyor. Bu deneyler hastalarda değil deney tüplerinde ve hücre kültürlerinde yapılmış olsa da, doktorların mıknatıslarla bu tür parçacıkları bir tümöre yönlendirebileceği, tümörün kendi asidik kimyasına güvenerek salımı tetikleyebileceği ve kemoterapiyle sıklıkla birlikte görülen yan hasarı azaltabileceği gelecekteki tedavilere işaret ediyor.
Atıf: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
Anahtar kelimeler: hedefli ilaç dağıtımı, nanopartiküller, pH-yanıt veren taşıyıcılar, imatinib, manyetik polimerler