Clear Sky Science · sv
Magnetisk molekylärt imprintskapad polymer belagd med kitsosanskal för förbättrad kontrollerad läkemedelsfrisättning
Varför detta betyder något för framtida cancerbehandlingar
Cancerläkemedel kan rädda liv, men de skadar ofta också friska celler på vägen, vilket orsakar allvarliga biverkningar och begränsar hur mycket medicin patienterna säkert kan få. Denna studie undersöker en mycket liten, smart bärare för leukemiläkemedlet imatinib som kan styras med magneter och bara öppnar sig fullt ut i sura, tumörliknande miljöer. Målet är enkelt men kraftfullt: skicka mer läkemedel precis dit det behövs, frigöra det långsamt över dagar, och skona resten av kroppen så mycket som möjligt.
Bygga en liten styrd läkemedelskapsel
Forskarna konstruerade en flerskikts nanokapsel—hundratals gånger mindre än en röd blodcell—med en magnetisk kärna i centrum. Runt denna kärna lade de ett tunt kiselskal för stabilitet, sedan ett speciellt polymerskikt formgivet kring imatinibmolekyler som ett anpassat nyckelhål runt en nyckel. Detta steg med ”molekylär imprintning” lämnar bakom sig mikroskopiska håligheter som starkt och selektivt fångar imatinib. Slutligen, efter lastning av läkemedlet, svepte de hela strukturen i ett mjukt ytterskikt gjort av kitsosan, en biopolymer relaterad till naturliga material som finns i skaldjur. Resultatet är en magnetisk, läkemedelsfylld partikel som kan dras av en extern magnet och som har inbyggd preferens för ett specifikt läkemedel.
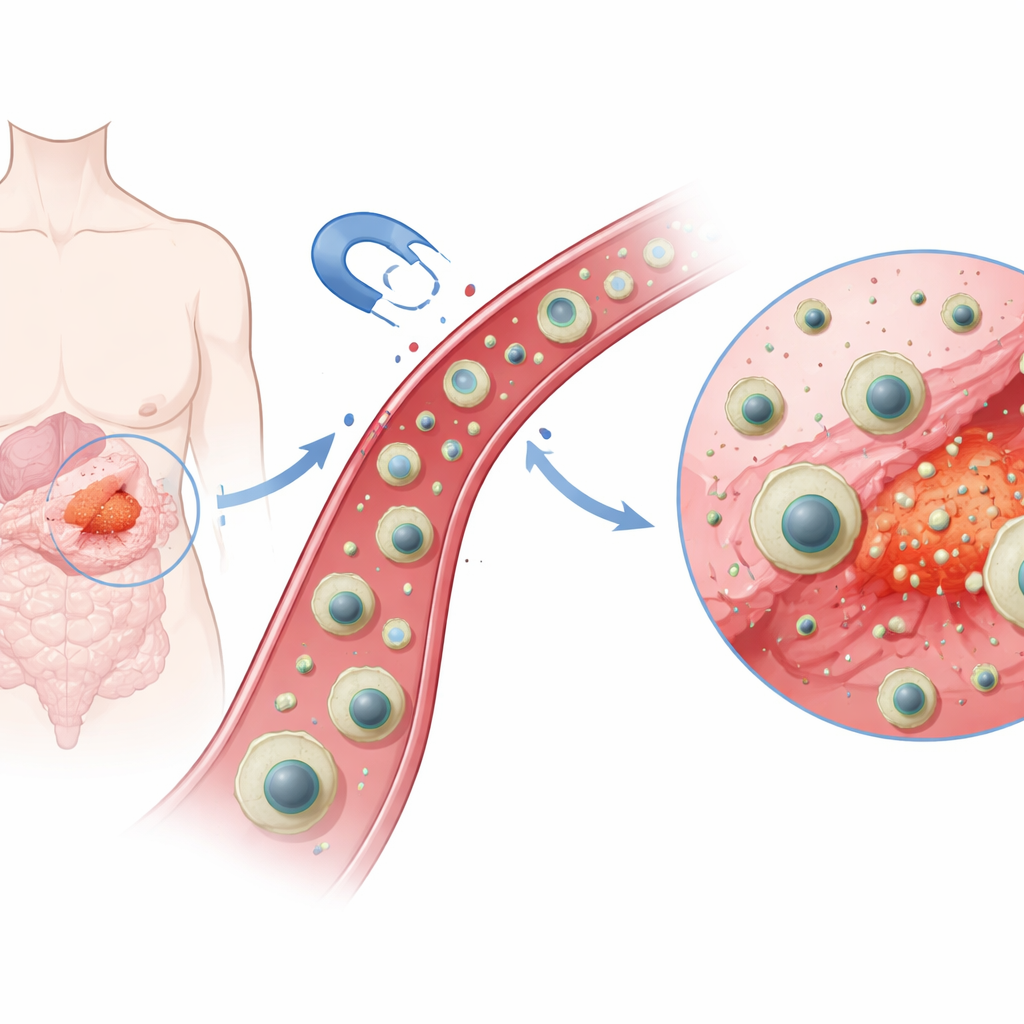
Smart respons på kroppens kemi
En av de mest slående egenskaperna hos tumörer är att deras omgivning tenderar att vara surare än normal vävnad. Teamet utnyttjade denna skillnad genom att välja kitsosan som yttre skal, eftersom dess kemiska grupper ändrar laddning beroende på pH. Vid de nästan neutrala förhållandena i frisk vävnad (runt pH 7,4) förblir kitsosanskalet relativt kompakt och mindre genomträngligt, vilket håller större delen av läkemedlet inneslutet. I en surare miljö (runt pH 5,5, liknande tumörkompartement och cellernas återvinningscentra) plockar skalets aminogrupper upp protoner, blir positivt laddade och stöter bort varandra. Detta får skalet att svälla och lossna, vilket öppnar vägar för läkemedelsmolekyler att ta sig ut.
Sätta bäraren på prov
För att se hur väl deras design fungerade mätte forskarna noggrant hur mycket imatinib partiklarna kunde hålla och hur snabbt det läckte ut under olika förhållanden. Tack vare det imprintade innerskiktet visade kapslarna en hög lastningskapacitet: ungefär två tredjedelar av deras massa kunde vara läkemedel, och de binder imatinib mycket starkare än två liknande cancerläkemedel med relaterade strukturer. När de placerades i vätskor som efterliknar kroppen frigjorde de obelagda partiklarna sitt innehåll relativt snabbt, särskilt i sura lösningar. Tillägget av kitsosanskalet bromsade allt och gjorde frisättningen starkt pH-beroende. Över fyra dagar läckte bara ungefär en fjärdedel av läkemedlet vid neutralt pH, medan runt tre fjärdedelar frigjordes under sura förhållanden, vilket indikerar att partiklarna förblir mestadels stängda i normal vävnad men öppnar mycket mer i tumörliknande miljöer.
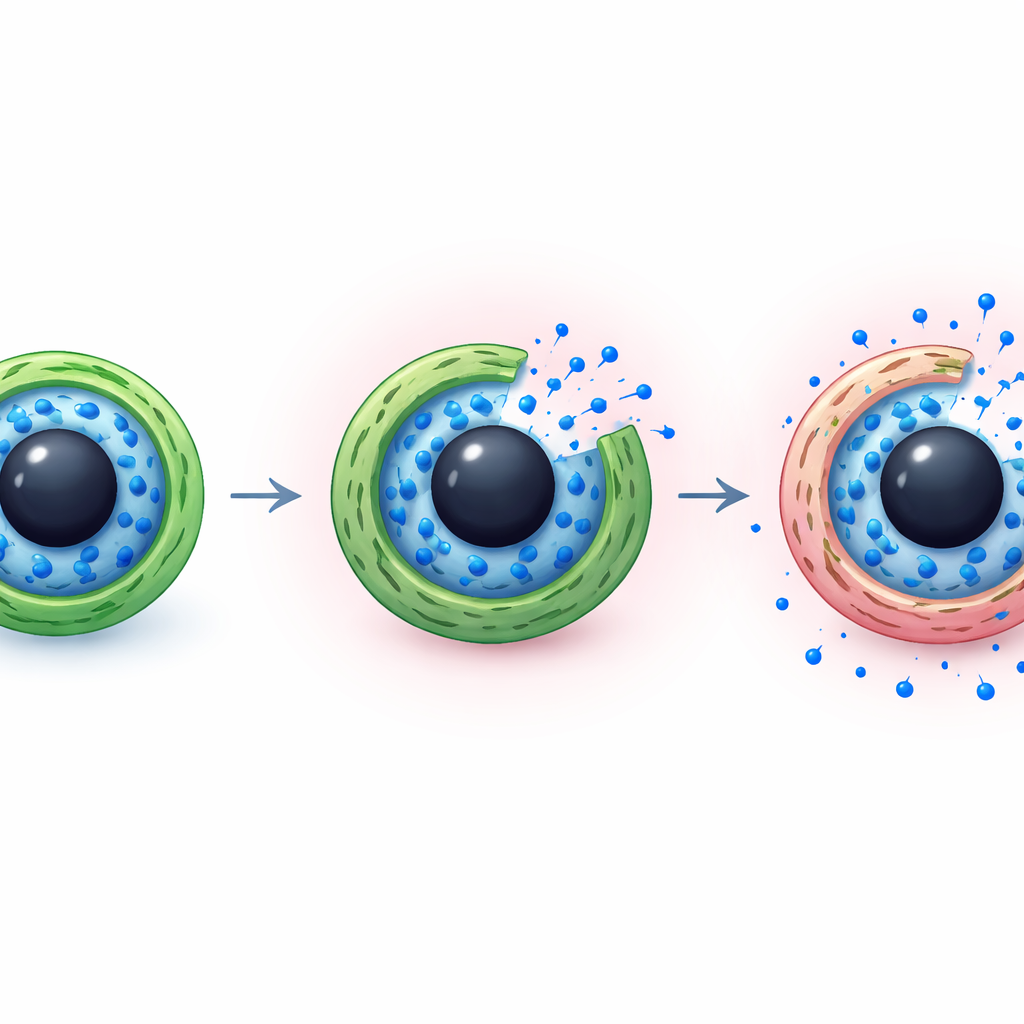
Hur läkemedlet sipprar ut över tid
Teamet analyserade också hur läkemedlet fysiskt lämnar kapslarna. Genom att jämföra mätta frisättningskurvor med standardiserade matematiska modeller som används i läkemedelsvetenskap, fann de att data bäst överensstämmer med en bild där både enkel diffusion och långsam relaxation av polymerskikten samverkar. I neutrala förhållanden tillför det täta kitsosanskiktet motstånd, så imatinibmolekylerna driver ut långsamt. I sura förhållanden gör det svällda skalet och försvagade bindningar inne i det imprintade skiktet det lättare för vatten att tränga in och för läkemedlet att röra sig, vilket snabbar upp frisättningen utan att förvandla den till ett okontrollerat rus. Denna kombination erbjuder en balans mellan att hålla medicinen säkert under cirkulation och att tillåta den att släppas när den nått sitt mål.
Säkrare angrepp på cancerceller
Laboratorietester på mänskliga leukemiceller och normala blodimmunceller visade varför sådan finjusterad kontroll spelar roll. Fritt imatinib var snabbt giftigt för både cancerceller och friska celler. I kontrast var de läkemedelslastade partiklarna mycket snällare mot normala celler, även vid högre doser och längre exponeringstider, samtidigt som de fortfarande dödade leukemiceller effektivt när läkemedlet gradvis frigjordes. Den kitsosanklädda varianten visade särskilt starkare tidsberoende effekter på cancerceller samtidigt som de flesta normala celler lämnades vid liv, vilket tyder på en bättre separation mellan nytta och biverkningar än det fria läkemedlet.
Vad detta skulle kunna innebära för patienter
Sammantaget presenterar arbetet ett proof of concept för en liten, magnetiskt styrbar kapsel som känner igen ett specifikt cancerläkemedel, bär en stor mängd av det och frigör det mer i tumörer än i frisk vävnad. Även om dessa experiment utfördes i provrör och cellkulturer snarare än på patienter, pekar de mot framtida behandlingar där läkare kan styra sådana partiklar mot en tumör med magneter, förlita sig på tumörens egen sura kemi för att utlösa frisättning, och minska de sidoeffekter som så ofta följer med kemoterapi.
Citering: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
Nyckelord: riktad läkemedelsleverans, nanopartiklar, pH-känsliga bärare, imatinib, magnetiska polymerer