Clear Sky Science · nl
Magnetische moleculair geïmplanteerde polymeer gecoat met chitosanomhulsel voor verbeterde gecontroleerde medicijnafgifte
Waarom dit belangrijk is voor toekomstige kankerbehandelingen
Kankermedicijnen kunnen levensreddend zijn, maar ze beschadigen vaak ook gezonde cellen, veroorzaken ernstige bijwerkingen en beperken hoeveel medicatie patiënten veilig kunnen krijgen. Deze studie onderzoekt een klein, slim dragersysteem voor het leukemiemedicijn imatinib dat door magneten gestuurd kan worden en alleen volledig opengaat in zure, tumorachtige omgevingen. Het doel is eenvoudig maar krachtig: meer medicijn precies daar afleveren waar het nodig is, het langzaam vrijgeven over dagen, en de rest van het lichaam zoveel mogelijk sparen.
Het bouwen van een klein geleid medicijnkapsel
De onderzoekers ontwierpen een gelaagd nanokapsel — honderden malen kleiner dan een rode bloedcel — met een magnetische kern in het midden. Rond die kern plaatsten ze een dunne silicalaag voor stabiliteit, gevolgd door een speciale polymeerlaag die rondom imatinibmoleculen werd gevormd als een op maat gemaakt sleutelgat rond een sleutel. Deze stap van “moleculaire imprinting” laat microscopische holtes achter die imatinib sterk en selectief vastleggen. Nadat het medicijn geladen was, omsloten ze de hele structuur met een zachte buitenlaag van chitosan, een biopolymeer verwant aan natuurlijke materialen uit schaaldieren. Het resultaat is een magnetisch, medicijngevuld deeltje dat door een externe magneet kan worden bewogen en dat een ingebouwde voorkeur heeft voor één specifiek geneesmiddel.
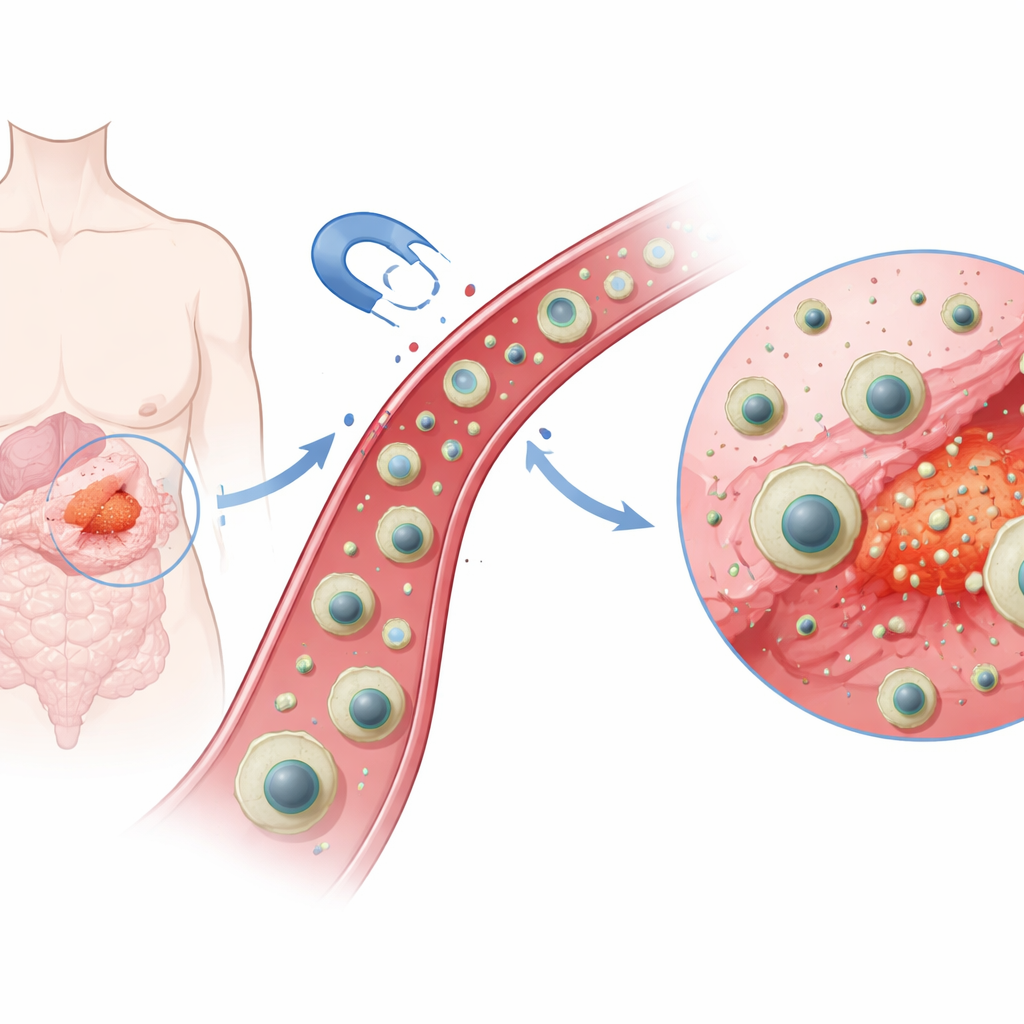
Slimme reactie op de chemie van het lichaam
Een van de meest opvallende kenmerken van tumoren is dat hun omgeving vaak zuurder is dan normale weefsels. Het team maakte gebruik van dit verschil door chitosan als buitenste laag te kiezen, omdat de chemische groepen daarin van lading veranderen afhankelijk van de pH. Onder de nagenoeg neutrale omstandigheden van gezonde weefsels (rond pH 7,4) blijft de chitosanlaag relatief compact en minder doorlaatbaar, waardoor het grootste deel van het medicijn binnen blijft. In een zuurdere omgeving (rond pH 5,5, vergelijkbaar met tumorcompartimenten en celrecyclingcentra) nemen de aminegroepen van de laag protonen op, worden positief geladen en stoten ze elkaar af. Dit doet de omhulling zwellen en versoepelen, waardoor paden openkomen voor medicijnmoleculen om te ontsnappen.
De drager op de proef stellen
Om te zien hoe goed hun ontwerp werkte, maten de wetenschappers nauwkeurig hoeveel imatinib de deeltjes konden opnemen en hoe snel het onder verschillende omstandigheden uitlekte. Dankzij de geïmplanteerde binnenlaag toonden de capsules een hoge laadcapaciteit: ongeveer tweederde van hun massa kon uit medicijn bestaan, en ze bonden imatinib veel sterker dan twee vergelijkbare kankermiddelen met verwante structuren. In lichaamsachtige vloeistoffen gaven de niet-gecoate deeltjes hun lading relatief snel af, vooral in zure oplossingen. Het toevoegen van de chitosanomhulsel vertraagde het proces en maakte de afgifte sterk pH-afhankelijk. Over vier dagen ontsnapte slechts ongeveer een kwart van het medicijn bij neutrale pH, terwijl ruwweg driekwart werd vrijgegeven onder zure condities, wat aangeeft dat de deeltjes in normale weefsels grotendeels gesloten blijven maar veel meer openen in tumorachtige omgevingen.
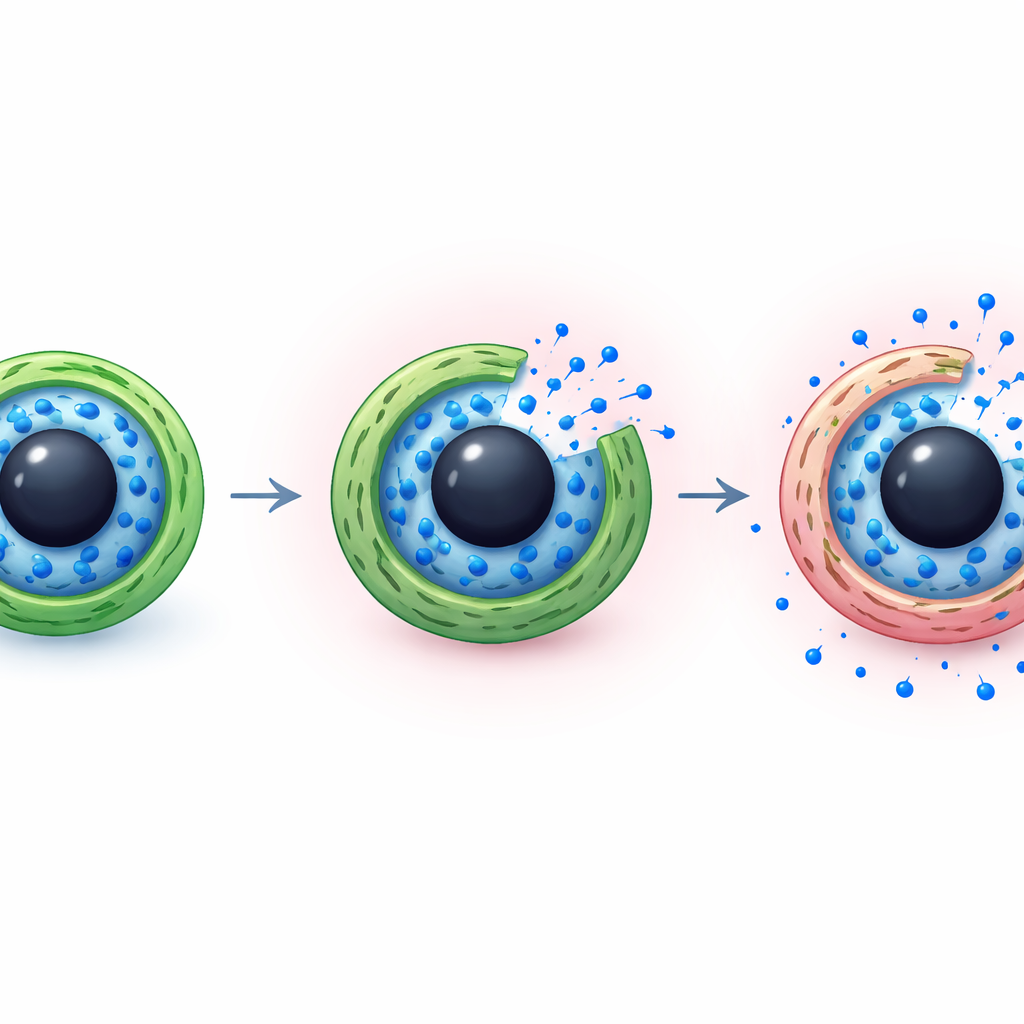
Hoe het medicijn in de loop van de tijd sijpelt
Het team analyseerde ook op welke fysieke manier het medicijn de capsules verlaat. Door de gemeten afgiftecurven te vergelijken met standaard wiskundige modellen die in de farmaceutische wetenschap worden gebruikt, vonden ze dat de gegevens het beste passen bij een beeld waarin zowel eenvoudige diffusie als langzame relaxatie van de polymeerlagen samenwerken. In neutrale omstandigheden voegt de strakke chitosancoating weerstand toe, waardoor imatinibmoleculen langzaam naar buiten drijven. In zure omstandigheden maken de gezwollen omhulling en de verzwakte bindingen in de geïmplanteerde laag het makkelijker voor water om binnen te dringen en voor het medicijn om te bewegen, waardoor de afgifte versnelt zonder te veranderen in een ongecontroleerde uitbarsting. Deze combinatie biedt een balans tussen het veilig vasthouden van het geneesmiddel tijdens circulatie en het toestaan dat het vrijkomt zodra het zijn doel heeft bereikt.
Veiliger aanval op kankercellen
Laboratoriumtests op menselijk leukemiesysteem en normale bloedimmuuncellen toonden aan waarom zo’n fijn afgestemde controle belangrijk is. Vrij imatinib was snel toxisch voor zowel kankercellen als gezonde cellen. In tegenstelling daarmee waren de medicijngeladen deeltjes veel milder voor normale cellen, zelfs bij hogere doses en langere blootstellingstijden, terwijl ze toch leukemiecellen efficiënt doodden naarmate het medicijn geleidelijk werd vrijgegeven. De chitosangecoate versie toonde met name sterkere tijdsafhankelijke effecten op kankercellen terwijl de meeste normale cellen in leven bleven, wat wijst op een betere scheiding tussen voordeel en bijwerkingen dan bij het vrije medicijn.
Wat dit voor patiënten zou kunnen betekenen
Alles bij elkaar presenteert het werk een proof of concept voor een klein, magnetisch stuurbaar kapsel dat een specifiek kankermedicijn herkent, grote hoeveelheden ervan vervoert en meer in tumoren loslaat dan in gezonde weefsels. Hoewel deze experimenten in reageerbuizen en celkweken zijn uitgevoerd en niet bij patiënten, wijzen ze op toekomstige behandelingen waarbij artsen zulke deeltjes met magneten naar een tumor zouden kunnen leiden, vertrouwen op de zure chemie van de tumor om afgifte te activeren, en de bijkomende schade die vaak samengaat met chemotherapie kunnen verminderen.
Bronvermelding: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
Trefwoorden: gerichte medicijnafgifte, nanodeeltjes, pH-responsieve dragers, imatinib, magnetische polymeren