Clear Sky Science · ru
Молекулярно импринтованный магнитный полимер в оболочке из хитозана для улучшенного контролируемого высвобождения лекарства
Почему это важно для будущего лечения рака
Противораковые препараты могут спасать жизни, но часто повреждают здоровые клетки, вызывая серьёзные побочные эффекты и ограничивая допустимые дозы. В этом исследовании изучают крошечный «умный» носитель для препарата от лейкемии иматиниба, которым можно управлять с помощью магнитов и который полностью открывается лишь в кислом, похожем на опухоль, окружении. Цель проста, но значительна: доставить больше лекарства точно туда, где оно нужно, выпускать его медленно в течение дней и по возможности щадить остальную часть организма.
Создание миниатюрной управляемой капсулы лекарства
Исследователи сконструировали многослойную нанокапсулу — в сотни раз меньшую, чем красная кровяная клетка — с магнитным ядром в центре. Вокруг ядра они нанесли тонкую кремнезёмную оболочку для устойчивости, затем специальный полимерный слой, сформованный вокруг молекул иматиниба, как индивидуальное «замочное отверстие» под ключ. Этот шаг молекулярного импринтинга оставляет микроскопические полости, которые сильно и селективно захватывают иматиниб. Наконец, после загрузки лекарства всю структуру оболачивают мягкой внешней плёнкой из хитозана — биополимера, близкого по природе к веществам, встречающимся в панцирях ракообразных. В результате получают магнитную частицу, заполненную лекарством, которую можно притянуть внешним магнитом и которая обладает встроенной селективностью к конкретному препарату.
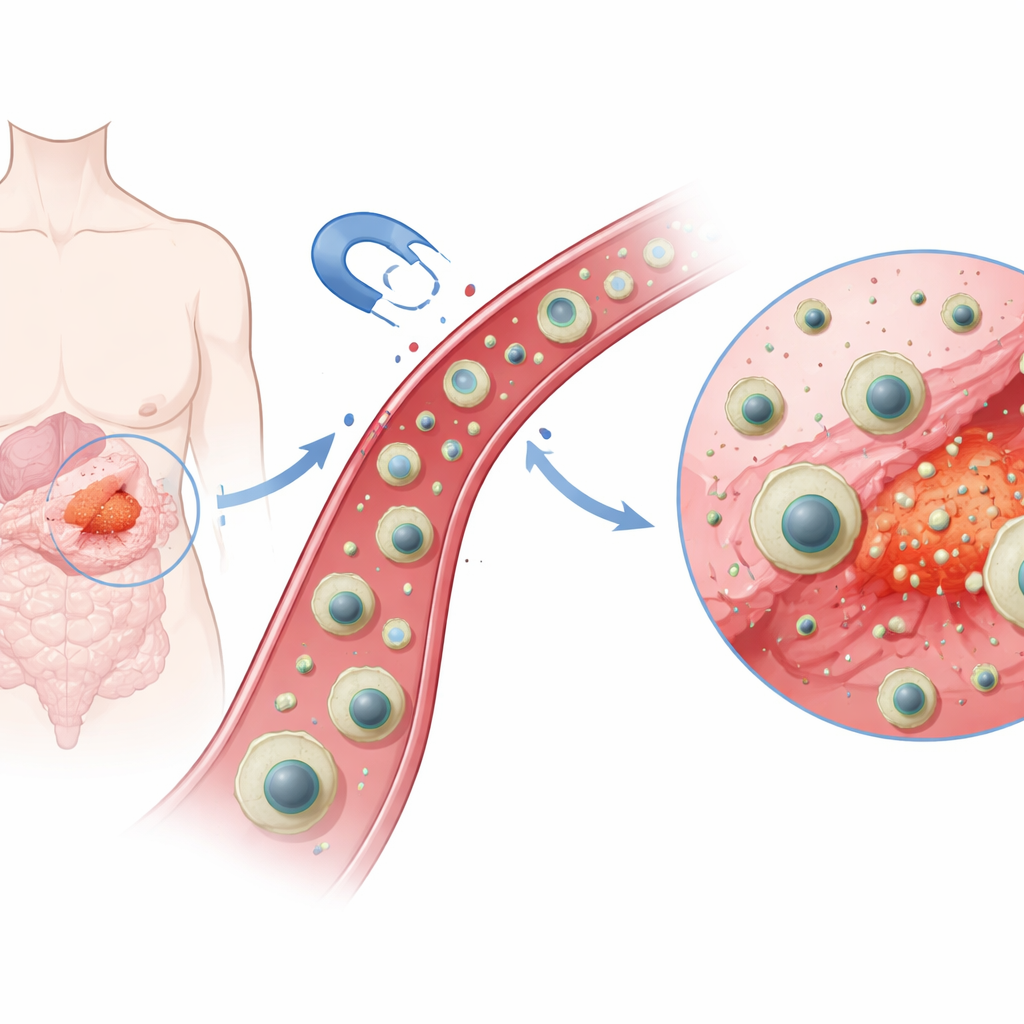
Интеллектуальный отклик на химию организма
Одна из характерных черт опухолей — их окружение обычно более кислое, чем в нормальных тканях. Команда использовала это различие, выбрав хитозан в качестве наружной оболочки, поскольку его химические группы меняют заряд в зависимости от pH. При близких к нейтральным условиях здоровых тканей (около pH 7,4) оболочка из хитозана остаётся относительно компактной и менее проницаемой, удерживая основную часть лекарства внутри. В более кислой среде (около pH 5,5, что похоже на опухолевые компартменты и клеточные перерабатывающие центры) аминогруппы хитозана присоединяют протоны, приобретают положительный заряд и отталкивают друг друга. Это вызывает набухание оболочки и её ослабление, открывая пути для выхода молекул лекарства.
Проверка носителя в действии
Чтобы оценить эффективность конструкции, учёные тщательно измеряли, сколько иматиниба частицы могут вместить и как быстро он выходит при разных условиях. Благодаря импринтованному внутреннему слою капсулы продемонстрировали высокую загрузочную способность: примерно две трети их массы приходились на лекарство, и они связывали иматиниб существенно сильнее, чем два схожих противораковых препарата с родственными структурами. В жидкостях, имитирующих биологическую среду, немодифицированные частицы быстро выпускали содержимое, особенно в кислых растворах. Добавление хитозановой оболочки замедляло процесс и делало высвобождение сильно зависимым от pH. За четыре дня при нейтральном pH вышло лишь около четверти лекарства, тогда как в кислых условиях было освобождено примерно три четверти, что указывает на то, что частицы в нормальных тканях в основном закрыты, но гораздо более открыты в опухолеобразных условиях.
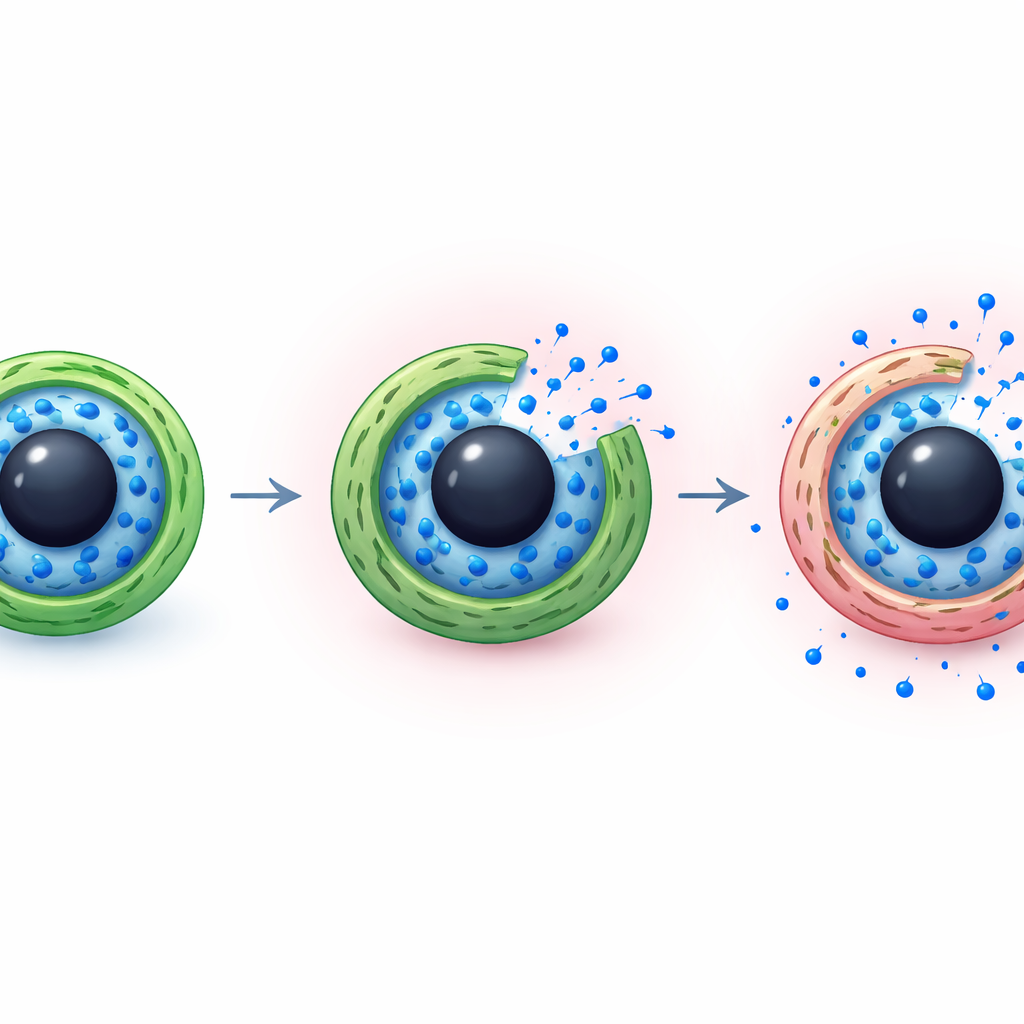
Как лекарство просачивается со временем
Команда также проанализировала физические механизмы выхода лекарства из капсул. Сравнивая экспериментальные кривые высвобождения со стандартными математическими моделями, применяемыми в фармацевтической науке, они обнаружили наилучшее соответствие сценарию, в котором одновременно действуют простая диффузия и медленная релаксация полимерных слоёв. В нейтральных условиях плотно прилегающая хитозановая оболочка создаёт сопротивление, поэтому молекулы иматиниба медленно диффундируют наружу. В кислой среде набухшая оболочка и ослабевшие связи во внутриимпринтованном слое облегчают проникновение воды и движение лекарства, ускоряя высвобождение, но не превращая его в неконтролируемый всплеск. Такое сочетание обеспечивает баланс между надёжным удержанием препарата во время циркуляции и его освобождением после достижения цели.
Более безопасная атака на раковые клетки
Лабораторные испытания на человеческих лейкемических клетках и нормальных иммунных клетках крови показали, почему такая тонкая настройка важна. Свободный иматиниб быстро оказывал токсическое действие и на раковые, и на здоровые клетки. В отличие от этого, загруженные лекарством частицы были значительно мягче для нормальных клеток, даже при более высоких дозах и длительном воздействии, при этом они эффективно убивали лейкемические клетки по мере постепенного высвобождения препарата. Особенно хитозановая версия демонстрировала усиленные временные эффекты на раковые клетки, оставляя большинства нормальных клеток живыми, что предполагает лучшее разделение пользы и побочных эффектов по сравнению со свободным препаратом.
Что это может значить для пациентов
В целом работа представляет доказательство концепции крошечной магнитно управляемой капсулы, которая распознаёт конкретное противораковое средство, несёт его в значительном количестве и высвобождает больше в опухолях, чем в здоровых тканях. Хотя эти эксперименты проводились в пробирках и культурах клеток, а не на пациентах, они указывают на перспективу будущих методов лечения, когда врачи смогут направлять такие частицы к опухоли с помощью магнитов, полагаться на кислую химию самой опухоли для запуска высвобождения и уменьшать сопутствующий ущерб, часто сопровождающий химиотерапию.
Цитирование: Sadri, N., Mazloum-Ardakani, M., Joseph, Y. et al. Magnetic molecularly imprinted polymer coated with chitosan shell for enhanced controlled drug release. Sci Rep 16, 11015 (2026). https://doi.org/10.1038/s41598-026-41273-0
Ключевые слова: целевое доставление лекарств, наночастицы, рН-ответственные носители, иматиниб, магнитные полимеры