Clear Sky Science · zh
FKBP51破坏胰岛素信号通路并损害HepG2细胞的线粒体生物能学
压力、糖分与肝脏
现代生活带来了慢性压力、富裕饮食和不断上升的2型糖尿病发病率。本研究考察了一种鲜为人知的与应激相关的蛋白FKBP51,以及它如何改变肝细胞对胰岛素的响应和能量利用。通过对体外人源肝细胞的精细观察,研究者表明FKBP51既能削弱胰岛素的信号传导,又在细胞能量工厂——线粒体内悄然耗损能量。理解这种拉锯可能有助于解释为何长期压力与代谢性疾病常常并存。
一个应激蛋白涉足代谢
FKBP51最著名的是作为由应激激素皮质醇激活的辅佐蛋白。早期研究已将其与肌肉、脂肪和大脑的体重增加及胰岛素抵抗联系起来。然而其在肝脏这一血糖调控核心器官中的作用尚不清楚。在本研究中,科学家使用了广泛应用的人类肝细胞模型HepG2,并人为提高FKBP51的表达以观察其对胰岛素信号传导和糖代谢的影响。他们关注胰岛素通路中的关键分子以及线粒体产生能量的方式,探讨FKBP51是否可能是应激、肝功能失调与高血糖之间的缺失环节。
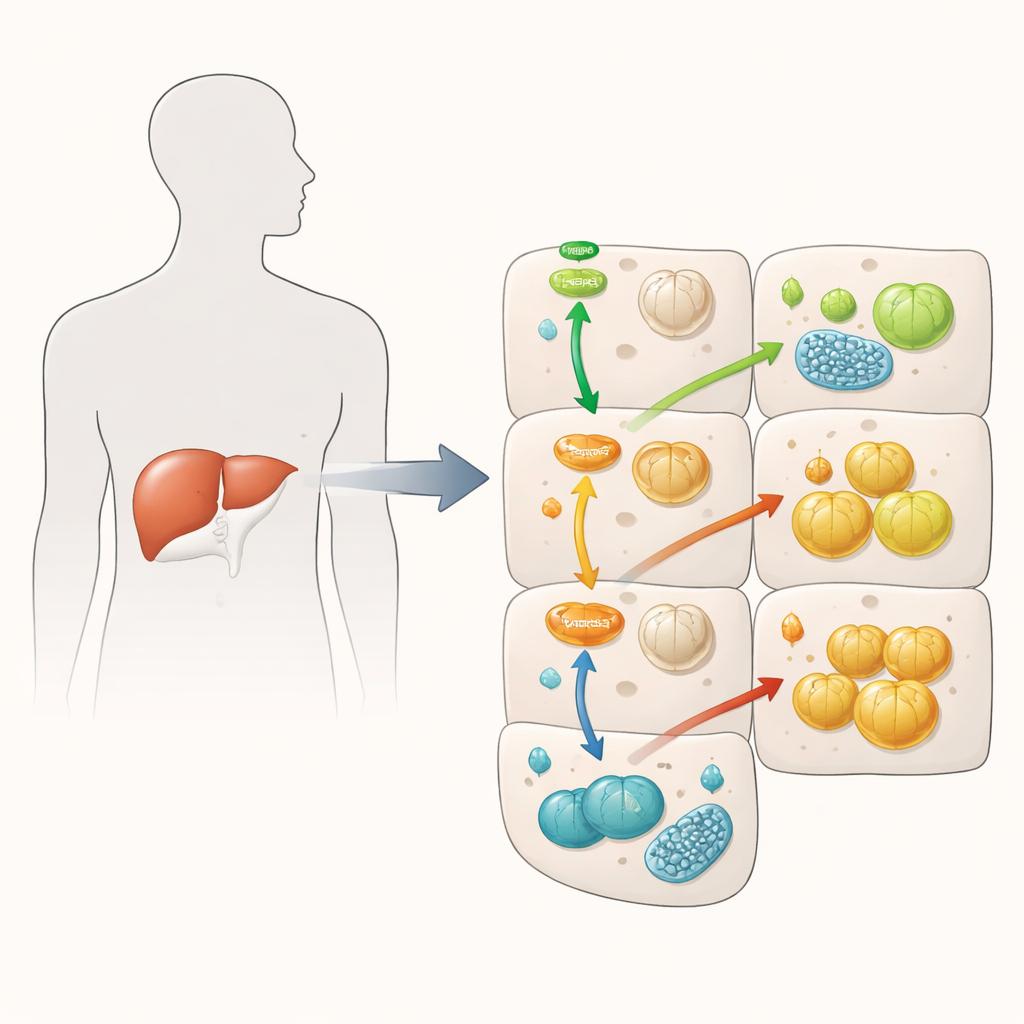
胰岛素信号减弱,但糖原储存增加
当胰岛素与肝细胞结合时,通常会激活一系列蛋白,降低血糖——通过促进糖原储存并减少新糖生成。研究团队证实了额外的FKBP51会削弱这条链路:它降低了作为胰岛素关键信使的Akt和调控促糖异生基因的FOXO1的激活。从理论上讲,这应导致更差的血糖控制。但令人惊讶的是,某些方面结果相反。富含FKBP51的细胞即便在被刺激产生新葡萄糖时也产生更少的新糖,而且在胰岛素存在时,它们的糖原储备反而比对照细胞更多。这表明FKBP51打乱了胰岛素通路的常规逻辑——通过替代途径抑制某些信号同时增强另一些信号。
能量工厂功能下降但外观不变
由于肝脏制造或储存糖的能力在很大程度上依赖于线粒体,研究者接着详细检查了这些细胞器。他们发现约一半细胞内的FKBP51定位于线粒体,确认了二者的物理联系。然而在显微镜下,线粒体的大小和形态在FKBP51升高或胰岛素处理下总体上看起来正常。变化体现在功能上:无论是FKBP51过表达还是胰岛素处理,都降低了线粒体的耗氧量、降低了其膜电位,并削减了细胞内的ATP这一能量货币。重要的是,富含FKBP51的细胞本就处于较低的能量状态,胰岛素进一步将ATP水平压低,但并未伴随有害活性氧的升高。
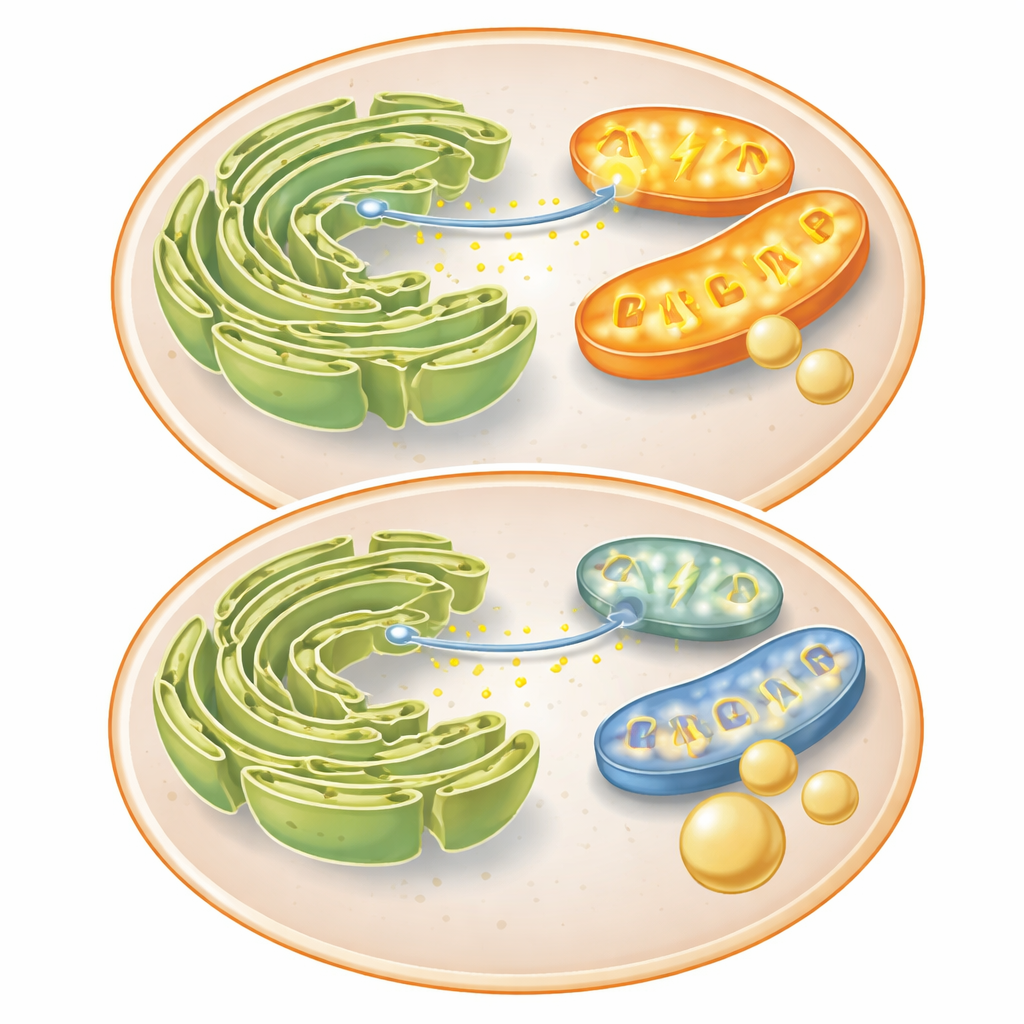
两个关键细胞器之间的对话中断
为弄清线粒体为何功能受损,团队考察了将线粒体与另一结构——内质网(ER,钙离子储存地)连接起来的蛋白。对于线粒体融合及与内质网紧密接触都很重要的蛋白Mitofusin 2在FKBP51高表达时下降。这些接触点通常允许钙快速从内质网流入线粒体,从而增强产能酶活。在对照细胞中,一个化学信号会引发线粒体内强烈的钙爆发;胰岛素和FKBP51都减慢了这种转移。FKBP51还降低了细胞胞液内的钙峰值,暗示其阻碍了内质网的钙释放。随着到达线粒体的钙减少,其能量产出下降,推动细胞远离耗能的过程(如糖异生),转而更倾向于将进入的糖储存为糖原。
对健康的意义
简言之,这项研究表明FKBP51在肝细胞中充当一种双刃的应激响应因子。一方面,它干扰胰岛素的早期信号步骤,这与胰岛素抵抗相关;另一方面,它通过扰乱内质网与线粒体之间的钙交换削弱能量制造机制。综合效应是肝细胞减少新糖生成,但更倾向于将可用糖以糖原形式储存,即便经典的胰岛素信号部分被抑制。对人体而言,这项工作提示长期压力——通过像FKBP51这样的蛋白——可能以微妙方式重塑肝脏能量利用,从而助长代谢性疾病。针对FKBP51或内质网-线粒体钙连接的干预,将来可能提供不使细胞能量工厂过度负担的新策略来微调血糖控制。
引用: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
关键词: 胰岛素抵抗, 肝脏代谢, 线粒体功能, 细胞应激, 钙信号