Clear Sky Science · es
FKBP51 interrumpe la vía de señalización de la insulina y deteriora la bioenergética mitocondrial en células HepG2
Estrés, azúcar y el hígado
La vida moderna trae estrés crónico, dietas ricas y tasas crecientes de diabetes tipo 2. Este estudio examina una proteína poco conocida relacionada con el estrés llamada FKBP51 y cómo modifica la respuesta de las células hepáticas a la insulina y el uso de energía. Al centrarse en células humanas derivadas del hígado en el laboratorio, los investigadores muestran que FKBP51 puede tanto atenuar la señal de la insulina como drenar silenciosamente la producción de energía dentro de las centrales celulares, las mitocondrias. Entender esta tensión puede ayudar a explicar por qué el estrés prolongado y las enfermedades metabólicas con frecuencia van de la mano.
Una proteína del estrés entra en el metabolismo
FKBP51 es conocida principalmente como una proteína coadyuvante activada por la hormona del estrés, el cortisol. Trabajos previos la vincularon con aumento de peso y resistencia a la insulina en músculo, grasa y cerebro. Sin embargo, su papel en el hígado —un órgano central para el control de la glucemia— no se comprendía bien. En este estudio, los científicos emplearon células HepG2, un modelo humano de hígado ampliamente usado, y aumentaron artificialmente los niveles de FKBP51 para ver cómo afectaba la señalización de la insulina y el manejo de la glucosa. Se centraron en moléculas clave de la vía de la insulina y en cómo las mitocondrias generan energía, preguntándose si FKBP51 podría ser un eslabón perdido entre el estrés, la disfunción hepática y la hiperglucemia.
Se debilita la señal de la insulina, pero aumenta el almacenamiento de azúcar
Cuando la insulina se une a las células hepáticas, normalmente activa una cadena de proteínas que reduce la glucosa en sangre promoviendo el almacenamiento en forma de glucógeno y disminuyendo la producción de nueva glucosa. El equipo confirmó que el exceso de FKBP51 debilita esta cadena: redujo la activación de Akt, un mensajero central de la insulina, y de FOXO1, un regulador de genes que impulsa al hígado a producir glucosa. En teoría, esto debería traducirse en un peor control de la glucosa. Sorprendentemente, ocurrió lo contrario en algunos aspectos. Las células ricas en FKBP51 generaron menos glucosa nueva incluso cuando se les estimuló, y con insulina presente, almacenaron más glucógeno que las células control. Esto sugiere que FKBP51 enreda la lógica habitual de la vía de la insulina, atenuando algunas señales mientras potencia otras por rutas alternativas.
Las centrales energéticas rinden menos sin cambiar de forma
Dado que la capacidad del hígado para producir o almacenar glucosa depende en gran medida de las mitocondrias, los investigadores examinaron estos orgánulos en detalle. Encontraron que alrededor de la mitad de la señal de FKBP51 dentro de las células se localiza en las mitocondrias, confirmando un vínculo físico. Aun así, al microscopio, el tamaño y la forma mitocondriales parecían en gran medida normales, incluso cuando FKBP51 era alto o se añadió insulina. En cambio, los cambios fueron funcionales. Tanto la sobreexpresión de FKBP51 como el tratamiento con insulina redujeron el consumo de oxígeno mitocondrial, bajaron su potencial de membrana eléctrica y recortaron el ATP celular, la moneda química de la energía. Es importante destacar que las células ricas en FKBP51 partían de un estado energético ya deprimido, y la insulina redujo aún más los niveles de ATP, sin un aumento de especies reactivas de oxígeno dañinas.
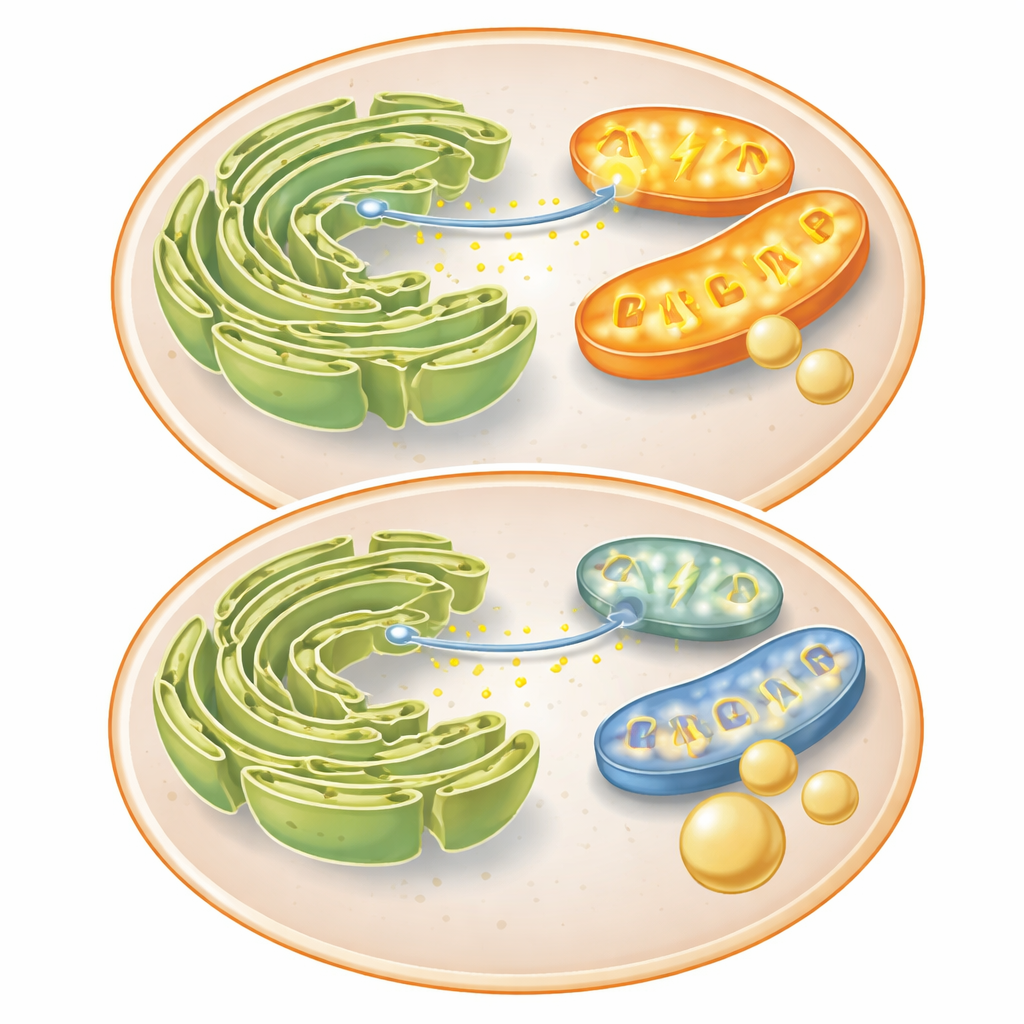
Conversación rota entre dos orgánulos clave
Para entender por qué las mitocondrias funcionaban peor, el equipo analizó proteínas que las conectan con otra estructura, el retículo endoplásmico (RE), donde se almacena el calcio. La proteína Mitofusina 2, importante tanto para la fusión mitocondrial como para el contacto estrecho con el RE, disminuyó cuando FKBP51 era elevado. Estos contactos normalmente permiten que el calcio se mueva rápidamente del RE a las mitocondrias, potenciando enzimas productoras de energía. En las células control, una señal química provocó una fuerte oleada de calcio hacia las mitocondrias; la insulina y FKBP51 ralentizaron esta transferencia. FKBP51 también redujo los picos de calcio en el citosol, lo que implica que dificulta la liberación de calcio desde el RE. Con menos calcio llegando a las mitocondrias, su producción energética cae, empujando a la célula lejos de procesos costosos como la producción de glucosa y hacia el almacenamiento del azúcar entrante.
Qué significa esto para la salud
En términos sencillos, el estudio sugiere que FKBP51 actúa como un respondedor al estrés con doble filo en las células hepáticas. Por un lado, interfiere con los primeros pasos de la señalización de la insulina, una característica asociada a la resistencia a la insulina. Por otro, debilita la maquinaria productora de energía al alterar el intercambio de calcio entre el RE y las mitocondrias. El efecto combinado es una célula hepática que produce menos glucosa nueva pero tiende más a almacenar el azúcar disponible como glucógeno, incluso cuando las señales clásicas de la insulina están parcialmente silenciadas. Para las personas, este trabajo sugiere que el estrés crónico —a través de proteínas como FKBP51— puede remodelar sutilmente el uso de energía hepática y contribuir a las enfermedades metabólicas. Dirigirse a FKBP51 o a la conexión de calcio entre RE y mitocondrias podría algún día ofrecer nuevas estrategias para afinar el control de la glucemia sin sobrecargar las centrales energéticas de la célula.
Cita: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
Palabras clave: resistencia a la insulina, metabolismo hepático, función mitocondrial, estrés celular, señalización por calcio