Clear Sky Science · pl
FKBP51 zakłóca szlak sygnalizacji insuliny i upośledza bioenergetykę mitochondriów w komórkach HepG2
Stres, cukier i wątroba
Współczesne życie przynosi przewlekły stres, bogate diety i rosnącą zapadalność na cukrzycę typu 2. To badanie dotyczy mało znanego białka związanego ze stresem, FKBP51, i tego, jak zmienia ono reakcję komórek wątroby na insulinę oraz ich gospodarkę energetyczną. Analizując komórki pochodzenia ludzkiego hodowane w laboratorium, badacze wykazali, że FKBP51 może zarówno tłumić sygnał insuliny, jak i cicho osłabiać produkcję energii w wewnętrznych elektrowniach komórkowych — mitochondriach. Zrozumienie tego wewnątrzkomórkowego przeciągania liny może pomóc wyjaśnić, dlaczego długotrwały stres i choroby metaboliczne tak często idą w parze.
Białko stresowe wkracza w metabolizm
FKBP51 jest najbardziej znane jako białko pomocnicze aktywowane przez hormon stresu — kortyzol. Wcześniejsze prace powiązały je ze wzrostem masy ciała i insulinoopornością w mięśniach, tkance tłuszczowej i mózgu. Jego rola w wątrobie — narządzie kluczowym dla kontroli poziomu glukozy we krwi — nie była jednak dobrze poznana. W tym badaniu naukowcy wykorzystali komórki HepG2, szeroko stosowany model ludzkich komórek wątroby, i sztucznie podnieśli poziom FKBP51, by sprawdzić, jak wpłynie to na sygnalizację insuliny i metabolizm cukru. Skoncentrowali się na kluczowych molekułach szlaku insulinowego oraz na tym, jak mitochondria wytwarzają energię, pytając, czy FKBP51 może być brakującym ogniwem łączącym stres, dysfunkcję wątroby i wysoki poziom cukru we krwi.
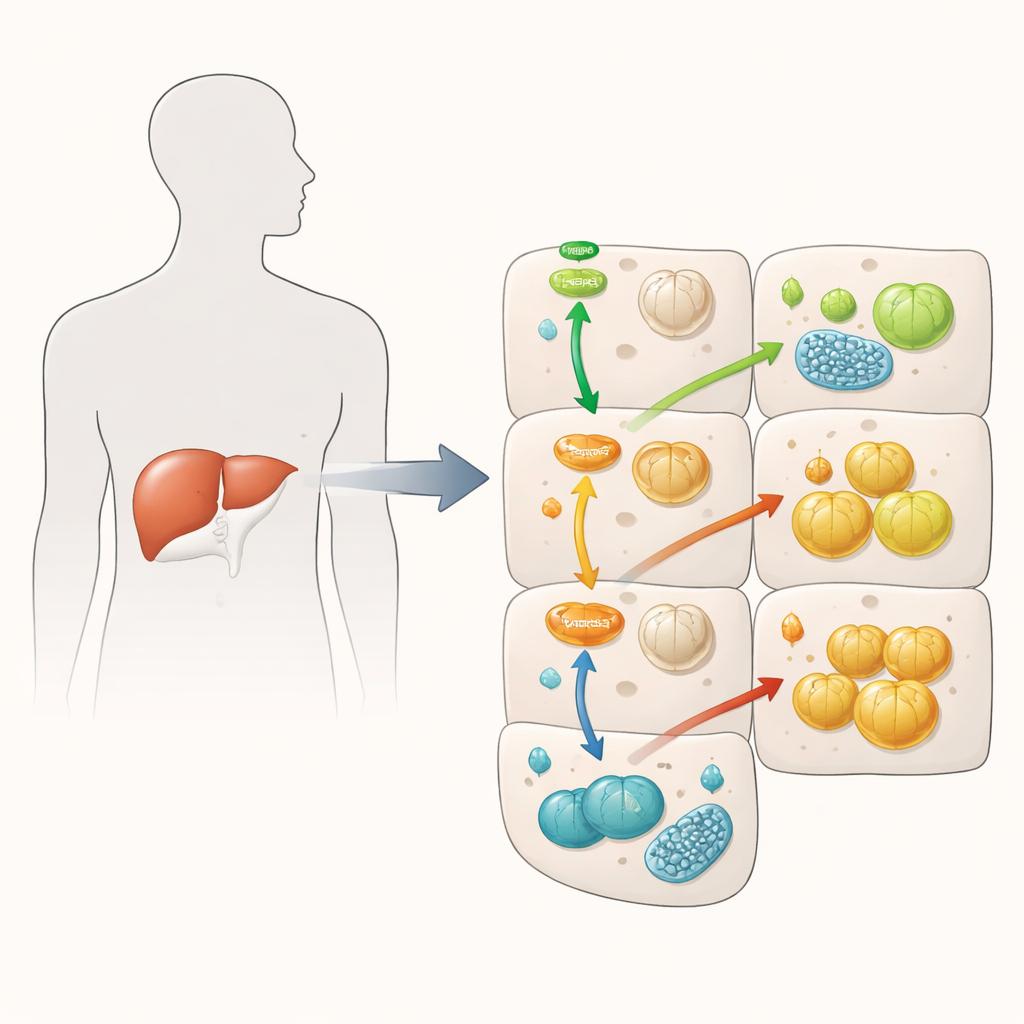
Sygnał insuliny osłabiony, a mimo to rośnie magazynowanie cukru
Kiedy insulina wiąże się z komórkami wątroby, normalnie aktywuje łańcuch białek obniżających poziom cukru przez promowanie magazynowania glukozy w postaci glikogenu i hamowanie jej nowej produkcji. Zespół potwierdził, że nadmiar FKBP51 osłabia ten łańcuch: zmniejszał aktywację Akt — centralnego przekaźnika insuliny — oraz FOXO1, regulatora genów napędzających wątrobę do wytwarzania nowej glukozy. Na papierze powinno to prowadzić do gorszej kontroli cukru. Zaskakująco jednak w pewnych aspektach stało się odwrotnie. Komórki bogate w FKBP51 wytwarzały mniej nowej glukozy nawet przy stymulacji, a w obecności insuliny faktycznie magazynowały więcej glikogenu niż komórki kontrolne. Sugeruje to, że FKBP51 miesza zwykłą logikę szlaku insulinowego, tłumiąc niektóre sygnały przy jednoczesnym wzmacnianiu innych przez alternatywne drogi.
Elektrownie zawiodły funkcjonalnie, bez zmiany kształtu
Ponieważ zdolność wątroby do wytwarzania lub magazynowania cukru zależy w dużym stopniu od mitochondriów, badacze przyjrzeli się tym organellom szczegółowo. Odkryli, że około połowa sygnału FKBP51 w komórkach znajduje się przy mitochondriach, potwierdzając fizyczne powiązanie. Jednak pod mikroskopem rozmiar i kształt mitochondriów pozostały w dużej mierze normalne, nawet przy wysokim poziomie FKBP51 lub po dodaniu insuliny. Zmiany były zamiast tego funkcjonalne. Zarówno nadekspresja FKBP51, jak i leczenie insuliną zmniejszały zużycie tlenu przez mitochondria, obniżały ich potencjał błonowy i redukowały komórkowe ATP, chemiczną walutę energii. Co istotne, komórki z wysokim poziomem FKBP51 startowały z już obniżonym stanem energetycznym, a insulina dodatkowo obniżała poziomy ATP, bez wzrostu szkodliwych reaktywnych form tlenu.
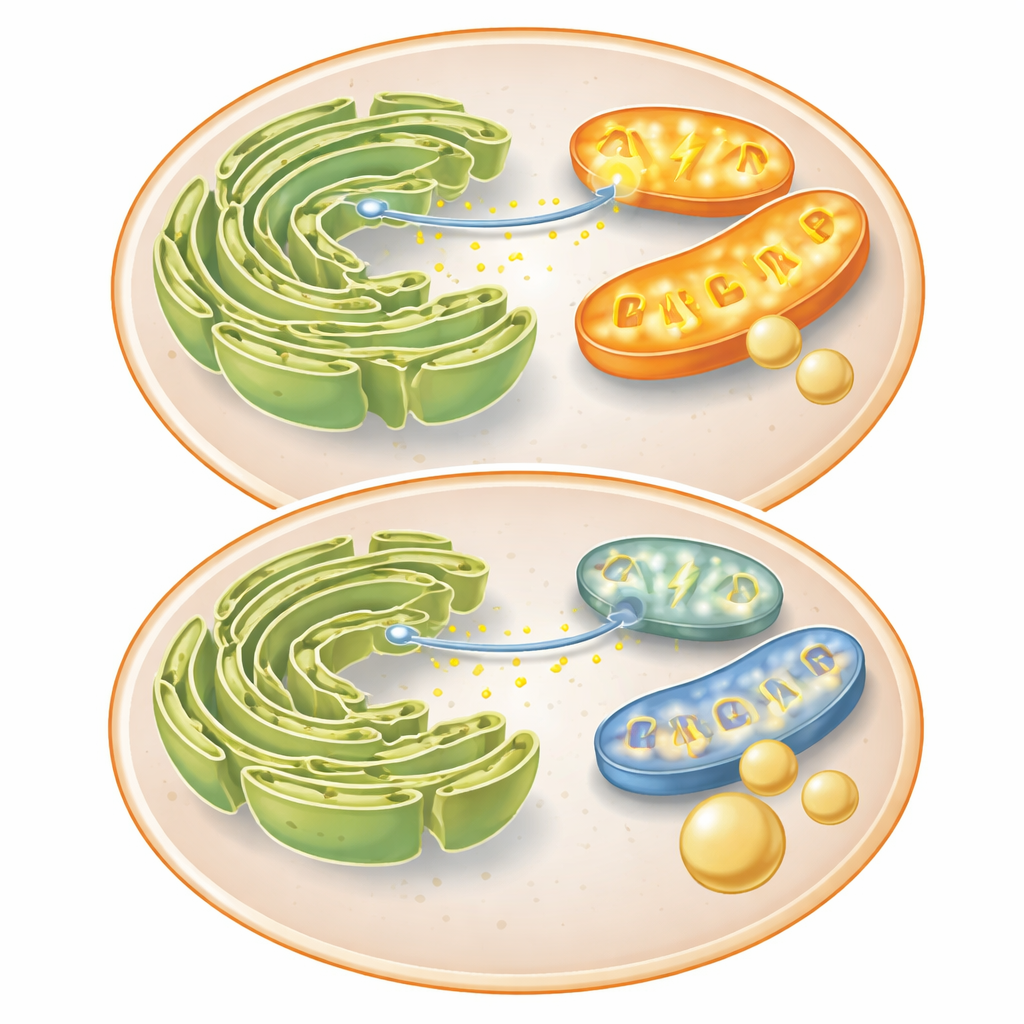
Zakłócona komunikacja między dwoma kluczowymi organellami
Aby zrozumieć, dlaczego mitochondria działały poniżej możliwości, zespół przeanalizował białka łączące je z inną strukturą — retikulum endoplazmatycznym (ER), gdzie magazynowany jest wapń. Poziom białka Mitofusin 2, ważnego zarówno dla fuzji mitochondriów, jak i dla bliskiego kontaktu z ER, spadł przy wysokim FKBP51. Te kontakty normalnie umożliwiają szybki transfer wapnia z ER do mitochondriów, co stymuluje enzymy produkujące energię. W komórkach kontrolnych sygnał chemiczny wywoływał silny wyrzut wapnia do mitochondriów; insulina i FKBP51 oba spowalniały ten transfer. FKBP51 także zmniejszał skoki wapnia w cytoplazmie, co sugeruje, że utrudnia uwalnianie wapnia z ER. Przy mniejszej ilości wapnia docierającej do mitochondriów ich wydajność energetyczna spada, co popycha komórkę w stronę oszczędniejszych procesów, takich jak ograniczona produkcja glukozy, i w kierunku magazynowania dostępnego cukru.
Co to znaczy dla zdrowia
Mówiąc wprost, badanie sugeruje, że FKBP51 działa jako obosieczny regulator stresowy w komórkach wątroby. Z jednej strony zaburza wczesne etapy sygnalizacji insuliny, co kojarzy się z insulinoopornością. Z drugiej strony osłabia maszynerię wytwarzającą energię przez zaburzenie wymiany wapnia między ER a mitochondriami. Efekt łączny to komórka wątroby, która wytwarza mniej nowej glukozy, ale jest bardziej skłonna magazynować dostępny cukier jako glikogen, nawet gdy klasyczne sygnały insulinowe są częściowo stłumione. Dla ludzi praca ta sugeruje, że przewlekły stres — poprzez białka takie jak FKBP51 — może subtelnie przeprogramowywać wykorzystanie energii w wątrobie i przyczyniać się do chorób metabolicznych. Ukierunkowanie FKBP51 lub połączenia wapniowego między ER a mitochondriami mogłoby w przyszłości zaoferować nowe strategie do regulacji poziomu cukru we krwi bez nadmiernego obciążania „elektrowni” komórkowych.
Cytowanie: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
Słowa kluczowe: oporność na insulinę, metabolizm wątroby, funkcja mitochondriów, stres komórkowy, sygnalizacja wapniowa