Clear Sky Science · it
FKBP51 altera la via di segnalazione dell’insulina e compromette la bioenergetica mitocondriale nelle cellule HepG2
Stress, zucchero e fegato
La vita moderna porta stress cronico, diete ricche e tassi in aumento di diabete di tipo 2. Questo studio esamina una proteina legata allo stress poco conosciuta, chiamata FKBP51, e come modifichi la risposta delle cellule epatiche all’insulina e l’uso dell’energia. Analizzando in dettaglio cellule umane derivate dal fegato coltivate in laboratorio, i ricercatori mostrano che FKBP51 può sia attenuare il segnale dell’insulina sia compromettere silenziosamente la produzione di energia all’interno delle centrali cellulari, i mitocondri. Capire questo tiro alla fune potrebbe aiutare a spiegare perché lo stress prolungato e le malattie metaboliche spesso vanno di pari passo.
Una proteina dello stress entra nel metabolismo
FKBP51 è nota soprattutto come proteina coadiuvante indotta dall’ormone dello stress, il cortisolo. Studi precedenti l’hanno collegata ad aumento di peso e resistenza all’insulina in muscolo, tessuto adiposo e cervello. Tuttavia, il suo ruolo nel fegato—un organo centrale nel controllo della glicemia—era poco chiaro. In questo studio, gli scienziati hanno usato cellule HepG2, un modello cellulare epatico umano molto diffuso, e hanno aumentato artificialmente i livelli di FKBP51 per osservare come ciò influisse sulla segnalazione dell’insulina e sul metabolismo del glucosio. Si sono concentrati su molecole chiave della via dell’insulina e su come i mitocondri generano energia, chiedendosi se FKBP51 potesse essere il anello mancante tra stress, disfunzione epatica e iperglicemia.
Segnale dell’insulina indebolito, ma aumenta lo stoccaggio degli zuccheri
Quando l’insulina si lega alle cellule epatiche, normalmente attiva una catena di proteine che riducono la glicemia promuovendo l’immagazzinamento del glucosio come glicogeno e riducendo la nuova produzione di glucosio. Il team ha confermato che un eccesso di FKBP51 indebolisce questa catena: riduce l’attivazione di Akt, un mediatore centrale dell’insulina, e di FOXO1, un regolatore dei geni che spingono il fegato a produrre nuovo glucosio. In teoria, questo avrebbe dovuto portare a un peggior controllo degli zuccheri. Sorprendentemente, in alcuni aspetti è successo il contrario. Le cellule ricche di FKBP51 producevano meno glucosio nuovo anche quando stimolate a farlo e, in presenza di insulina, immagazzinavano più glicogeno rispetto alle cellule di controllo. Questo suggerisce che FKBP51 confonde la logica abituale della via insulinica, attenuando alcuni segnali mentre ne potenzia altri tramite percorsi alternativi.
Le centrali energetiche sottoeseguono senza cambiare forma
Poiché la capacità del fegato di produrre o immagazzinare glucosio dipende molto dai mitocondri, i ricercatori hanno esaminato questi organelli in dettaglio. Hanno rilevato che circa la metà del segnale di FKBP51 all’interno delle cellule si localizza ai mitocondri, confermando un legame fisico. Tuttavia, al microscopio, dimensione e forma mitocondriale apparivano in gran parte normali, sia con alti livelli di FKBP51 sia dopo trattamento con insulina. Le modifiche erano invece funzionali. Sia la sovraespressione di FKBP51 sia il trattamento con insulina riducevano il consumo di ossigeno mitocondriale, abbassavano il potenziale di membrana elettrico e diminuivano l’ATP cellulare, la moneta chimica dell’energia. Importante, le cellule ricche di FKBP51 partivano da uno stato energetico già depresso e l’insulina abbassava ulteriormente i livelli di ATP, senza un aumento di specie reattive dell’ossigeno dannose.
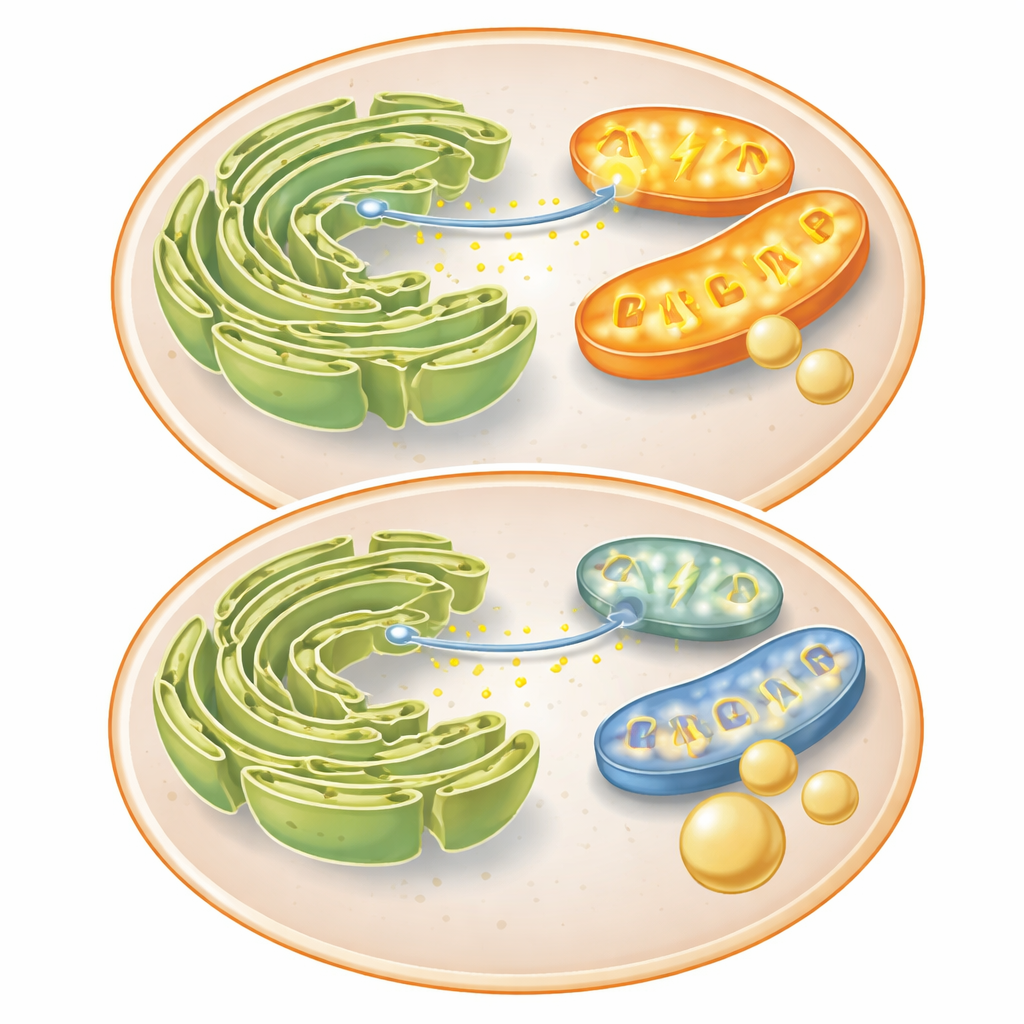
Conversazione interrotta tra due organelli chiave
Per capire perché i mitocondri funzionassero meno, il team ha esaminato proteine che li collegano a un’altra struttura, il reticolo endoplasmatico (RE), dove il calcio è immagazzinato. La proteina Mitofusina 2, importante sia per la fusione mitocondriale sia per i contatti stretti con il RE, diminuiva quando FKBP51 era elevata. Questi contatti normalmente permettono al calcio di passare rapidamente dal RE ai mitocondri, potenziando enzimi che producono energia. Nelle cellule di controllo, un segnale chimico provocava un forte picco di calcio nei mitocondri; insulina e FKBP51 rallentavano entrambi questo trasferimento. FKBP51 riduceva anche i picchi di calcio nel citosol, il che suggerisce che ostacola il rilascio di calcio dal RE. Con meno calcio che raggiunge i mitocondri, la loro produzione energetica cala, spingendo la cellula lontano da processi costosi come la gluconeogenesi e verso l’immagazzinamento del glucosio in arrivo.
Cosa significa per la salute
In parole semplici, lo studio suggerisce che FKBP51 agisce come un doppio effetto nelle cellule epatiche in risposta allo stress. Da un lato interferisce con i primi passaggi della segnalazione insulinica, una caratteristica associata alla resistenza all’insulina. Dall’altro indebolisce la macchina produttrice di energia disturbando lo scambio di calcio tra RE e mitocondri. L’effetto combinato è una cellula epatica che produce meno glucosio nuovo ma è più propensa a mettere da parte lo zucchero disponibile come glicogeno, anche quando i segnali classici dell’insulina sono parzialmente attenuati. Per le persone, questo lavoro suggerisce che lo stress cronico—attraverso proteine come FKBP51—può rimodellare l’uso energetico epatico in modi sottili che contribuiscono alle malattie metaboliche. Mirare a FKBP51 o alla connessione calcio RE‑mitocondri potrebbe un giorno offrire nuove strategie per modulare il controllo della glicemia senza sovraccaricare le centrali energetiche della cellula.
Citazione: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
Parole chiave: resistenza all’insulina, metabolismo epatico, funzione mitocondriale, stress cellulare, segnalazione del calcio