Clear Sky Science · nl
FKBP51 verstoort het insulinesignaleringspad en schaadt de mitochondriale bio-energetica in HepG2-cellen
Stress, suiker en de lever
Het moderne leven brengt chronische stress, rijke voeding en sterk stijgende aantallen type 2-diabetes met zich mee. Deze studie bekijkt een weinig bekend stressgerelateerd eiwit genaamd FKBP51 en hoe het de reactie van levercellen op insuline en hun energiegebruik verandert. Door in geisoleerde menselijke leverafgeleide cellen in het lab te kijken, tonen de onderzoekers aan dat FKBP51 zowel het insulinesignaal kan verzwakken als stilletjes de energieproductie in de energiecentrales van de cel, de mitochondriën, kan uitputten. Begrijpen hoe deze strijd verloopt kan helpen verklaren waarom langdurige stress en metabole ziekten zo vaak samen voorkomen.
Een stress-eiwit betreedt het metabolisme
FKBP51 is vooral bekend als een helper-eiwit dat wordt aangestuurd door het stresshormoon cortisol. Eerder werk bracht het in verband met gewichtstoename en insulineresistentie in spier, vet en hersenen. De rol ervan in de lever — een orgaan dat centraal staat in de regulatie van bloedglucose — was echter weinig onderzocht. In deze studie gebruikten wetenschappers HepG2-cellen, een veelgebruikt menselijk levercelmodel, en verhoogden ze kunstmatig de FKBP51-niveaus om te zien hoe dit insulinesignalering en suikerverwerking beïnvloedt. Ze richtten zich op sleutelmoleculen in het insulinepad en op hoe mitochondriën energie genereren, met de vraag of FKBP51 de ontbrekende schakel kan zijn tussen stress, leverdisfunctie en hoge bloedglucose.
Insulinesignaal verzwakt, maar suikervoorraad stijgt
Wanneer insuline zich bindt aan levercellen, activeert het normaal gesproken een keten van eiwitten die de bloedglucose verlaagt door opslag van suiker als glycogeen te bevorderen en de nieuwvorming van glucose te verminderen. Het team bevestigde dat extra FKBP51 deze keten verzwakt: het verminderde de activatie van Akt, een centraal insulineboodschapper, en van FOXO1, een regelaar van genen die de lever aanzet tot gluconeogenese. Op papier zou dit moeten leiden tot slechtere suikerregeling. Verrassend genoeg gebeurde in sommige opzichten het tegenovergestelde. Cellen met veel FKBP51 maakten minder nieuwe glucose, zelfs wanneer ze daartoe werden aangespoord, en in aanwezigheid van insuline slaagden ze er juist in om meer glycogeen op te slaan dan controlecellen. Dit suggereert dat FKBP51 de gebruikelijke logica van het insulinepad in de war stuurt, bepaalde signalen dempt maar andere via alternatieve routes versterkt.
Energiecentrales presteren ondermaats zonder van vorm te veranderen
Aangezien het vermogen van de lever om glucose te maken of op te slaan sterk afhankelijk is van mitochondriën, onderzochten de onderzoekers deze organellen in detail. Ze vonden dat ongeveer de helft van het FKBP51-signaal binnen cellen op de mitochondriën zit, wat een fysieke koppeling bevestigt. Toch zagen mitochondriën onder de microscoop grotendeels normale grootte en vorm, zelfs wanneer FKBP51 verhoogd was of insuline werd toegevoegd. De veranderingen waren functioneel. Zowel overexpressie van FKBP51 als insulinebehandeling verminderden het zuurstofverbruik door mitochondriën, verlaagden hun membraanpotentiaal en verlaagden de cellulaire ATP-voorraad, de chemische energievaluta. Belangrijk is dat cellen met veel FKBP51 al vanaf een verlaagde energiestatus begonnen, en insuline de ATP-niveaus nog verder naar beneden duwde, zonder een toename van schadelijke reactieve zuurstofspecies.
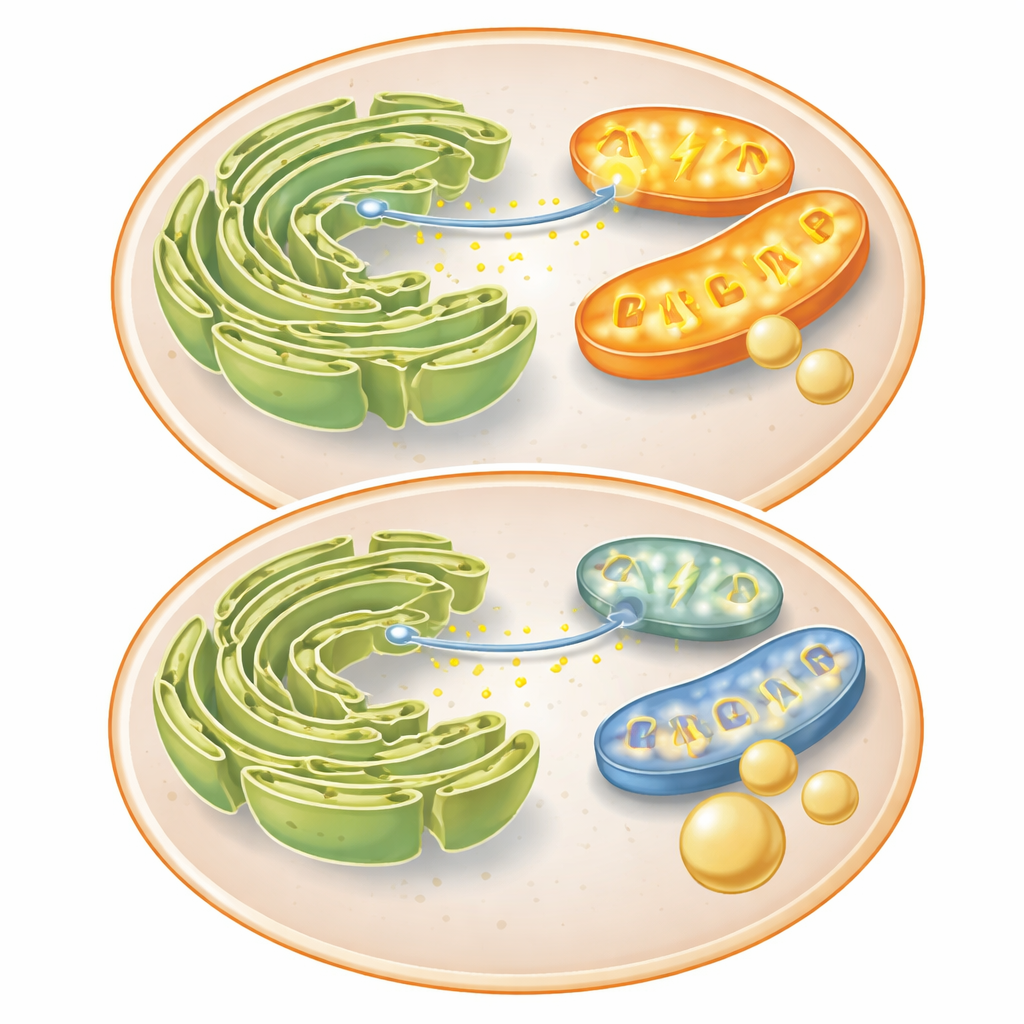
Verbroke communicatie tussen twee sleutelorganellen
Om te begrijpen waarom mitochondriën niet goed presteerden, keek het team naar eiwitten die ze verbinden met een andere structuur, het endoplasmatisch reticulum (ER), waar calcium wordt opgeslagen. Het eiwit Mitofusine 2, belangrijk voor zowel mitochondriale fusie als nauwe contacten met het ER, nam af wanneer FKBP51 hoog was. Deze contacten staan normaal toe dat calcium snel van het ER naar de mitochondriën stroomt, waardoor energieproducerende enzymen worden gestimuleerd. In controlecellen veroorzaakte een chemisch signaal een sterke calciumpiek in mitochondriën; zowel insuline als FKBP51 vertraagden deze overdracht. FKBP51 verminderde ook calciumpieken in het cytosol zelf, wat impliceert dat het de calciumvrijgave uit het ER belemmert. Met minder calcium dat mitochondriën bereikt, daalt hun energieproductie, waardoor de cel wordt aangestuurd weg van energie-intensieve processen zoals gluconeogenese en meer richting het opslaan van binnenkomende suiker.
Wat dit betekent voor de gezondheid
Simpel gezegd suggereert de studie dat FKBP51 in levercellen als een tweesnijdende stressreactor werkt. Enerzijds verstoort het vroege insulinesignalen, een kenmerk dat geassocieerd wordt met insulineresistentie. Anderzijds verzwakt het de energieproducerende machinerie door de calciumuitwisseling tussen ER en mitochondriën te verstoren. Het gecombineerde effect is een levercel die minder nieuwe glucose maakt maar eerder geneigd is beschikbare suiker als glycogeen op te slaan, zelfs wanneer klassieke insulinesignalen gedeeltelijk zijn gedempt. Voor mensen wijst dit werk erop dat chronische stress — via eiwitten als FKBP51 — het energiegebruik van de lever op subtiele manieren kan herschikken en zo kan bijdragen aan metabole ziektes. Het richten op FKBP51 of de ER-mitochondriale calciumverbinding zou op termijn nieuwe strategieën kunnen bieden om de bloedsuikerregeling bij te sturen zonder de energiecentrales van de cel te overbelasten.
Bronvermelding: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
Trefwoorden: insulineresistentie, levermetabolisme, mitochondriale functie, cellulaire stress, calciumsignalerings