Clear Sky Science · de
FKBP51 stört den Insulinsignalweg und beeinträchtigt die mitochondriale Bioenergetik in HepG2-Zellen
Stress, Zucker und die Leber
Das moderne Leben bringt chronischen Stress, kalorienreiche Ernährung und stark steigende Raten von Typ‑2‑Diabetes mit sich. Diese Studie untersucht ein wenig bekanntes, stressassoziiertes Protein namens FKBP51 und wie es verändert, wie Leberzellen auf Insulin reagieren und Energie nutzen. An humanen, leberabgeleiteten Zellen im Labor zeigen die Forschenden, dass FKBP51 sowohl die Insulin‑Signalübertragung abschwächen als auch die Energieproduktion in den Mitochondrien, den Kraftwerken der Zelle, beeinträchtigen kann. Dieses Tauziehen könnte erklären, warum langfristiger Stress und Stoffwechselkrankheiten so häufig zusammen auftreten.
Ein Stressprotein tritt in den Stoffwechsel ein
FKBP51 ist vor allem als ein Helferprotein bekannt, das durch das Stresshormon Cortisol hochreguliert wird. Frühere Arbeiten verbanden es mit Gewichtszunahme und Insulinresistenz in Muskel, Fettgewebe und Gehirn. Seine Rolle in der Leber — einem Organ, das zentral für die Blutzuckerregulation ist — war jedoch weniger gut verstanden. In dieser Studie verwendeten die Wissenschaftler HepG2‑Zellen, ein häufig genutztes Modell menschlicher Leberzellen, und erhöhten künstlich die FKBP51‑Spiegel, um zu untersuchen, wie dies Insulinsignale und den Zuckerstoffwechsel beeinflusst. Sie konzentrierten sich auf Schlüsselmoleküle des Insulinwegs und darauf, wie Mitochondrien Energie erzeugen, mit der Fragestellung, ob FKBP51 die fehlende Verbindung zwischen Stress, Leberdysfunktion und hohem Blutzucker sein könnte.
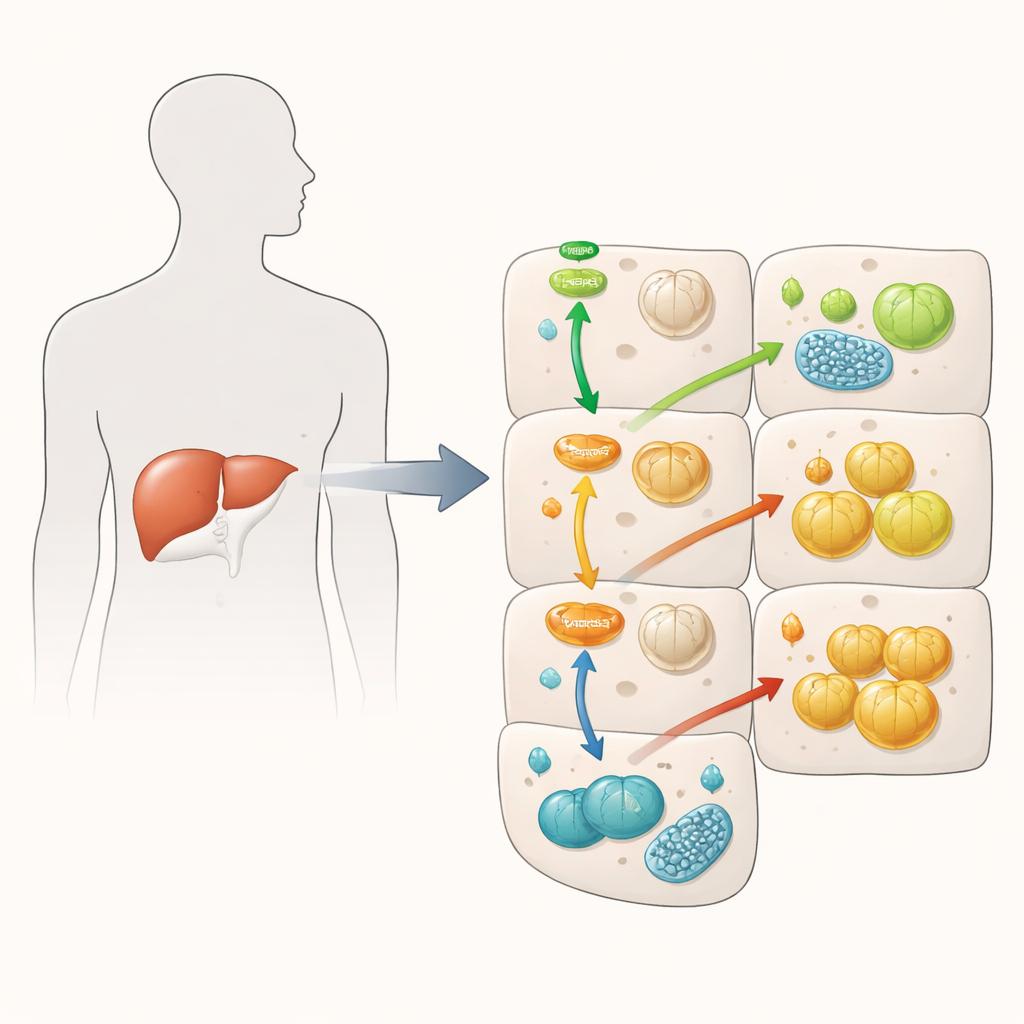
Insulinsignal abgeschwächt, dennoch steigt Glykogenspeicherung
Wenn Insulin an Leberzellen bindet, aktiviert es normalerweise eine Kaskade von Proteinen, die den Blutzucker senken, indem sie die Speicherung als Glykogen fördern und die Neubildung von Zucker reduzieren. Das Team bestätigte, dass ein Überschuss an FKBP51 diese Kaskade schwächt: Es verringerte die Aktivierung von Akt, einem zentralen Insulinboten, und von FOXO1, einem Regulator von Genen, die die Leber zur Glukoseproduktion treiben. Theoretisch sollte dies zu schlechterer Zuckerregulation führen. Überraschenderweise trat in mancher Hinsicht das Gegenteil ein. FKBP51‑reiche Zellen produzierten weniger neue Glukose, selbst wenn sie dazu angeregt wurden, und in Anwesenheit von Insulin speicherten sie sogar mehr Glykogen als Kontrollzellen. Das deutet darauf hin, dass FKBP51 die übliche Logik des Insulinwegs durcheinanderbringt, indem es einige Signale dämpft und andere über alternative Wege verstärkt.
Kraftwerke arbeiten schwächer, ohne ihre Form zu ändern
Da die Fähigkeit der Leber, Zucker herzustellen oder zu speichern, stark von Mitochondrien abhängt, untersuchten die Forschenden diese Organellen genauer. Sie fanden heraus, dass etwa die Hälfte des FKBP51‑Signals in den Zellen an Mitochondrien lokalisiert ist, was eine physische Verbindung bestätigt. Unter dem Mikroskop wirkten Größe und Form der Mitochondrien jedoch weitgehend normal, selbst bei hohem FKBP51 oder nach Insulinzugabe. Stattdessen zeigten sich funktionelle Veränderungen. Sowohl FKBP51‑Überexpression als auch Insulinbehandlung reduzierten die Sauerstoffverbrauchsrate der Mitochondrien, senkten ihr elektrisches Membranpotenzial und verringerten zelluläres ATP, die chemische Energiewährung. Wichtig ist: FKBP51‑reiche Zellen starteten bereits aus einem gedämpften energetischen Zustand, und Insulin drückte die ATP‑Werte noch weiter, ohne dass schädliche reaktive Sauerstoffspezies zunahmen.
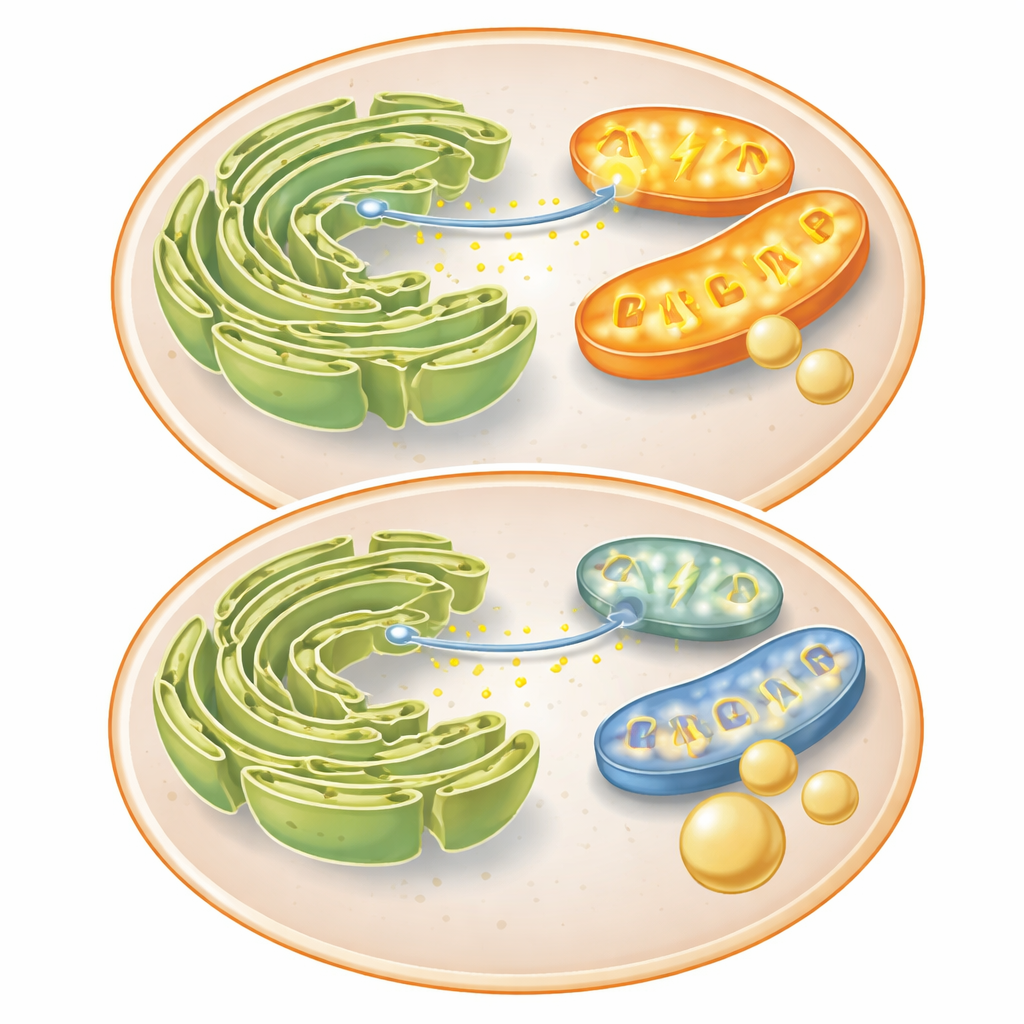
Gestörte Kommunikation zwischen zwei Schlüsselorganellen
Um zu verstehen, warum Mitochondrien leistungsschwach waren, untersuchte das Team Proteine, die sie mit einem anderen Kompartiment, dem endoplasmatischen Retikulum (ER), verbinden, in dem Calcium gespeichert wird. Das Protein Mitofusin 2, wichtig sowohl für mitochondriale Fusion als auch für enge Kontakte zum ER, war bei hohen FKBP51‑Spiegeln erniedrigt. Diese Kontakte ermöglichen normalerweise den schnellen Transfer von Calcium vom ER in die Mitochondrien und aktivieren so energieproduzierende Enzyme. In Kontrollzellen führte ein chemisches Signal zu einem starken Calcium‑Einstrom in die Mitochondrien; Insulin und FKBP51 verzögerten diesen Transfer. FKBP51 reduzierte auch Calcium‑Spitzen im Zellplasma, was darauf hindeutet, dass es die Calciumfreisetzung aus dem ER hemmt. Da weniger Calcium die Mitochondrien erreicht, sinkt deren Energieproduktion, wodurch die Zelle weg von energieintensiven Prozessen wie der Glukoneogenese und hin zur Speicherung eingehender Glukose gelenkt wird.
Was das für die Gesundheit bedeutet
Kurz gesagt legt die Studie nahe, dass FKBP51 in Leberzellen als zweischneidiger Stressantworter wirkt. Einerseits stört es frühe Insulinsignalschritte — ein Merkmal, das mit Insulinresistenz assoziiert ist. Andererseits schwächt es die Energieerzeugung, indem es den Calcium‑Austausch zwischen ER und Mitochondrien stört. Die kombinierte Wirkung ist eine Leberzelle, die weniger neue Glukose produziert, aber eher dazu neigt, verfügbaren Zucker als Glykogen einzulagern, selbst wenn klassische Insulinsignale teilweise abgeschwächt sind. Für Menschen deutet diese Arbeit darauf hin, dass chronischer Stress — vermittelt durch Proteine wie FKBP51 — die Leberenergieverwendung subtil umformen kann und so zu Stoffwechselerkrankungen beiträgt. Die gezielte Modulation von FKBP51 oder der ER‑Mitochondrien‑Calciumverbindung könnte eines Tages neue Strategien bieten, den Blutzucker zu regulieren, ohne die Kraftwerke der Zelle zu überlasten.
Zitation: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
Schlüsselwörter: Insulinresistenz, Leberstoffwechsel, mitochondriale Funktion, zellulärer Stress, Calcium-Signalübertragung