Clear Sky Science · he
FKBP51 מפריע למסלול איתות האינסולין ופוגע בביו-אנרגטיקה המיטוכונדריאלית בתאי HepG2
מתח, סוכר והכבד
החיים המודרניים מביאים מתח כרוני, תזונה עשירה ושיעורי סוכרת מסוג 2 שעולים. במחקר זה נבדק חלבון הקשור למתח, FKBP51, ואופן שבו הוא משנה את תגובת תאי הכבד לאינסולין ואת ניצול האנרגיה שלהם. בהסתכלות מעמיקה על תאי כבד ממקור אנושי בתנאי מעבדה, הממצאים מראים כי FKBP51 יכול גם להחליש את איתות האינסולין וגם להפחית בעדינות את ייצור האנרגיה במפעלי הכוח של התא — המיטוכונדריה. הבנת המאבק הזה עשויה לעזור להסביר מדוע מתח כרוני ומחלות מטבוליות נוטים להופיע יחד.
חלבון מתח נכנס למטבוליזם
FKBP51 ידוע בעיקר כחלבון מסייע המופעל על ידי הורמון המתח קורטיזול. עבודות קודמות קישרו אותו לעלייה במשקל ולעמידות לאינסולין בשריר, בשומן ובמוח. עם זאת, תפקידו בכבד — איבר מרכזי בשליטה על רמות הסוכר בדם — לא היה מובן היטב. במחקר זה השתמשו המדענים בתאי HepG2, מודל תאי כבד אנושי נפוץ, והגבירו באופן מלאכותי את רמות FKBP51 כדי לבדוק כיצד הדבר ישפיע על איתות האינסולין וטיפול בסוכרים. הם התמקדו במולקולות מפתח במסלול האינסולין ובאופן שבו המיטוכונדריות מייצרות אנרגיה, ובדקו האם FKBP51 יכול להיות הקשר החסר בין מתח, תפקוד בלתי תקין של הכבד ורמות סוכר גבוהות.
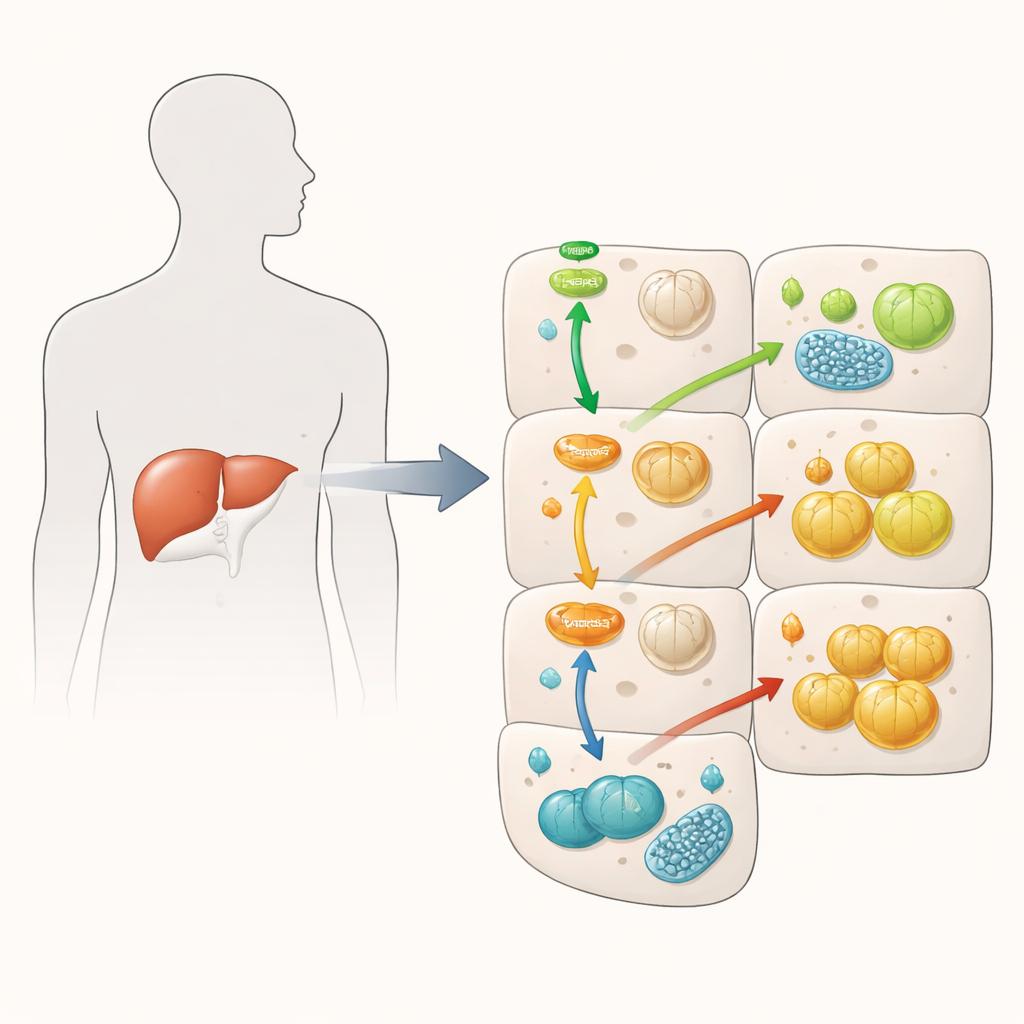
אות האינסולין מוחלש, אך אגירת סוכר עולה
כאשר אינסולין נקשר לתאי הכבד, זה בדרך כלל מפעיל שרשרת חלבונים שמורידה את רמת הסוכר בדם על ידי עידוד אגירת סוכר כגликוגן והפחתת יצירת סוכר חדש. החוקרים איששו כי עודף FKBP51 מחליש שרשרת זו: הוא הפחית את ההפעלה של Akt, שליח מרכזי של האינסולין, ושל FOXO1, רגולטור גנים המניע את הכבד ליצור גלוקוז חדש. על הנייר, זה היה אמור להוביל לשליטה לקויה בסוכר. באופן מפתיע, חלק מהתוצאות הראו את ההפך. תאים עשירים ב-FKBP51 ייצרו פחות גלוקוז חדש גם כאשר היו מאוששים לכך, וכאשר האינסולין היה נוכח — הם אגרו בפועל יותר גликוגן מתאי הבקרה. הממצא מרמז כי FKBP51 מבלבל את הלוגיקה הרגילה של מסלול האינסולין, מדכא אותות מסוימים בעוד שמגביר אחרים באמצעות מסלולים חלופיים.
מפעלי הכוח מפגרים בביצועים בלי לשנות צורה
מכיוון שיכולת הכבד לייצר או לאגור סוכר תלויה במידה רבה במיטוכונדריה, חקרו החוקרים את האורגנלות הללו בפירוט. הם מצאו שכחמישית עד חצי מסיגנל ה-FKBP51 בתוך התאים יושב על המיטוכונדריה, מה שמאמת קשר פיזי. עם זאת, תחת המיקרוסקופ, גודל וצורת המיטוכונדריה נראו ברובם תקינים, גם כאשר FKBP51 היה גבוה או כאשר הוסיפו אינסולין. השינויים היו תפקודיים במקום זאת. גם ביטוי יתר של FKBP51 וגם טיפול באינסולין הורידו את צריכת החמצן המיטוכונדריאלית, הפחיתו את פוטנציאל הממברנה החשמלי והקטינו את רמות ה-ATP התאית, מטבע האנרגיה הכימי. משמעותי שנקודת ההתחלה של תאים עשירים ב-FKBP51 הייתה מצב אנרגטי מדוכא כבר מלכתחילה, והאינסולין הוריד עוד יותר את רמות ה-ATP, ללא עלייה ברדיקלים חופשיים מזיקים של חמצן.
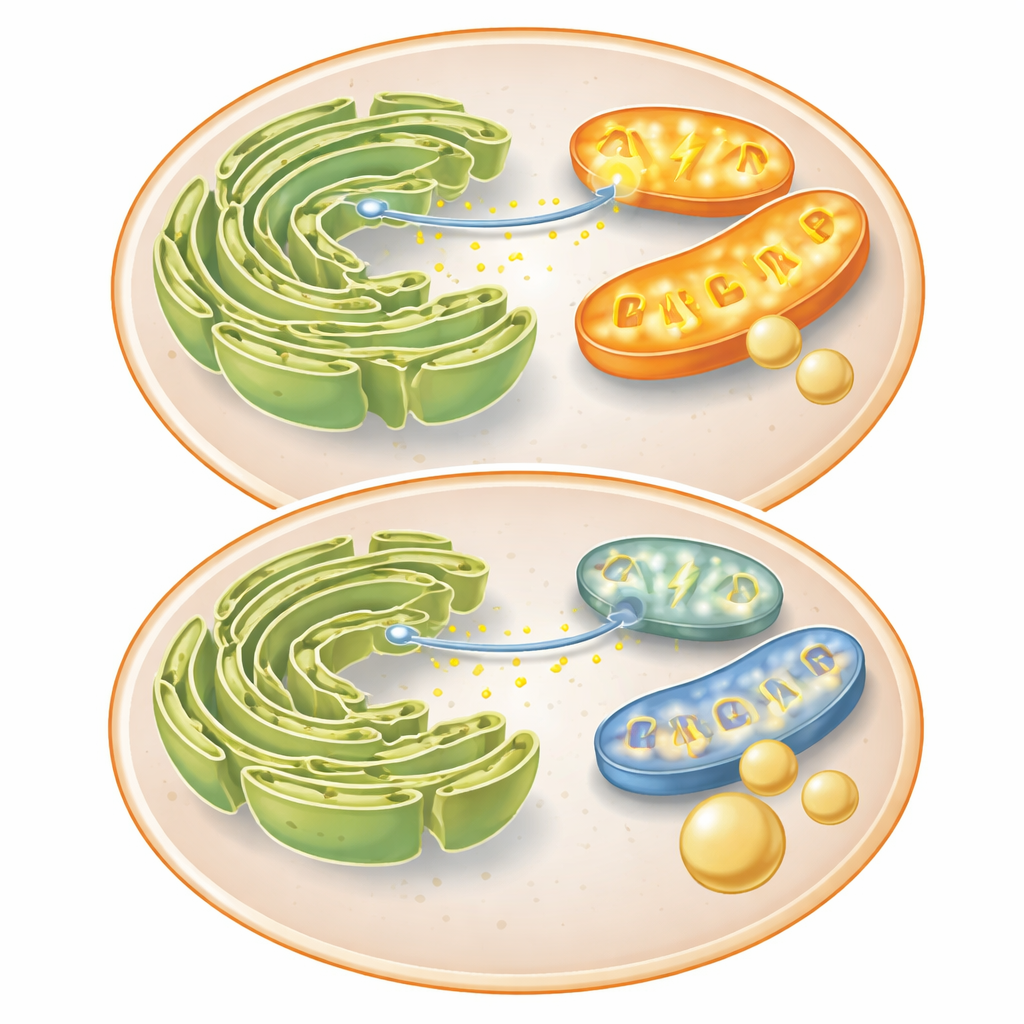
שיחה שבורה בין שתי אורגנלות מרכזיות
כדי להבין מדוע המיטוכונדריה היו חלשות, בדקו החוקרים חלבונים שמקשרים אותן למבנה אחר — הרשתית האנדופלסמטית (ER), שם מאוחסן הסידן. חלבון Mitofusin 2, החשוב גם למיזוג מיטוכונדריאלי וגם למגע הדוק עם ה-ER, פחת כאשר FKBP51 היה גבוה. המגעים הללו בדרך כלל מאפשרים לסידן לזרום במהירות מה-ER אל המיטוכונדריה, מה שמפעיל אנזימים שמייצרים אנרגיה. בתאי בקרה, אות כימי גרם לפרץ חזק של סידן לתוך המיטוכונדריה; אינסולין ו-FKBP51 שניהם האטו את ההעברה הזו. FKBP51 גם הפחית את קפיצות הסידן בנוזל התא עצמו, מה שמרמז שהוא מעכב את שחרור הסידן מה-ER. עם פחות סידן שמגיע אל המיטוכונדריה, תפוקת האנרגיה שלהן יורדת, מה שדוחף את התא להתרחק מתהליכים יקרים באנרגיה כמו יצירת גלוקוז חדש ולהעדיף במקום זאת לאגור סוכר נכנס.
מה המשמעות הבריאותית של זה
באופן פשוט, המחקר מציע כי FKBP51 פועל כגורם מתח דו-חרבי בתאי כבד. מצד אחד, הוא מתערב בשלבי האיתות המוקדמים של האינסולין — תכונה המקושרת לעמידות לאינסולין. מצד שני, הוא מחליש את מכונת ייצור האנרגיה על ידי פגיעה בהחלפת הסידן בין ה-ER למיטוכונדריה. האפקט המשולב הוא תא כבד שמייצר פחות גלוקוז חדש אך נוטה יותר לאגור סוכר זמין כגلیکוגן, אפילו כאשר אותות האינסולין הקלאסיים מעוכים חלקית. עבור בני אדם, העבודה מצביעה על כך שמתח כרוני — דרך חלבונים כמו FKBP51 — עשוי לעצב מחדש את שימוש האנרגיה בכבד בדרכים עדינות התורמות למחלת מטבוליזם. כיוונון של FKBP51 או של חיבור הסידן בין ה-ER למיטוכונדריה עשוי יום אחד להציע אסטרטגיות חדשות לכוונון רמת הסוכר בדם בלי לנדוש את מפעלי הכוח של התא.
ציטוט: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
מילות מפתח: עמידות לאינסולין, מטבוליזם כבד, תפקוד מיטוכונדריה, מתח תאי, איתות סידן