Clear Sky Science · fr
FKBP51 perturbe la voie de signalisation de l’insuline et altère la bioénergétique mitochondriale dans les cellules HepG2
Stress, sucre et foie
La vie moderne apporte un stress chronique, des régimes riches et une hausse spectaculaire du diabète de type 2. Cette étude examine une protéine liée au stress, peu connue, nommée FKBP51, et la manière dont elle modifie la réponse des cellules hépatiques à l’insuline et leur utilisation de l’énergie. En se concentrant sur des cellules dérivées du foie humain en culture, les chercheurs montrent que FKBP51 peut à la fois affaiblir le signal de l’insuline et réduire silencieusement la production d’énergie au sein des centrales cellulaires, les mitochondries. Comprendre cette lutte interne peut aider à expliquer pourquoi le stress chronique et les maladies métaboliques vont si souvent de pair.
Une protéine du stress entre dans le métabolisme
FKBP51 est surtout connue comme une protéine d’assistance activée par l’hormone du stress, le cortisol. Des travaux antérieurs l’avaient liée à la prise de poids et à la résistance à l’insuline dans le muscle, le tissu adipeux et le cerveau. Son rôle dans le foie — organe central du contrôle de la glycémie — était cependant mal compris. Dans cette étude, les scientifiques ont utilisé des cellules HepG2, un modèle hépatique humain largement employé, et ont artificiellement augmenté les niveaux de FKBP51 pour voir comment cela affecterait la signalisation de l’insuline et le métabolisme du glucose. Ils se sont focalisés sur des molécules clés de la voie de l’insuline et sur la manière dont les mitochondries produisent de l’énergie, pour déterminer si FKBP51 pourrait être un lien manquant entre le stress, la dysfonction hépatique et l’hyperglycémie.
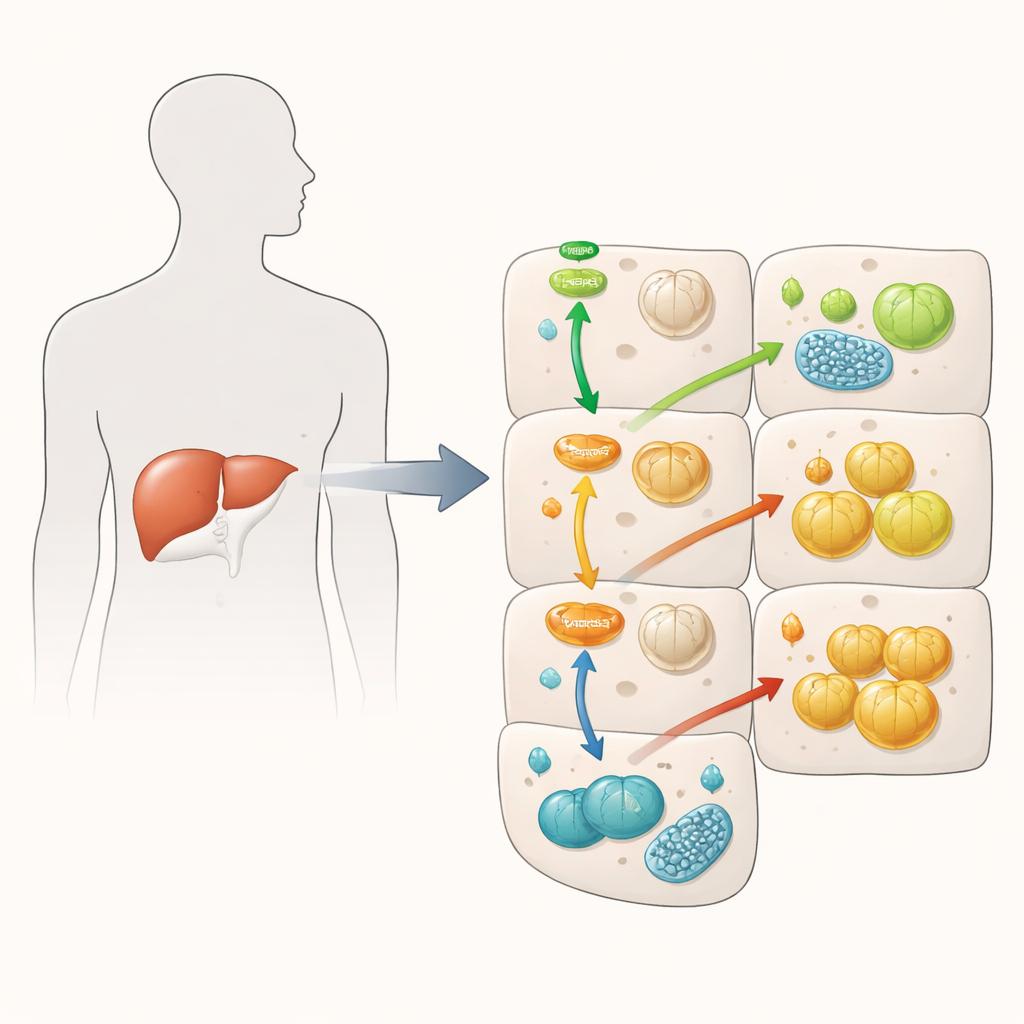
Signal de l’insuline affaibli, mais augmentation du stockage du sucre
Quand l’insuline se lie aux cellules hépatiques, elle active normalement une cascade de protéines qui abaissent la glycémie en favorisant le stockage du glucose sous forme de glycogène et en réduisant la néoglucogenèse. L’équipe a confirmé que un excès de FKBP51 affaiblit cette cascade : il réduit l’activation d’Akt, un messager central de l’insuline, et de FOXO1, un régulateur de gènes responsables de la production de nouveau glucose par le foie. Sur le papier, cela aurait dû entraîner un contrôle glycémique moins bon. De façon surprenante, l’inverse est survenu à certains égards. Les cellules riches en FKBP51 produisaient moins de glucose de novo même lorsqu’on les stimulait, et en présence d’insuline, elles stockaient en fait plus de glycogène que les cellules témoins. Cela suggère que FKBP51 brouille la logique habituelle de la voie de l’insuline, atténuant certains signaux tout en en renforçant d’autres via des voies alternatives.
Des centrales énergétiques moins performantes sans modification visible de la structure
Puisque la capacité du foie à produire ou stocker du glucose dépend fortement des mitochondries, les chercheurs ont ensuite examiné ces organites en détail. Ils ont constaté qu’environ la moitié du signal FKBP51 dans les cellules se trouvait au niveau des mitochondries, confirmant un lien physique. Pourtant, au microscope, la taille et la morphologie mitochondriales semblaient largement normales, même lorsque FKBP51 était élevé ou que l’insuline était ajoutée. Ce sont plutôt les fonctions qui changeaient. Tant la surexpression de FKBP51 que le traitement par l’insuline réduisaient la consommation d’oxygène mitochondriale, abaissaient le potentiel de membrane électrique et diminuaient l’ATP cellulaire, la monnaie chimique de l’énergie. De manière importante, les cellules riches en FKBP51 démarraient d’un état énergétique déjà déprimé, et l’insuline abaissait encore davantage les niveaux d’ATP, sans augmentation des espèces réactives de l’oxygène nuisibles.
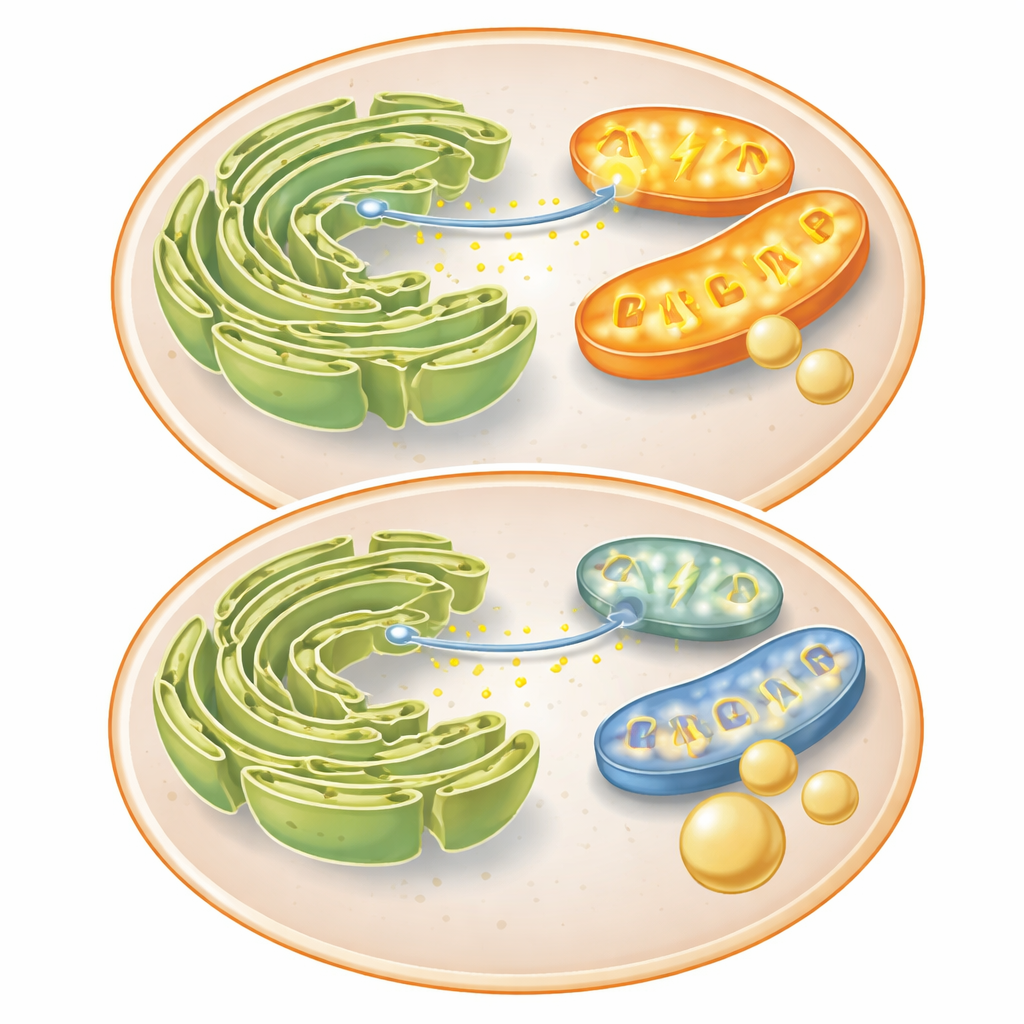
Conversation rompue entre deux organites clés
Pour comprendre pourquoi les mitochondries étaient moins performantes, l’équipe a examiné des protéines qui les relient à une autre structure, le réticulum endoplasmique (RE), où le calcium est stocké. La protéine Mitofusine 2, importante à la fois pour la fusion mitochondriale et pour des contacts étroits avec le RE, diminuait lorsque FKBP51 était élevé. Ces contacts permettent normalement au calcium de passer rapidement du RE vers les mitochondries, stimulant des enzymes productrices d’énergie. Dans les cellules témoins, un signal chimique induisait un fort afflux de calcium dans les mitochondries ; l’insuline et FKBP51 ralentissaient tous deux ce transfert. FKBP51 réduisait également les pics calciques dans le cytosol, ce qui suggère qu’il entrave la libération du calcium depuis le RE. Avec moins de calcium atteignant les mitochondries, leur rendement énergétique diminue, poussant la cellule à renoncer à des processus coûteux comme la néoglucogenèse et à favoriser le stockage du glucose entrant sous forme de glycogène.
Ce que cela signifie pour la santé
En termes simples, l’étude suggère que FKBP51 agit comme un répondeur au stress à double tranchant dans les cellules hépatiques. D’une part, il interfère avec les étapes initiales de la signalisation de l’insuline, caractéristique associée à la résistance à l’insuline. D’autre part, il affaiblit la machinerie de production d’énergie en perturbant l’échange calcique entre le RE et les mitochondries. L’effet combiné est une cellule hépatique qui produit moins de glucose de novo mais est plus encline à stocker le glucose disponible sous forme de glycogène, même lorsque les signaux classiques de l’insuline sont partiellement atténués. Pour l’humain, ces travaux suggèrent que le stress chronique — via des protéines comme FKBP51 — peut remodeler subtilement l’utilisation énergétique hépatique et contribuer aux maladies métaboliques. Cibler FKBP51 ou la connexion calcique RE‑mitochondrie pourrait un jour offrir de nouvelles stratégies pour ajuster le contrôle de la glycémie sans surmener les centrales énergétiques de la cellule.
Citation: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
Mots-clés: résistance à l’insuline, métabolisme hépatique, fonction mitochondriale, stress cellulaire, signalisation calcique