Clear Sky Science · sv
FKBP51 stör insulinsignalering och försämrar mitokondriell bioenergetik i HepG2‑celler
Stress, socker och levern
Det moderna livet medför kronisk stress, kaloririka dieter och en kraftig ökning av typ 2‑diabetes. Denna studie undersöker ett lite känt stressrelaterat protein, FKBP51, och hur det förändrar levercellers respons på insulin och deras energianvändning. Genom att zooma in på människoderiverade leverceller i laboratoriet visar forskarna att FKBP51 både kan dämpa insulinsignalering och tyst urholka energiproduktionen i cellens kraftverk, mitokondrierna. Att förstå denna dragkamp kan hjälpa förklara varför långvarig stress och metabola sjukdomar så ofta går hand i hand.
Ett stressprotein tar plats i metabolismen
FKBP51 är mest känt som ett hjälpprotein som aktiveras av stresshormonet kortisol. Tidigare arbete har kopplat det till viktuppgång och insulinresistens i muskel, fett och hjärna. Dess roll i levern — ett organ centralt för blodsockerreglering — var dock mindre klarlagd. I denna studie använde forskarna HepG2‑celler, en välanvänd modell för mänskliga leverceller, och ökade artificiellt nivåerna av FKBP51 för att se hur det påverkar insulinsignalering och sockerhantering. De fokuserade på nyckelmolekyler i insulinsignalen och på hur mitokondrier genererar energi, med frågan om FKBP51 kan vara en saknad länk mellan stress, leverdysfunktion och förhöjt blodsocker.
Insulinsignalen försvagas, men sockerlager ökar
När insulin binder till leverceller aktiverar det normalt en kedja av proteiner som sänker blodsockret genom att främja lagring som glykogen och minska nybildning av glukos. Teamet bekräftade att extra FKBP51 försvagar denna kedja: det minskade aktiveringen av Akt, en central insulinbudbärare, och av FOXO1, en regulator för gener som driver levern att tillverka ny glukos. På pappret borde detta leda till sämre sockerkontroll. Överraskande nog skedde i vissa avseenden motsatsen. FKBP51‑rika celler bildade mindre nysyntetiserad glukos även när de stimulerades att göra det, och i närvaro av insulin lagrade de faktiskt mer glykogen än kontrollceller. Detta tyder på att FKBP51 rör till den vanliga logiken i insulinsignalen, genom att dämpa vissa signaler samtidigt som andra förstärks via alternativa vägar.
Kraftverken presterar sämre utan att ändra form
Där leverns förmåga att göra eller lagra socker till stor del beror på mitokondrierna, undersökte forskarna dessa organeller i detalj. De fann att ungefär hälften av FKBP51‑signalen i cellerna lokaliserar till mitokondrierna, vilket bekräftar en fysisk koppling. Ändå såg mitokondriernas storlek och form i stort sett normala ut i mikroskopet, även när FKBP51 var hög eller insulin tillsattes. Istället var förändringarna funktionella. Både överuttryck av FKBP51 och insulinbehandling minskade mitokondriernas syreförbrukning, sänkte deras elektriska membranpotential och reducerade cellernas ATP, energins kemiska valuta. Viktigt är att FKBP51‑rika celler redan utgick från ett nedtryckt energitillstånd, och insulin pressade ATP‑nivåerna ännu lägre, utan någon ökning av skadliga reaktiva syreradikaler.
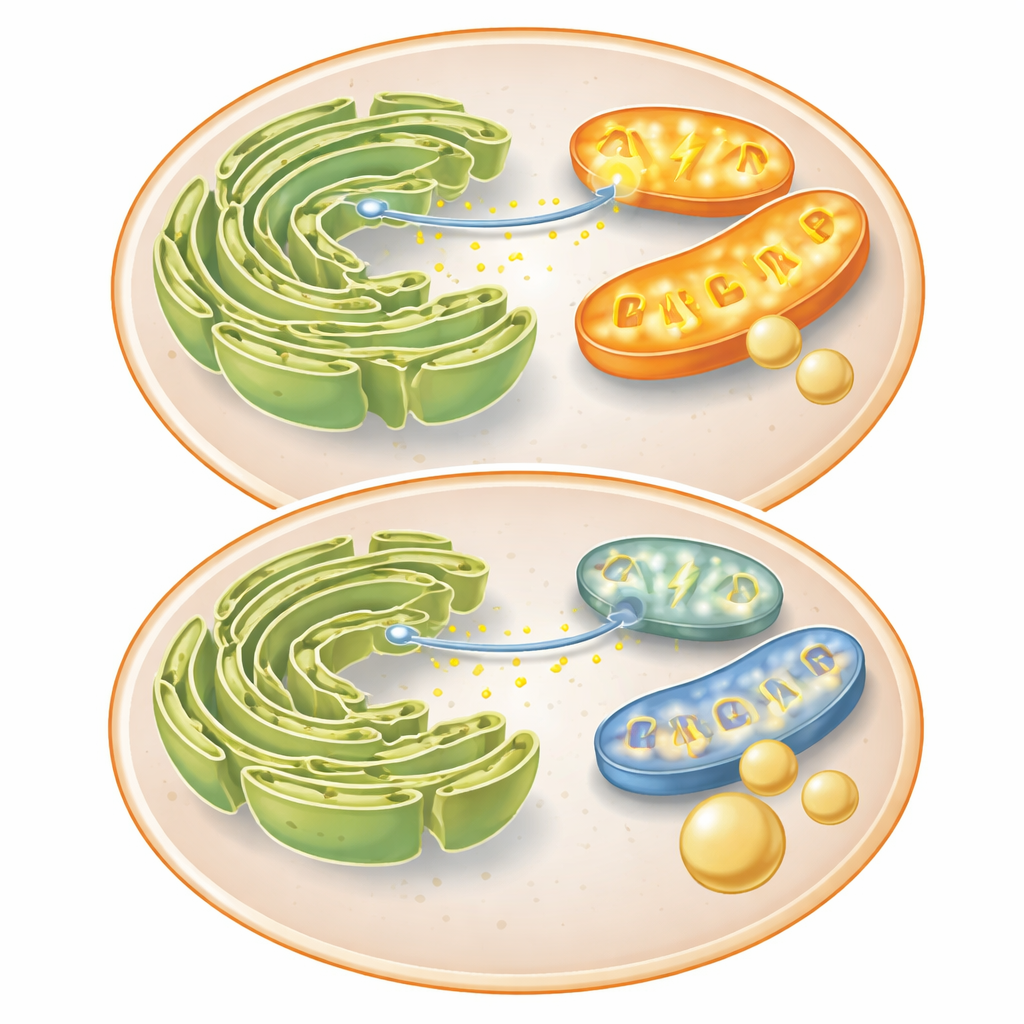
Bruten kommunikation mellan två nyckelorganeller
För att förstå varför mitokondrierna underpresterade tittade teamet på proteiner som kopplar dem till en annan struktur, endoplasmatiska retiklet (ER), där kalcium lagras. Proteinet Mitofusin 2, viktigt både för mitokondriell fusion och för täta kontakter med ER, minskade när FKBP51 var hög. Dessa kontakter tillåter normalt kalcium att snabbt röra sig från ER in i mitokondrierna och därigenom stimulera energiproducerande enzymer. I kontrollceller orsakade en kemisk signal ett starkt utflöde av kalcium in i mitokondrierna; insulin och FKBP51 dämpade båda denna överföring. FKBP51 minskade också kalciumspikar i cytosolen, vilket antyder att det hämmar kalciumfrigörelse från ER. Med mindre kalcium som når mitokondrierna faller deras energiproduktion, vilket leder cellen bort från energikrävande processer som glukoneogenes och mot att lagra inkommande socker istället.
Vad detta betyder för hälsan
Enkelt uttryckt föreslår studien att FKBP51 fungerar som en tvåeggad stressresponder i leverceller. Å ena sidan stör det insulins tidiga signalsteg, en egenskap kopplad till insulinresistens. Å andra sidan försvagar det maskineriet för energiproduktion genom att rubba kalciumutbytet mellan ER och mitokondrier. Den samlade effekten är en levercell som bildar mindre ny glukos men som i högre grad tenderar att lagra tillgängligt socker som glykogen, även när de klassiska insulinsignalerna delvis är dämpade. För människors del antyder arbetet att kronisk stress — via proteiner som FKBP51 — kan omforma leverns energianvändning på subtila sätt som bidrar till metabola sjukdomar. Att rikta in sig på FKBP51 eller ER‑mitokondriellt kalciumutbyte kan en dag erbjuda nya strategier för att finjustera blodsockerreglering utan att överbelasta cellernas kraftverk.
Citering: Donoso-Barraza, C., Díaz-Roblero, M., Sepúlveda, C. et al. FKBP51 disrupts the insulin signaling pathway and impairs mitochondrial bioenergetics in HepG2 cells. Sci Rep 16, 9896 (2026). https://doi.org/10.1038/s41598-026-40414-9
Nyckelord: insulinresistens, levermetabolism, mitokondriell funktion, cellstress, kalciumsignalering