Clear Sky Science · zh
GPR109a-AMPK轴介导Lacticaseibacillus rhamnosus M2b来源的β-羟基丁酸减轻尿酸诱导的M1巨噬细胞极化
为何肠道微生物与关节疼痛有关
血中尿酸偏高的人常会出现痛风及其他炎性问题,但目前的治疗大多侧重于降低尿酸,而不是平抑被尿酸激活的免疫系统。本研究探讨了一种有益的肠道细菌及其小分子产物,如何温和地将免疫细胞从有害的攻击状态引导到有助修复的抚慰状态,为缓解高尿酸相关炎症提供了新的视角。
从高尿酸到愤怒的免疫细胞
高尿酸血症在全球越来越常见,且不仅与痛风相关,还与更广泛的慢性炎症有关。尿酸能将某些白细胞——巨噬细胞——推向一种侵袭性状态,分泌大量炎性物质,损伤周围组织。研究人员已知这种常称为M1型的侵袭性状态在疾病中起着核心作用,但能够直接且安全地将这些细胞重新引导至更平静、修复型状态的治疗手段仍然有限。
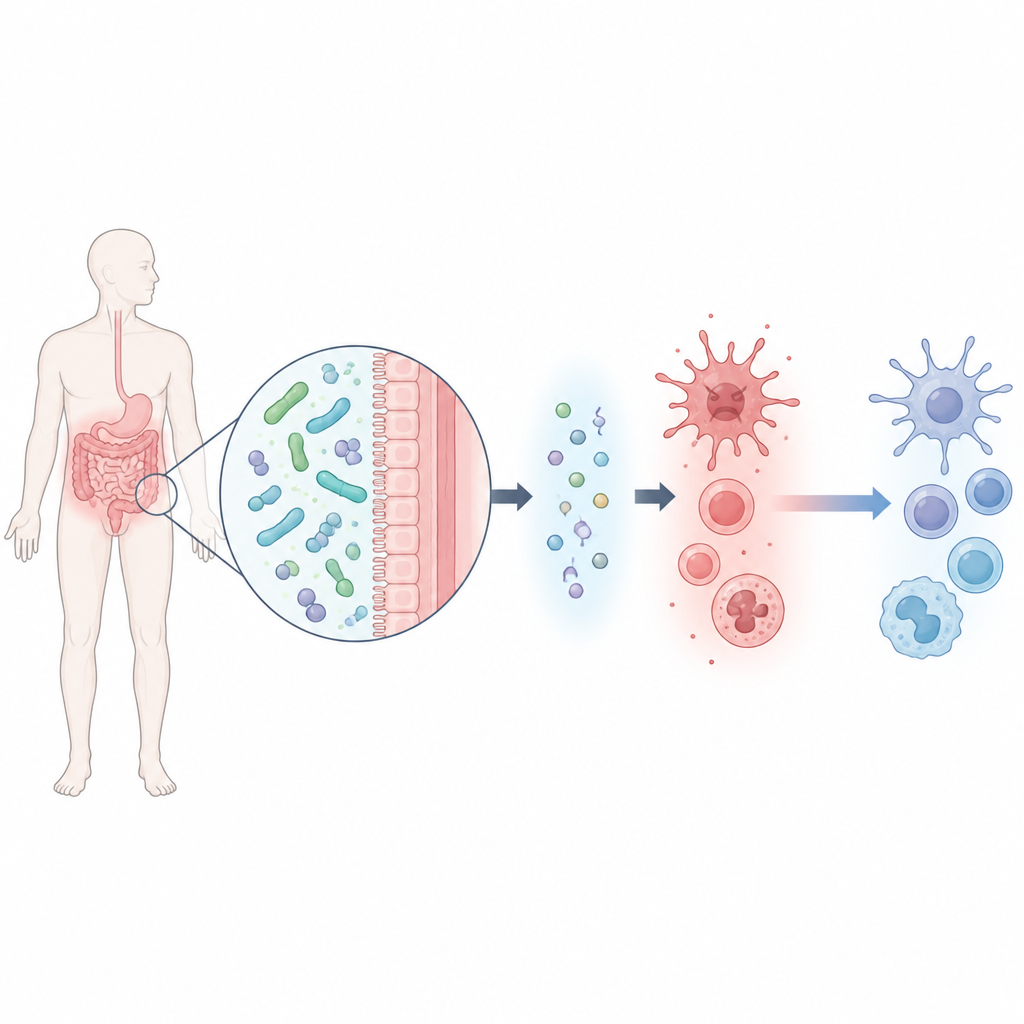
一种有益的肠道微生物及其小分子信号
研究团队首先从尿酸水平较低的健康男性粪便中分离出一株Lacticaseibacillus rhamnosus,命名为M2b。该菌株在体外表现出优异的降解尿酸能力。通过对该微生物释放的代谢产物进行广泛筛查,科学家鉴定出六种候选分子,并测试了它们能否保护受尿酸胁迫的小鼠巨噬细胞。其中一种分子β-羟基丁酸脱颖而出:它不仅改善了细胞存活,还显著降低了若干关键炎性因子,同时增强了一种名为IL-10的抗炎信号。
将攻击型细胞转为修复型细胞
为了解该小分子如何重塑免疫行为,研究人员将巨噬细胞暴露于单独的尿酸或与β-羟基丁酸或M2b菌液共同作用下。单独的尿酸使细胞呈现典型的攻击姿态,M1相关标志物升高,而与更抚慰、类似M2的状态相关的标志物降低。加入β-羟基丁酸或菌液后,这些模式发生逆转:攻击标志下降,修复标志上升,细胞在显微镜下的形态也转向更平静的外观。这表明肠道细菌产生的代谢物能够直接将免疫细胞从有害反应倾斜开来。
受体开关与细胞内的能量感应器
研究并未止步于观察这些变化;科学家还想弄清其发生机制。他们将注意力集中在巨噬细胞表面的一种蛋白GPR109a上,该受体可感知类似β-羟基丁酸的分子。计算机建模建议β-羟基丁酸能够紧密结合该受体。实验确认尿酸会降低GPR109a的表达,而β-羟基丁酸和M2b菌液能恢复其水平。当研究者刻意降低细胞中的GPR109a时,β-羟基丁酸的抑炎效果消失;相反,提升GPR109a时,即便在尿酸胁迫下,细胞也自发向修复型转变。
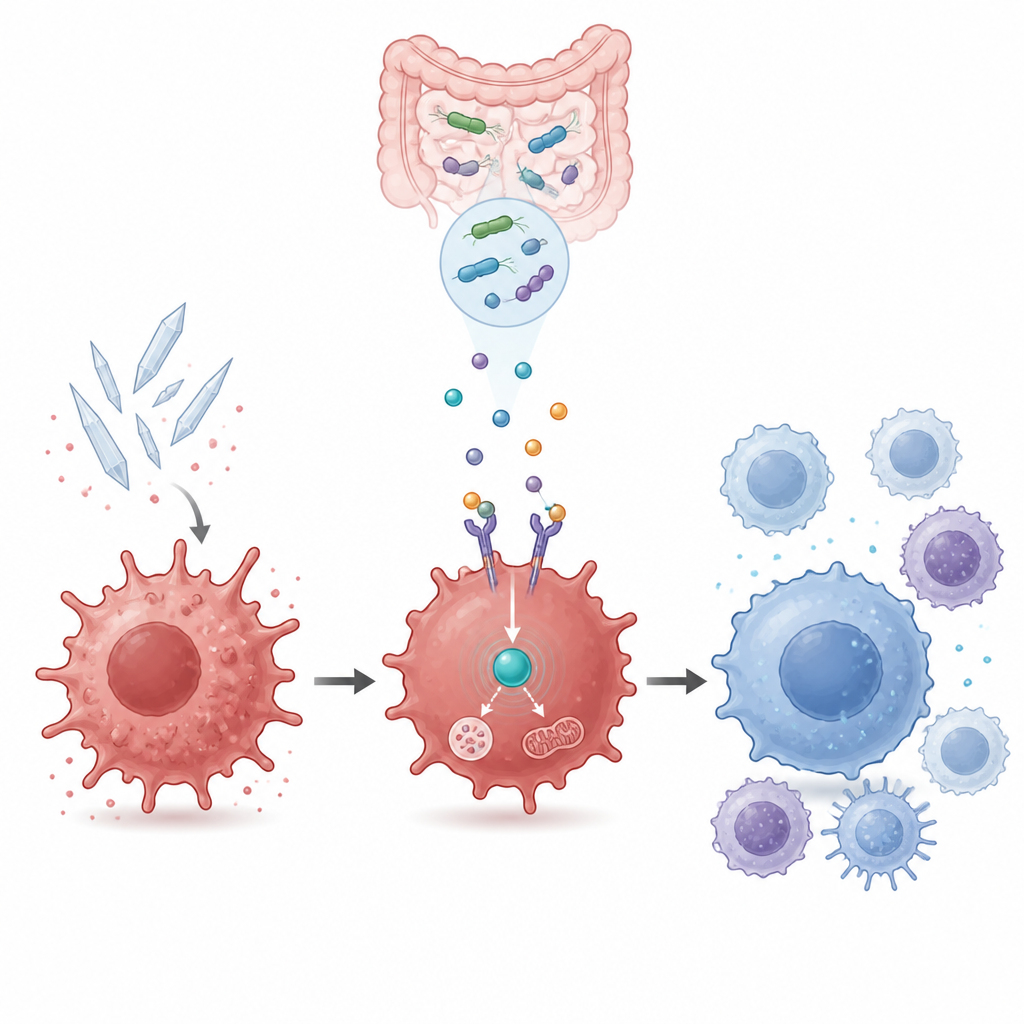
将细胞能量利用与炎症控制联系起来
在细胞内部,GPR109a与另一个关键分子AMPK相连,后者是细胞能量状态的传感器。基因表达和蛋白检测显示,尿酸抑制了AMPK活性,而β-羟基丁酸则在依赖GPR109a的情况下恢复了AMPK活性。用化学抑制剂阻断AMPK会抹去β-羟基丁酸及M2b菌液的益处:炎性标志再次升高,修复标志消退。这将免疫的平抑转变与一个必须保持活性的细胞内能量感应回路联系起来,表明该细胞内通路对细菌代谢物发挥作用至关重要。
这对高尿酸患者意味着什么
综合来看,研究描绘了一条简明的事件链:肠道细菌产生β-羟基丁酸,这种小分子激活免疫细胞表面的GPR109a受体,进而启动AMPK,帮助巨噬细胞从有害的攻击模式转向更平和的修复导向模式。尽管这些工作是在培养的小鼠细胞中完成,尚需在动物和人群中进一步验证,但研究指出,肠道微生物代谢物通过GPR109a-AMPK通路可能成为缓解高尿酸相关炎症的有前景靶点,或可与常规降尿酸药物互为补充,提供更精确的免疫抚慰策略。
引用: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
关键词: 高尿酸血症, 肠道微生物群, 巨噬细胞极化, β-羟基丁酸, GPR109a AMPK通路