Clear Sky Science · ja
GPR109a-AMPK軸はLacticaseibacillus rhamnosus M2b由来のβ-ヒドロキシ酪酸による尿酸誘発M1マクロファージ分極の緩和を媒介する
関節痛において腸内細菌が重要な理由
血中の尿酸が高い人は痛風やその他の炎症性疾患を発症しやすいが、現在の治療は主に尿酸値を下げることに焦点を当てており、尿酸が刺激する免疫系をいかに鎮めるかには十分に対処していない。本研究は、有益な腸内細菌とその小さな化学産物が、免疫細胞を有害な攻撃モードから穏やかな修復モードへとそっと誘導しうることを探り、高尿酸に関連する炎症の緩和に新しい視点を提示する。
高尿酸から活性化した免疫細胞へ
高尿酸血症は世界的に増加しており、痛風だけでなく慢性的な炎症とも関連している。尿酸はマクロファージと呼ばれる白血球の一部を攻撃的な状態へと押しやり、炎症性物質を大量に放出して周囲組織を傷つけることがある。この攻撃的な状態はしばしばM1型と呼ばれ、疾患の中心的な役割を果たすことが知られているが、これらの細胞を直接かつ安全に落ち着かせ、修復寄りの状態へと導く治療法はまだ限られている。
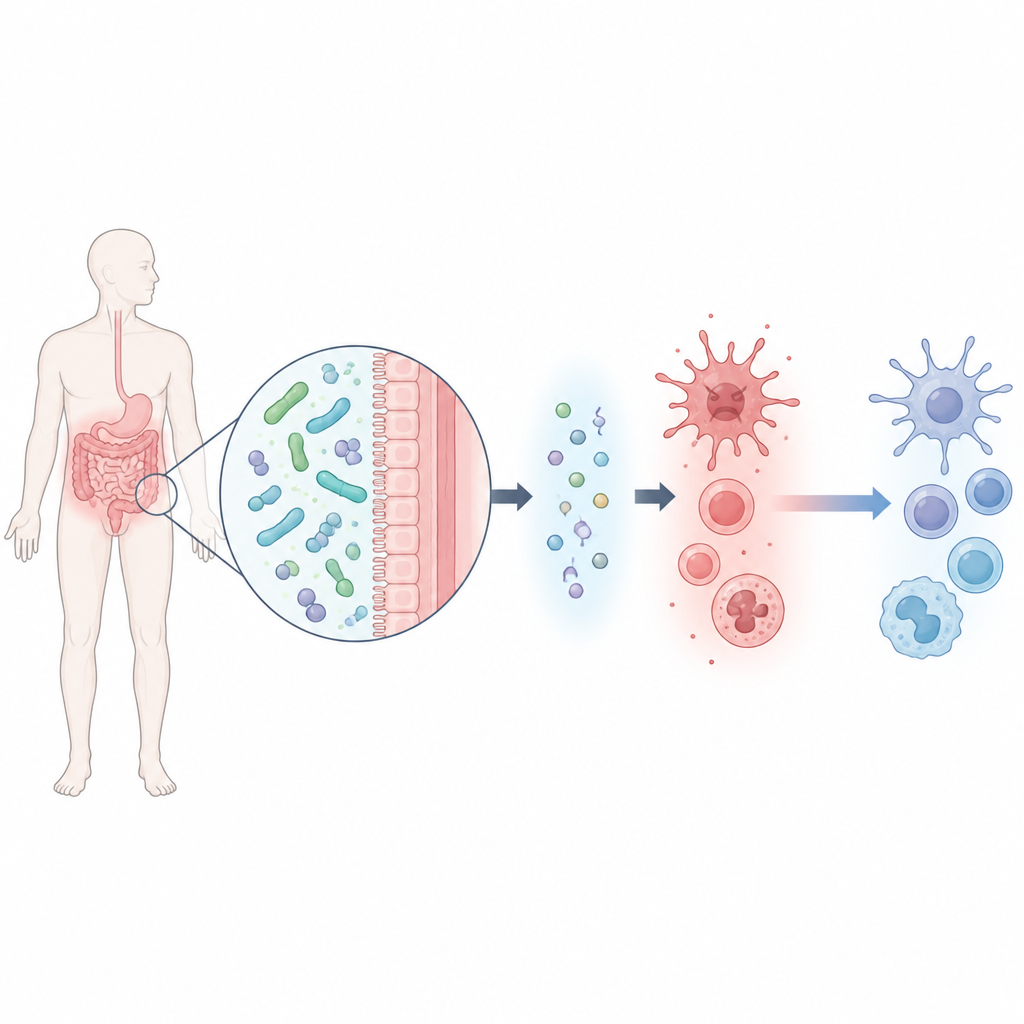
有用な腸内微生物と小さな化学信号
研究チームはまず、低尿酸レベルの健康な男性の糞便からLacticaseibacillus rhamnosus株(M2bと命名)を分離した。この細菌は試験管内で尿酸を分解する能力に優れていた。微生物が放出する化学的副産物を幅広く解析したところ、6つの候補分子が特定され、それらが尿酸でストレスを受けたマウスマクロファージ細胞をどれだけ保護できるかが試験された。β-ヒドロキシ酪酸と呼ばれる一つの分子が際立っており、細胞生存率を向上させるだけでなく、いくつかの主要な炎症性物質を大幅に減少させ、抗炎症性シグナルであるIL-10を増強した。
攻撃的な細胞を修復志向の細胞に変える
この小分子が免疫応答をどのように変えるかを調べるため、研究者はマクロファージを尿酸単独、あるいはβ-ヒドロキシ酪酸やM2b培養上清とともに曝露させた。尿酸単独は細胞を典型的な攻撃姿勢へと駆り立て、M1状態に関連するマーカーが高く、より鎮静的なM2様状態に結びつくマーカーが低下した。β-ヒドロキシ酪酸や細菌培養上清を加えると、これらのパターンは反転した:攻撃マーカーは低下し、修復マーカーは上昇し、顕微鏡下での細胞形態もより落ち着いた様相へと変化した。これは、腸内細菌由来の代謝物が免疫細胞を直接的に有害な反応から遠ざけうることを示した。
受容体の切り替えと細胞内のエネルギーセンサー
変化を観察するだけで終わらず、研究者らはその仕組みを解明しようとした。彼らはマクロファージ表面にあるGPR109aというタンパク質に注目した。GPR109aはβ-ヒドロキシ酪酸のような分子を感知することができる。コンピューターによるモデリングはβ-ヒドロキシ酪酸がこの受容体にぴったり収まることを示唆した。実験では尿酸がGPR109aの発現を低下させる一方で、β-ヒドロキシ酪酸やM2b培養上清がそれを回復させることが確認された。研究者が意図的に細胞内のGPR109aを減らすと、β-ヒドロキシ酪酸の鎮静効果は失われた。逆にGPR109aを増強すると、尿酸ストレス下でも細胞は自然に修復志向へとシフトした。
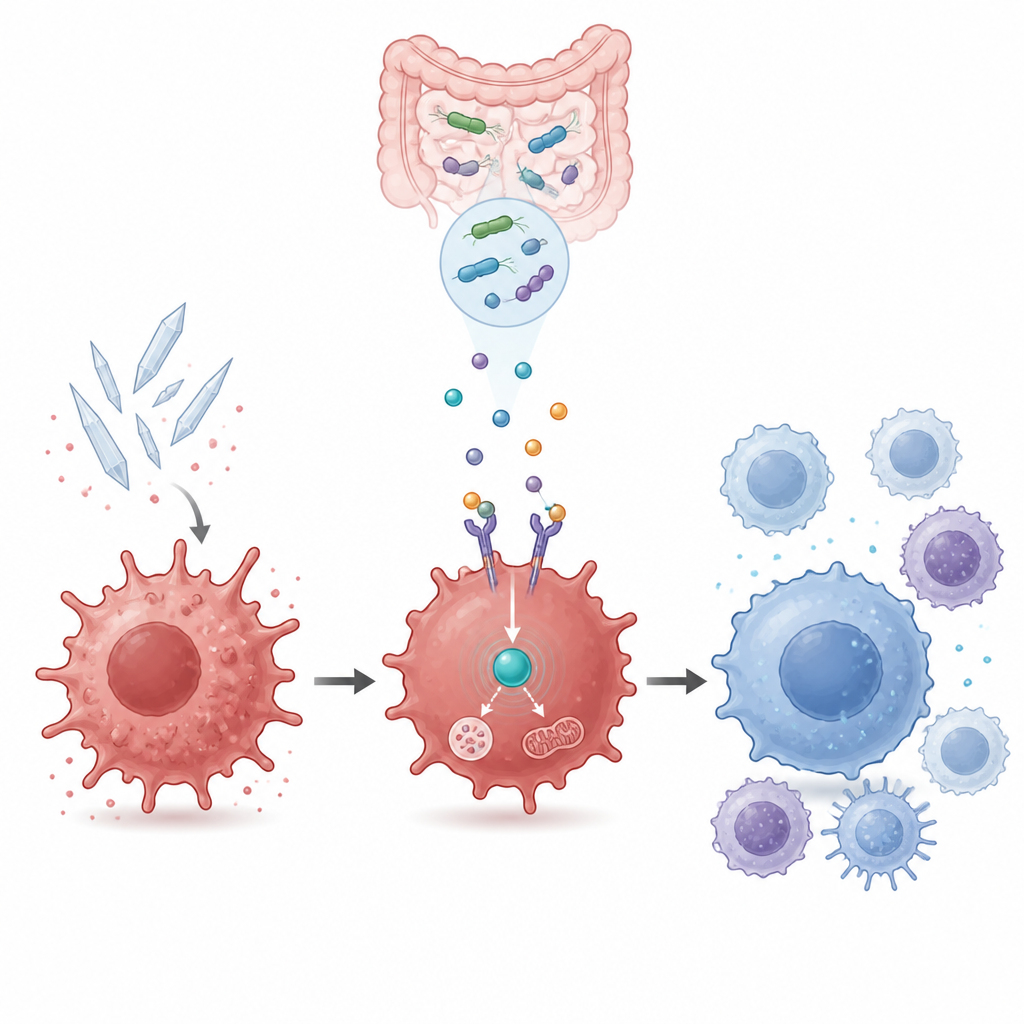
細胞のエネルギー利用と炎症制御の結びつき
細胞内では、GPR109aは細胞のエネルギー状態を感知する重要な因子であるAMPKとつながっている。遺伝子発現測定とタンパク質解析は、尿酸がAMPK活性を鈍らせる一方で、β-ヒドロキシ酪酸がGPR109a依存的にAMPKを回復させることを示した。化学的阻害剤でAMPKをブロックすると、β-ヒドロキシ酪酸やM2b培養上清の利点は消失した:炎症性マーカーが再び増加し、修復マーカーは弱まった。これは、腸菌由来の代謝物が効果を発揮するためには内部のエネルギー感知回路が活性である必要があることを示している。
高尿酸の人々にとっての意味
総合すると、本研究は単純な一連の流れを描き出す:腸内細菌がβ-ヒドロキシ酪酸を産生し、この小分子が免疫細胞上のGPR109a受容体を活性化し、それがAMPKを作動させることでマクロファージを有害な攻撃モードからより穏やかな修復志向のモードへと移行させる。実験は培養されたマウス細胞で行われており、動物や人での検証がまだ必要だが、腸内微生物由来代謝物–GPR109a–AMPK経路は高尿酸に伴う炎症を和らげる有望な標的であり、尿酸低下薬と補完してより精密な免疫鎮静戦略を提供する可能性がある。
引用: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
キーワード: 高尿酸血症, 腸内細菌叢, マクロファージの分極, β-ヒドロキシ酪酸, GPR109a AMPK経路