Clear Sky Science · es
El eje GPR109a-AMPK media la atenuación de la polarización M1 de macrófagos inducida por ácido úrico por β-hidroxibutirato de Lacticaseibacillus rhamnosus M2b
Por qué importan los microbios intestinales para las articulaciones doloridas
Las personas con niveles altos de ácido úrico en sangre a menudo desarrollan gota dolorosa y otros problemas inflamatorios; sin embargo, los tratamientos actuales se centran principalmente en reducir el ácido úrico en lugar de calmar el sistema inmunitario que este activa. Este estudio explora cómo una bacteria intestinal beneficiosa y uno de sus pequeños productos químicos podrían empujar suavemente a las células inmunitarias desde un modo dañino de ataque hacia un modo reparador y calmante, ofreciendo un enfoque novedoso para aliviar la inflamación vinculada al exceso de ácido úrico.
Del ácido úrico elevado a las células inmunitarias enfadadas
La hiperuricemia, o exceso de ácido úrico, es cada vez más común en todo el mundo y se relaciona no solo con la gota, sino también con una inflamación crónica más amplia. El ácido úrico puede inducir a ciertos glóbulos blancos llamados macrófagos a un estado agresivo que libera sustancias inflamatorias y daña los tejidos cercanos. Los investigadores saben que este estado agresivo, a menudo denominado tipo M1, desempeña un papel central en la enfermedad, pero las terapias que guíen de forma directa y segura a estas células hacia un estado más calmado y reparador siguen siendo limitadas.
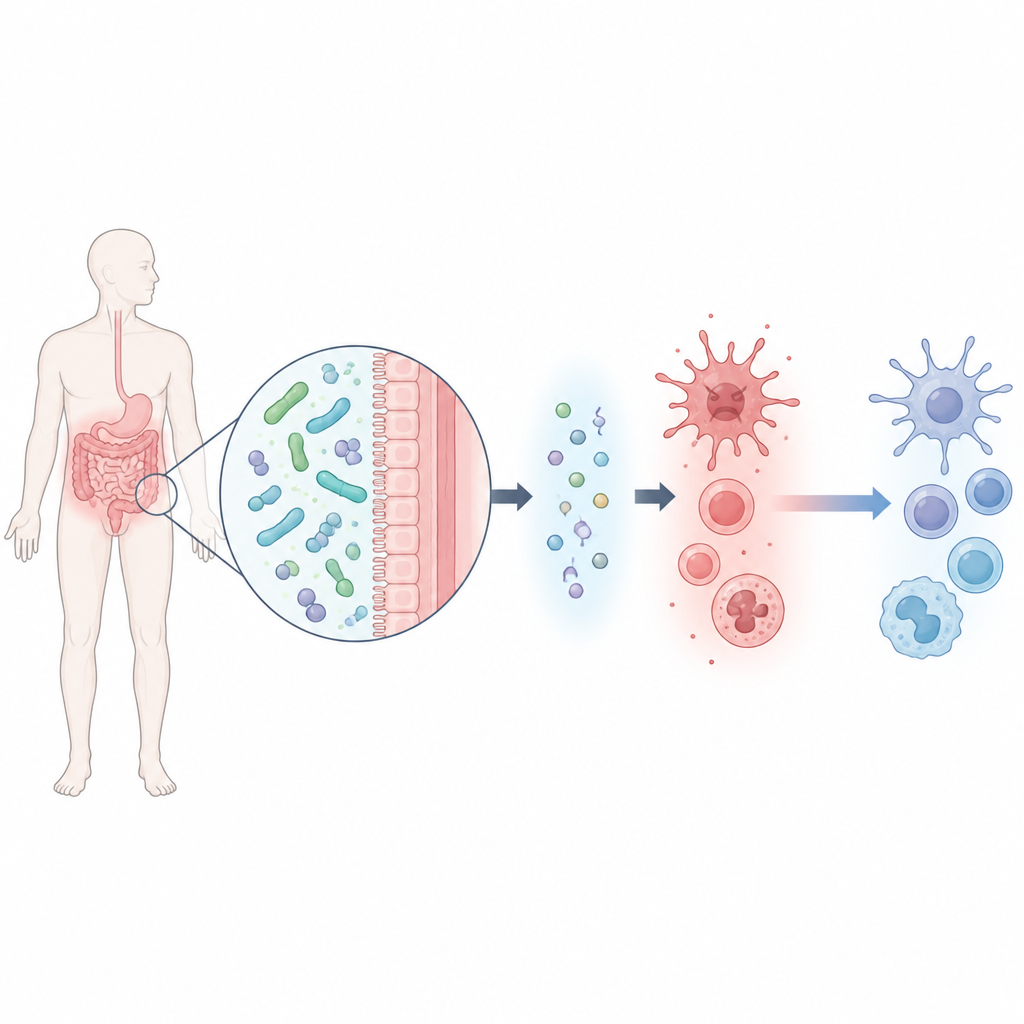
Un microbio intestinal útil y una pequeña señal química
El equipo empezó aislando una cepa de Lacticaseibacillus rhamnosus, llamada M2b, a partir de heces de hombres sanos con bajos niveles de ácido úrico. Esta bacteria destacó por su capacidad para degradar el ácido úrico en el laboratorio. Mediante un análisis amplio de los subproductos químicos que el microbio liberaba, los científicos identificaron seis moléculas candidatas y probaron cuáles podían proteger a macrófagos de ratón estresados por ácido úrico. Una molécula, llamada β-hidroxibutirato, destacó: no solo mejoró la supervivencia celular, sino que también redujo drásticamente varias sustancias inflamatorias clave mientras aumentaba una señal antiinflamatoria llamada IL-10.
Convertir células de ataque en células reparadoras
Para ver cómo esta pequeña molécula modificaba el comportamiento inmunitario, los investigadores expusieron macrófagos a ácido úrico solos o junto con β-hidroxibutirato o con el líquido procedente de cultivos de M2b. El ácido úrico por sí solo impulsó a las células hacia una postura clásica de ataque, con niveles altos de marcadores vinculados al estado M1 y niveles bajos de marcadores asociados a un estado más tranquilizador tipo M2. Cuando se añadió β-hidroxibutirato o el sobrenadante bacteriano, estos patrones se invirtieron: los marcadores de ataque cayeron, los marcadores de reparación aumentaron y la morfología celular observada al microscopio se desplazó hacia una apariencia más calmada. Esto mostró que un metabolito producido por una bacteria intestinal puede inclinar directamente a las células inmunitarias para evitar una respuesta dañina.
Un interruptor de receptor y un sensor de energía dentro de la célula
La historia no terminó al observar estos cambios; los científicos quisieron saber cómo ocurrían. Se centraron en una proteína en la superficie del macrófago conocida como GPR109a, que puede detectar moléculas como el β-hidroxibutirato. Modelos por ordenador sugirieron que el β-hidroxibutirato encaja bien en este receptor. Experimentos confirmaron que el ácido úrico reducía los niveles de GPR109a, mientras que el β-hidroxibutirato y el cultivo M2b los restauraban. Cuando los investigadores redujeron deliberadamente GPR109a en las células, el β-hidroxibutirato perdió sus efectos calmantes. Al potenciar GPR109a, las células cambiaron hacia el estado reparador, incluso bajo estrés por ácido úrico.
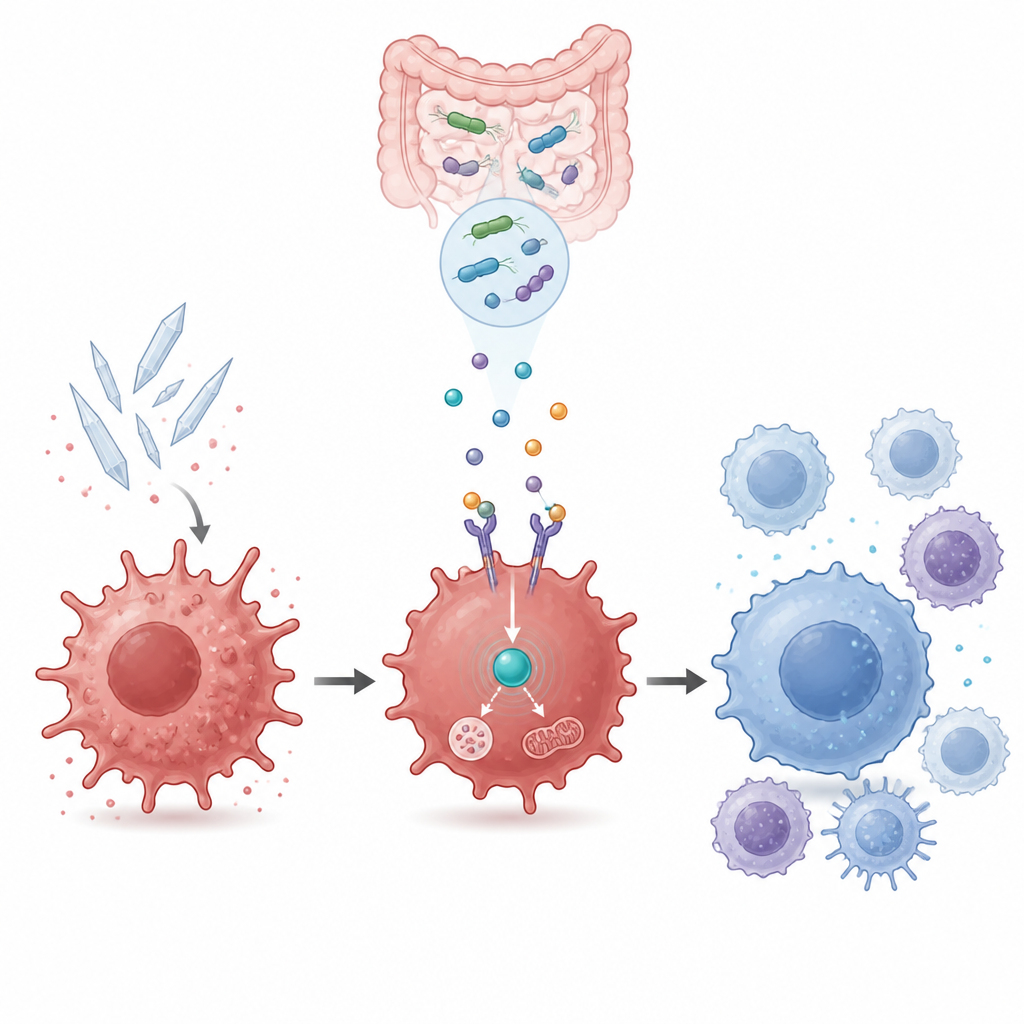
Vincular el uso energético celular al control de la inflamación
Dentro de la célula, GPR109a se conecta con otro actor clave llamado AMPK, un sensor del estado energético celular. Mediciones de la actividad génica y pruebas de proteínas mostraron que el ácido úrico disminuía la actividad de AMPK, mientras que el β-hidroxibutirato la reactivaba de una manera dependiente de GPR109a. Bloquear AMPK con un inhibidor químico eliminó los beneficios del β-hidroxibutirato y del sobrenadante M2b: los marcadores inflamatorios aumentaron de nuevo y los marcadores de reparación se desvanecieron. Esto vinculó el cambio calmante del sistema inmunitario a un circuito de detección energética interno que debe permanecer activo para que el metabolito bacteriano funcione.
Qué podría significar esto para las personas con ácido úrico alto
En conjunto, los hallazgos dibujan una cadena sencilla de eventos: una bacteria intestinal produce β-hidroxibutirato, esta pequeña molécula activa el receptor GPR109a en las células inmunitarias, lo que a su vez enciende AMPK y ayuda a mover a los macrófagos de un modo dañino de ataque a un modo más pacífico y orientado a la reparación. Aunque el trabajo se realizó en cultivos de células de ratón y aún necesita pruebas en animales y en personas, apunta a la ruta metabólito microbiano → GPR109a → AMPK como un objetivo prometedor para aliviar la inflamación en la hiperuricemia, potencialmente complementando los fármacos estándar que reducen el ácido úrico con estrategias más precisas de calma inmunitaria.
Cita: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
Palabras clave: hiperuricemia, microbiota intestinal, polarización de macrófagos, β-hidroxibutirato, vía GPR109a AMPK