Clear Sky Science · he
ציר GPR109a-AMPK מתווך האטת הקוטביות של מאקרופאגים מסוג M1 המועלת על ידי חומצת שתן על ידי β-הידרוקסיבוטיראט מ‑Lacticaseibacillus rhamnosus M2b
למה חיידקי המעיים חשובים במפרקים כואבים
אנשים עם רמות גבוהות של חומצת שתן בדם מפתחים לעיתים קרובות גאוטה וכאבים דלקתיים אחרים, אך הטיפולים הנוכחיים מתמקדים בעיקר בהורדת חומצת השתן ולא בהרגעת מערכת החיסון שהיא מגרה. מחקר זה בוחן כיצד חיידק מעיים מועיל ואחת מהמולקולות הקטנות שהוא מייצר עשויים בעדינות לדחוף תאי חיסון ממצב התקפי מזיק למצב מרגיע ותיקוני, ומציע זווית חדשה להקלת דלקת הקשורה לחומצת שתן גבוהה.
מחומצת שתן גבוהה לתאי חיסון כועסים
היפראוריצמיה, או רמות גבוהות של חומצת שתן, נפוצה יותר בעולם ומתקשרת לא רק לגאוטה אלא גם לדלקות כרוניות נרחבות. חומצת שתן יכולה לדחוף סוגים מסוימים של תאי דם לבנים, המכונים מאקרופאגים, למצב תוקפני שפולט חומרים דלקתיים ופוגע ברקמות סמוכות. חוקרים יודעים שמצב תוקפני זה, שלעיתים נקרא סוג M1, ממלא תפקיד מרכזי במחלה, אך יש עדיין מעט טיפולים שמכוונים באופן ישיר ובטוח להחזיר תאים אלה למצב מרגיע ומרפא.
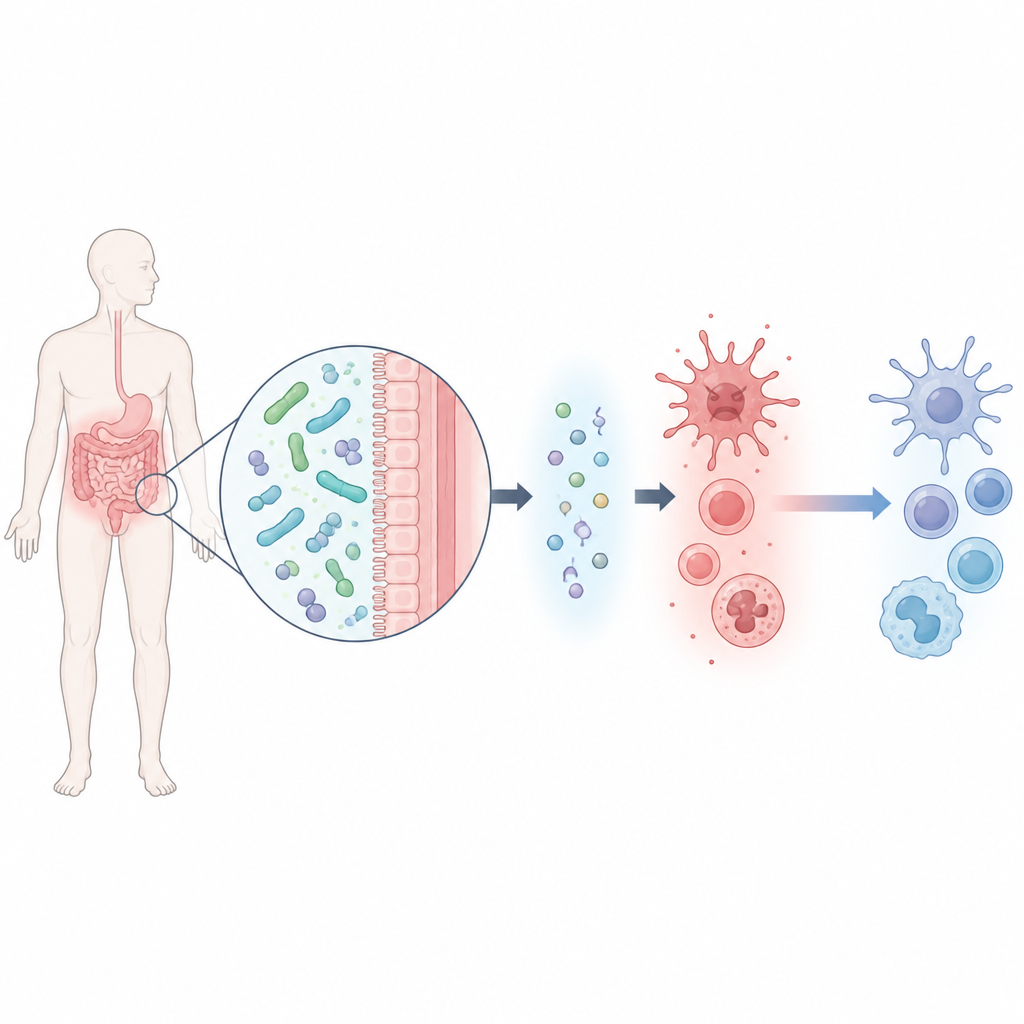
מיקרוב מועיל ואות כימי קטן
הצוות התחיל בבידוד זן של Lacticaseibacillus rhamnosus, שנקרא M2b, מצואה של גברים בריאים עם רמות חומצת שתן נמוכות. חיידק זה הצטיין בפירוק חומצת שתן במעבדה. באמצעות סקר רחב של תוצרי הלוואי הכימיים שהמיקרוב שחרר, זיהו המדענים שישה מולקולות מועמדות ובחנו אילו מהן יכולות להגן על תאי מאקרופאג של עכבר שנפגעו על ידי חומצת שתן. מולקולה אחת, שנקראת ביתא‑הידרוקסיבוטיראט, בלטה: היא לא רק שיפרה את הישרדות התאים אלא גם הפחיתה באופן חד מספר חומרים דלקתיים מרכזיים ובו זמנית הגבירה אות אנטי‑דלקתי שנקרא IL‑10.
להפוך תאים תוקפניים לתאים מרפאים
כדי להבין כיצד המולקולה הקטנה הזו שינתה את התנהגות החיסון, החוקרים חשפו מאקרופאגים לחומצת שתן לבדה או יחד עם ביתא‑הידרוקסיבוטיראט או נוזל מתרביות M2b. חומצת השתן לבד הובילה את התאים לתנוחה התקפית אופיינית, עם רמות גבוהות של סמנים המקושרים למצב M1 ורמות נמוכות של סמנים הקשורים למצב מרגיע, בדומה ל‑M2. כשהתווסף ביתא‑הידרוקסיבוטיראט או נוזל התרבית החיידקי, הדפוסים הללו התהפכו: סמני ההתקפה ירדו, סמני הריפוי עלו, וצורת התאים במיקרוסקופ נטתה למראה רגוע יותר. זה הראה שמטבוליט שמיוצר על‑ידי חיידק מעיים יכול להפנות ישירות את תאי החיסון מריאקציה מזיקה.
מחליף קולטן וחיישן אנרגיה בתוך התא
הסיפור לא הסתיים בתצפית על השינויים; המדענים רצו לדעת כיצד הם מתרחשים. הם התמקדו בחלבון על פני המאקרופאגים הידוע כ‑GPR109a, שיכול לחוש מולקולות כמו ביתא‑הידרוקסיבוטיראט. סימולציה ממוחשבת רמזה שביתא‑הידרוקסיבוטיראט מתיישב בנוחות בתוך הקולטן הזה. ניסויים אישרו שחומצת שתן מורידה את רמות GPR109a, בעוד שביתא‑הידרוקסיבוטיראט ונוזל תרבית M2b משחזרים אותן. כאשר החוקרים הפחיתו במכוון את GPR109a בתאים, ביתא‑הידרוקסיבוטיראט איבד את אפקט ההרגעה שלו. כשהגבילו את GPR109a, למעשה כשהעלו את הביטוי שלו, התאים נטו מעצמם למצב ריפוי, גם תחת לחץ חומצת שתן.
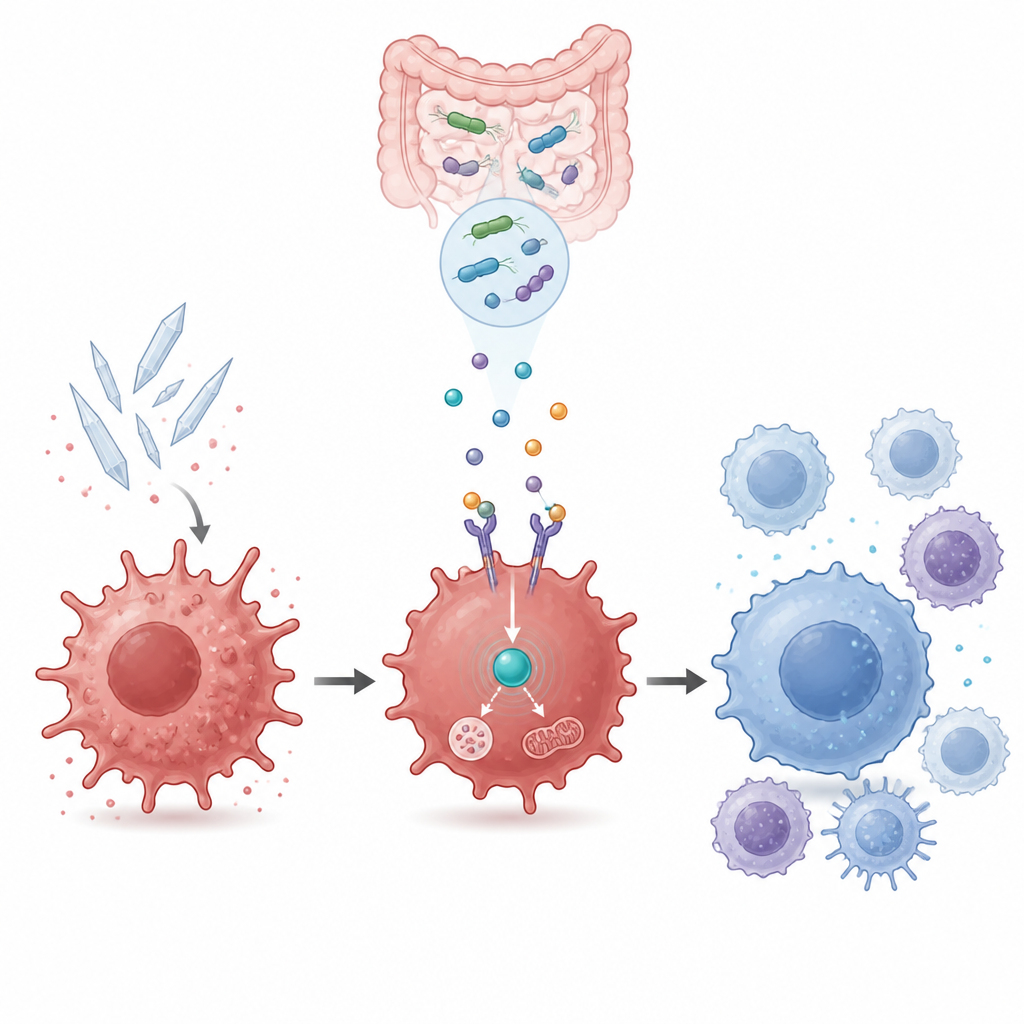
קישור בין שימוש באנרגיה לשליטה בדלקת
בתוך התא, GPR109a מקשר לשחקן מרכזי נוסף שנקרא AMPK, חיישן מעמד האנרגיה של התא. מדידות ביטוי גנים ובדיקות חלבון הראו שחומצת שתן מדכאת את פעילות AMPK, בעוד שביתא‑הידרוקסיבוטיראט משחזר אותה בצורה שתלויה ב‑GPR109a. חסימה של AMPK באמצעות מעכב כימי מחקה את היתרונות של ביתא‑הידרוקסיבוטיראט ונוזל התרבית של M2b: סמני הדלקת עלו שוב, וסמני הריפוי פחתו. זה קישר את ההתקדמות לעבר מצב חיסוני מרגיע למעגל חיישן אנרגיה פנימי שצריך להיות פעיל כדי שהמטבוליט החיידקי יעבוד.
מה המשמעות לאנשים עם חומצת שתן גבוהה
ביחד, הממצאים מציירים שרשרת אירועים פשוטה: חיידק מעיים מייצר ביתא‑הידרוקסיבוטיראט, המולקולה הפעילה את קולטן GPR109a על תאי החיסון, אשר בתורו מפעיל את AMPK ועוזר להזיז מאקרופאגים ממצב התקפי מזיק למצב שיותר שקט ומכוון תיקון. אמנם העבודה נעשתה בתאים מושרשים של עכברים ודורשת עדיין בדיקות בבעלי חיים ובאנשים, אך היא מצביעה על מסלול המטבוליט‑GPR109a‑AMPK כחיסכון מבטיח להרפיית דלקת בהיפראוריצמיה, וכפוטנציאל להשלים טיפולים סטנדרטיים להורדת חומצת שתן עם אסטרטגיות מדויקות להרגעת המערכת החיסונית.
ציטוט: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
מילות מפתח: היפר-אוריצמיה, מיקרוביוטת מעיים, קוטביות מאקרופאגים, ביתא הידרוקסיבוטיראט, מסלול GPR109a AMPK