Clear Sky Science · sv
GPR109a-AMPK-axeln förmedlar dämpningen av urinsyra‑inducerad M1‑makrofagpolarisering av β‑hydroxibutyrat från Lacticaseibacillus rhamnosus M2b
Varför tarmbakterier spelar roll för ömma leder
Människor med höga nivåer urinsyra i blodet utvecklar ofta smärtsam gikt och andra inflammatoriska problem, men dagens behandlingar fokuserar mest på att sänka urinsyran snarare än på att lugna immunsystemet som den aktiverar. Denna studie undersöker hur en nyttig tarmbakterie och en av dess små kemiska produkter kan skjuta immunceller försiktigt bort från ett skadligt, aggressivt läge och mot ett lugnande, reparerande läge, vilket erbjuder en ny vinkel för att lindra inflammation kopplad till hög urinsyra.
Från hög urinsyra till arga immunceller
Hyperurikemi, eller hög urinsyra, blir allt vanligare globalt och är kopplat inte bara till gikt utan även till mer utbredd kronisk inflammation. Urinsyra kan driva vissa vita blodkroppar, så kallade makrofager, in i ett aggressivt tillstånd som utsöndrar inflammatoriska substanser och skadar närliggande vävnader. Forskare vet att detta aggressiva tillstånd, ofta kallat M1‑typen, spelar en central roll i sjukdom, men terapeutiska metoder som direkt och säkert styr dessa celler tillbaka mot ett lugnare, läkningsinriktat tillstånd är fortfarande begränsade.
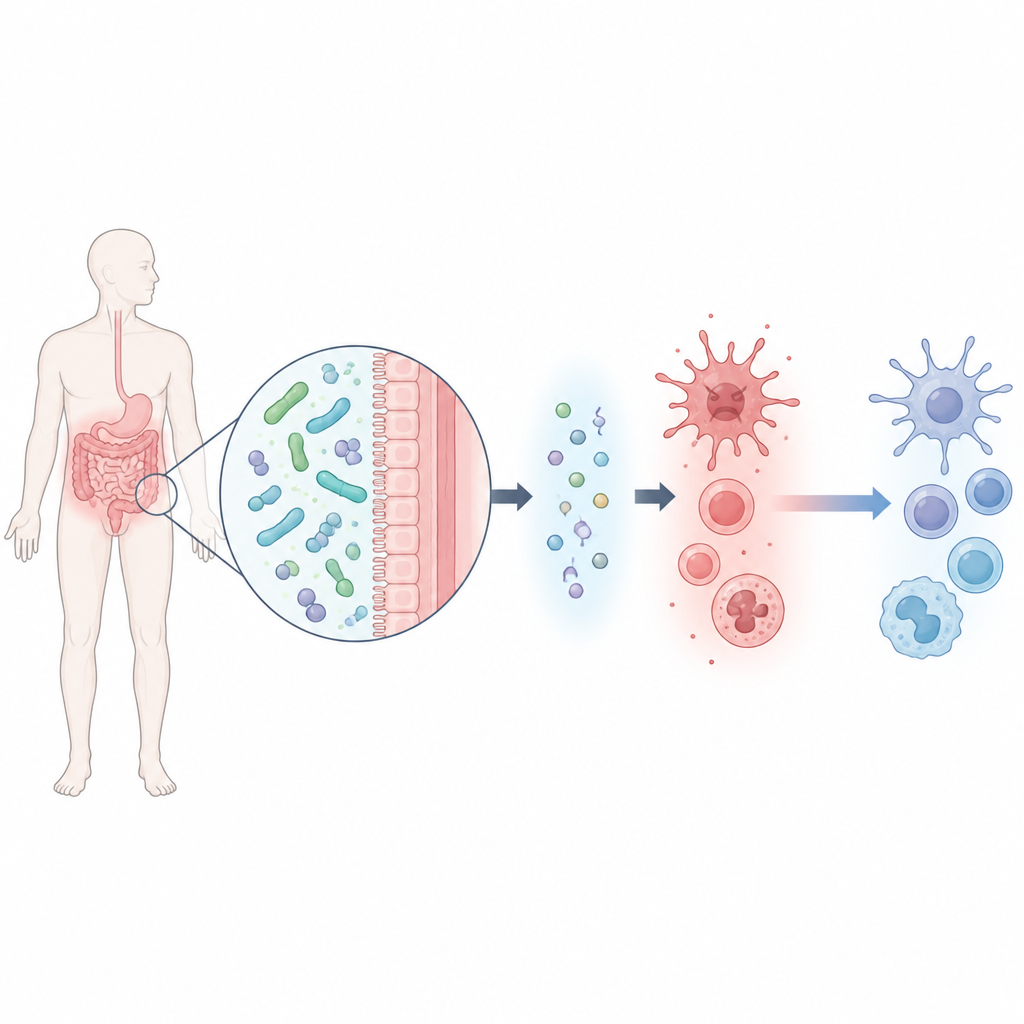
En hjälpsam tarmmikrob och en liten kemisk signal
Teamet började med att isolera en stam av Lacticaseibacillus rhamnosus, kallad M2b, från avföring hos friska män med låga urinsyranivåer. Denna bakterie var särskilt bra på att bryta ner urinsyra i laboratoriet. Genom en bred kartläggning av de kemiska biprodukterna som mikroben frisatte identifierade forskarna sex kandidatmolekyler och testade vilka som kunde skydda musmakrofagceller som stressats av urinsyra. En molekyl, kallad beta‑hydroxibutyrat, utmärkte sig: den förbättrade inte bara cellöverlevnad utan minskade också markant flera nyckelinflammatoriska ämnen samtidigt som den ökade en antiinflammatorisk signal kallad IL‑10.
Att förvandla angripande celler till läkande celler
För att se hur denna lilla molekyl omformade immunsvar exponerade forskarna makrofager för urinsyra ensam eller tillsammans med beta‑hydroxibutyrat eller vätska hämtad från M2b‑kulturer. Urinsyra ensam drev cellerna in i en klassisk attackpostur, med höga nivåer av markörer kopplade till M1‑tillståndet och låga nivåer av markörer för ett mer lugnande, M2‑liknande tillstånd. När beta‑hydroxibutyrat eller bakteriekulturvätskan tillsattes vändes dessa mönster: attackmarkörerna sjönk, läkarmarkörerna steg och cellernas form under mikroskopet skiftade mot ett lugnare utseende. Detta visade att en metabolit från en tarmbakterie direkt kan luta immunceller bort från ett skadligt svar.
En receptoromkopplare och en energisensor inne i cellen
Berättelsen slutade inte vid observationen av dessa förändringar; forskarna ville veta hur de uppstod. De fokuserade på ett protein på makrofagernas yta känt som GPR109a, som kan känna av molekyler som beta‑hydroxibutyrat. Datorbaserad modellering föreslog att beta‑hydroxibutyrat passar väl i denna receptor. Experiment bekräftade att urinsyra sänkte GPR109a‑nivåerna, medan beta‑hydroxibutyrat och M2b‑kultur återställde dem. När forskarna avsiktligt minskade GPR109a i cellerna, förlorade beta‑hydroxibutyrat sina lugnande effekter. När de ökade GPR109a skiftade cellerna naturligt mot läkning, även under urinsyra‑stress.
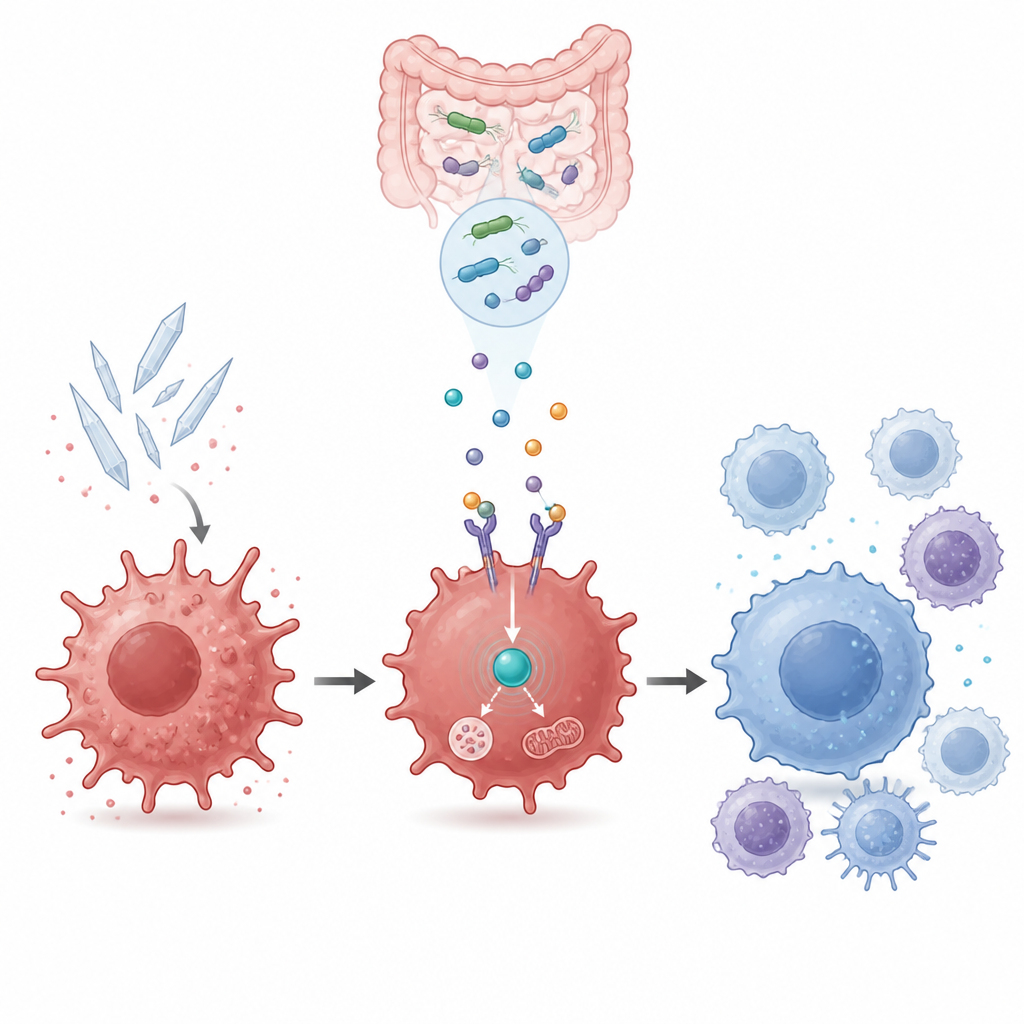
Att koppla cellens energianvändning till inflammationskontroll
Inne i cellen kopplar GPR109a till en annan nyckelspelare kallad AMPK, en sensor för cellens energistatus. Genuttrycksmätningar och proteinanalyser visade att urinsyra dämpade AMPK‑aktiviteten, medan beta‑hydroxibutyrat återupplivade den på ett sätt som var beroende av GPR109a. Blockering av AMPK med en kemisk hämmare utsuddade fördelarna med beta‑hydroxibutyrat och M2b‑kulturen: inflammatoriska markörer steg igen och läkarmarkörer avtog. Det kopplade det lugnande immunskiftet till en intern energisensorkrets som måste vara aktiv för att den bakteriella metaboliten ska verka.
Vad detta kan betyda för personer med hög urinsyra
Sammantaget skissar fynden en enkel händelsekedja: en tarmbakterie tillverkar beta‑hydroxibutyrat, denna lilla molekyl aktiverar GPR109a‑receptorn på immunceller, vilket i sin tur slår på AMPK och hjälper till att flytta makrofager från ett skadligt attackläge till ett mer fridfullt, reparationsinriktat tillstånd. Även om arbetet utförts i odlade musceller och fortfarande behöver testas i djur och människor, pekar det på tarmmikrobmetaboliten GPR109a‑AMPK‑vägen som ett lovande mål för att lindra inflammation vid hyperurikemi, och potentiellt komplettera standardbehandlingar som sänker urinsyra med mer precisa strategier för att lugna immunsvaret.
Citering: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
Nyckelord: hyperurikemi, tarmmikrobiota, makrofagpolarisering, beta‑hydroxibutyrat, GPR109a AMPK‑väg