Clear Sky Science · it
L’asse GPR109a-AMPK media l’attenuazione della polarizzazione M1 dei macrofagi indotta dall’acido urico da parte del beta-idrossibutirrato prodotto da Lacticaseibacillus rhamnosus M2b
Perché i batteri intestinali sono importanti per le articolazioni doloranti
Le persone con livelli alti di acido urico nel sangue sviluppano spesso gotta dolorosa e altri problemi infiammatori, mentre i trattamenti correnti si concentrano principalmente sull’abbassamento dell’acido urico piuttosto che sul calmare il sistema immunitario che esso agita. Questo studio esplora come un batterio intestinale utile e uno dei suoi piccoli prodotti chimici possano spingere delicatamente le cellule immunitarie lontano da uno stato dannoso e d’attacco verso una modalità più lenitiva e riparativa, offrendo un nuovo approccio per alleviare l’infiammazione legata all’elevato acido urico.
Dall’acido urico elevato alle cellule immunitarie infiammate
L’iperuricemia, ovvero l’aumento dell’acido urico, è sempre più comune a livello mondiale ed è collegata non solo alla gotta ma anche a forme più diffuse di infiammazione cronica. L’acido urico può indurre alcuni globuli bianchi chiamati macrofagi in uno stato aggressivo che riversa mediatori infiammatori danneggiando i tessuti vicini. I ricercatori sanno che questo stato aggressivo, spesso definito tipo M1, svolge un ruolo centrale nella malattia, ma le terapie che riportano direttamente e in modo sicuro queste cellule verso uno stato più calmo e riparativo sono ancora limitate.
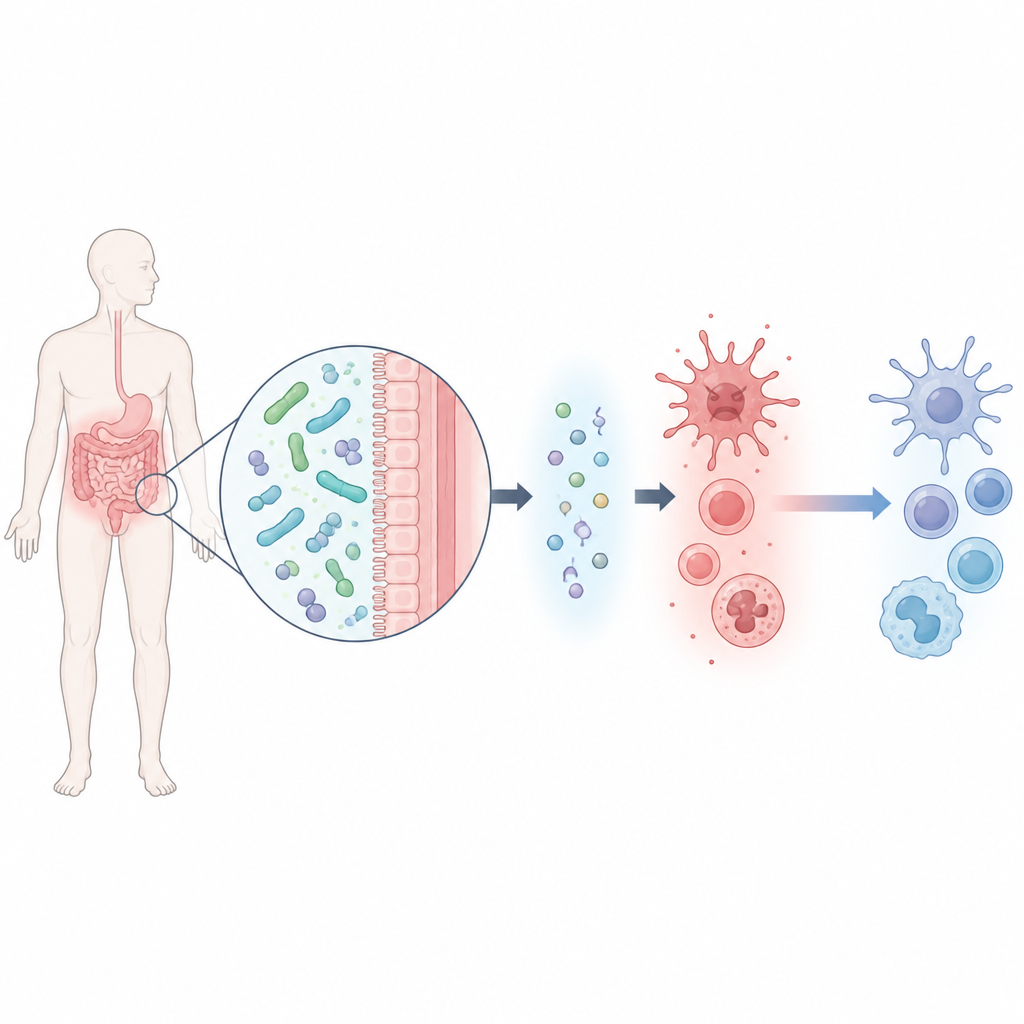
Un microbo intestinale utile e un piccolo segnale chimico
Il gruppo ha iniziato isolando un ceppo di Lacticaseibacillus rhamnosus, chiamato M2b, dalle feci di uomini sani con bassi livelli di acido urico. Questo batterio si è dimostrato particolarmente efficace nel degradare l’acido urico in laboratorio. Tramite un’analisi ampia dei sottoprodotti chimici rilasciati dal microbo, gli scienziati hanno identificato sei molecole candidate e hanno testato quali di esse potessero proteggere macrofagi murini stressati dall’acido urico. Una molecola, chiamata beta-idrossibutirrato, è emersa con evidenza: non solo migliorava la sopravvivenza cellulare, ma riduceva nettamente diverse sostanze infiammatorie chiave aumentando al contempo un segnale anti-infiammatorio chiamato IL-10.
Trasformare cellule d’attacco in cellule che riparano
Per capire come questa piccola molecola rimodellasse il comportamento immunitario, i ricercatori hanno esposto i macrofagi all’acido urico da soli o in combinazione con il beta-idrossibutirrato o con il liquido di coltura di M2b. L’acido urico da solo spingeva le cellule in una postura classica d’attacco, con livelli elevati di marcatori associati allo stato M1 e livelli bassi di marcatori legati a uno stato più lenitivo, simile a M2. Quando venivano aggiunti il beta-idrossibutirrato o il liquido di coltura batterica, questi schemi si invertivano: i marcatori d’attacco diminuivano, i marcatori di riparazione aumentavano e la morfologia delle cellule osservata al microscopio assumeva un aspetto più calmo. Ciò dimostrava che un metabolita prodotto da un batterio intestinale poteva inclinare direttamente le cellule immunitarie lontano da una risposta dannosa.
Un interruttore recettoriale e un sensore energetico dentro la cellula
La storia non si è fermata all’osservazione di questi cambiamenti; gli scienziati hanno voluto capire come avvenissero. Si sono concentrati su una proteina presente sulla superficie dei macrofagi nota come GPR109a, che può rilevare molecole come il beta-idrossibutirrato. Modellizzazione al computer ha suggerito che il beta-idrossibutirrato si incastra comodamente in questo recettore. Gli esperimenti hanno confermato che l’acido urico riduceva i livelli di GPR109a, mentre il beta-idrossibutirrato e il liquido di coltura M2b li ripristinavano. Quando i ricercatori hanno ridotto deliberatamente GPR109a nelle cellule, il beta-idrossibutirrato ha perso i suoi effetti calmanti. Quando hanno aumentato GPR109a, le cellule si sono spostate naturalmente verso lo stato di riparazione, anche sotto stress da acido urico.
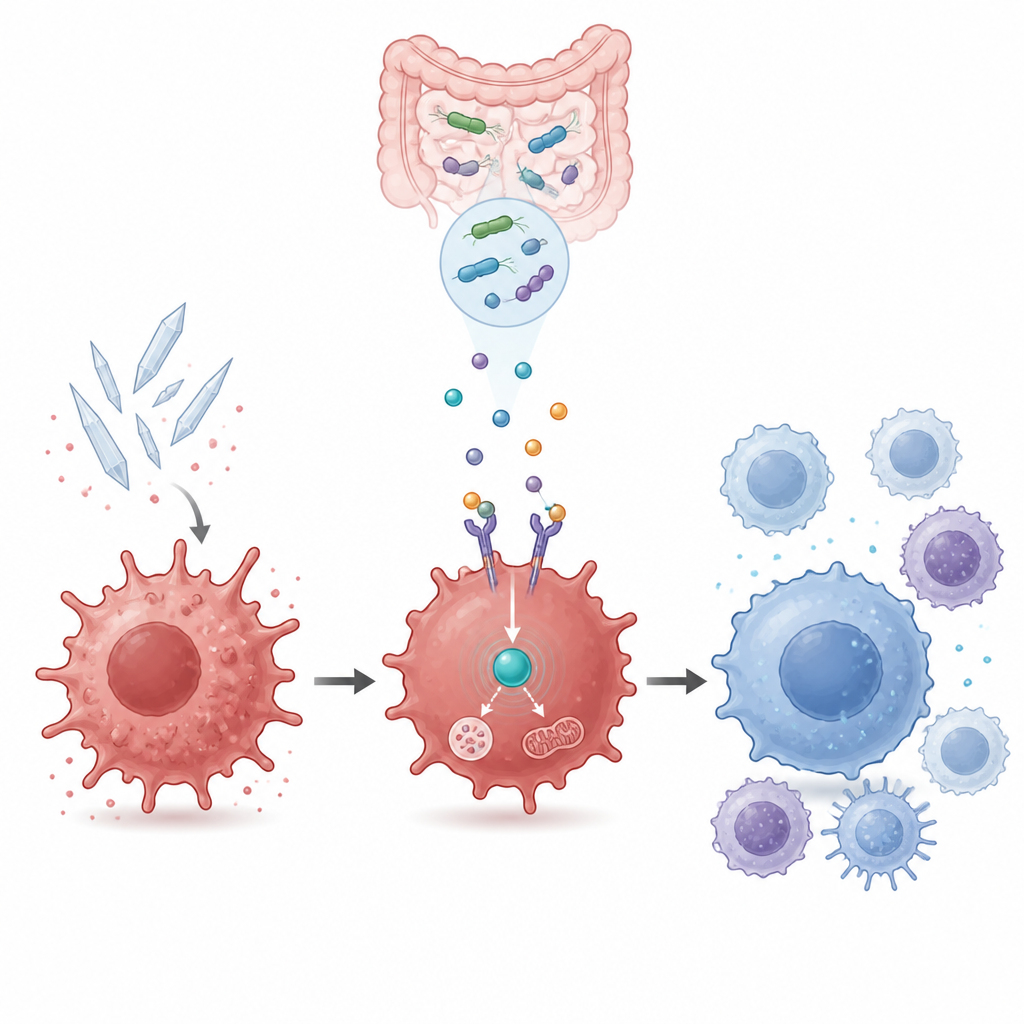
Collegare l’uso energetico cellulare al controllo dell’infiammazione
All’interno della cellula, GPR109a si collega a un altro attore chiave chiamato AMPK, un sensore dello stato energetico cellulare. Misurazioni dell’attività genica e test proteici hanno mostrato che l’acido urico attenuava l’attività di AMPK, mentre il beta-idrossibutirrato la riattivava in modo dipendente da GPR109a. Il blocco di AMPK con un inibitore chimico annullava i benefici del beta-idrossibutirrato e del liquido di coltura M2b: i marcatori infiammatori ritornavano elevati e i marcatori di riparazione diminuivano. Questo ha collegato il cambiamento calmante del sistema immunitario a un circuito interno di rilevamento energetico che deve rimanere attivo affinché il metabolita batterico eserciti il suo effetto.
Cosa potrebbe significare per le persone con acido urico elevato
Nel complesso, i risultati delineano una catena di eventi semplice: un batterio intestinale produce beta-idrossibutirrato, questa piccola molecola attiva il recettore GPR109a sulle cellule immunitarie, che a sua volta accende AMPK e aiuta a spostare i macrofagi da una modalità d’attacco dannosa a una modalità più pacifica e orientata alla riparazione. Sebbene il lavoro sia stato eseguito su cellule murine in coltura e richieda ancora verifiche in animali e persone, esso indica la via metabolita microbico → GPR109a → AMPK come un bersaglio promettente per attenuare l’infiammazione nell’iperuricemia, potenzialmente complementare ai farmaci tradizionali che abbassano l’acido urico con strategie più mirate di modulazione immunitaria.
Citazione: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
Parole chiave: iperuricemia, microbiota intestinale, polarizzazione dei macrofagi, beta-idrossibutirrato, via GPR109a AMPK