Clear Sky Science · fr
L’axe GPR109a-AMPK médie l’atténuation de la polarisation M1 des macrophages induite par l’acide urique par le β-hydroxybutyrate de Lacticaseibacillus rhamnosus M2b
Pourquoi les microbes intestinaux comptent pour les articulations douloureuses
Les personnes présentant un taux élevé d’acide urique dans le sang développent souvent la goutte douloureuse et d’autres troubles inflammatoires. Pourtant, les traitements actuels se concentrent principalement sur la diminution de l’acide urique plutôt que sur l’apaisement du système immunitaire qu’il irrite. Cette étude examine comment une bactérie intestinale bénéfique et l’un de ses petits produits chimiques peuvent doucement pousser les cellules immunitaires hors d’un état agressif et nocif vers un état de réparation plus apaisé, offrant une nouvelle perspective pour soulager l’inflammation liée à l’acide urique élevé.
De l’acide urique élevé aux cellules immunitaires en colère
L’hyperuricémie, ou excès d’acide urique, devient de plus en plus fréquente dans le monde et est liée non seulement à la goutte mais aussi à une inflammation chronique plus large. L’acide urique peut pousser certains globules blancs appelés macrophages dans un état agressif qui sécrète des substances inflammatoires endommageant les tissus voisins. Les chercheurs savent que cet état agressif, souvent désigné sous le nom de type M1, joue un rôle central dans la maladie, mais les thérapies qui orientent ces cellules de manière directe et sûre vers un état plus calme et réparateur restent limitées.
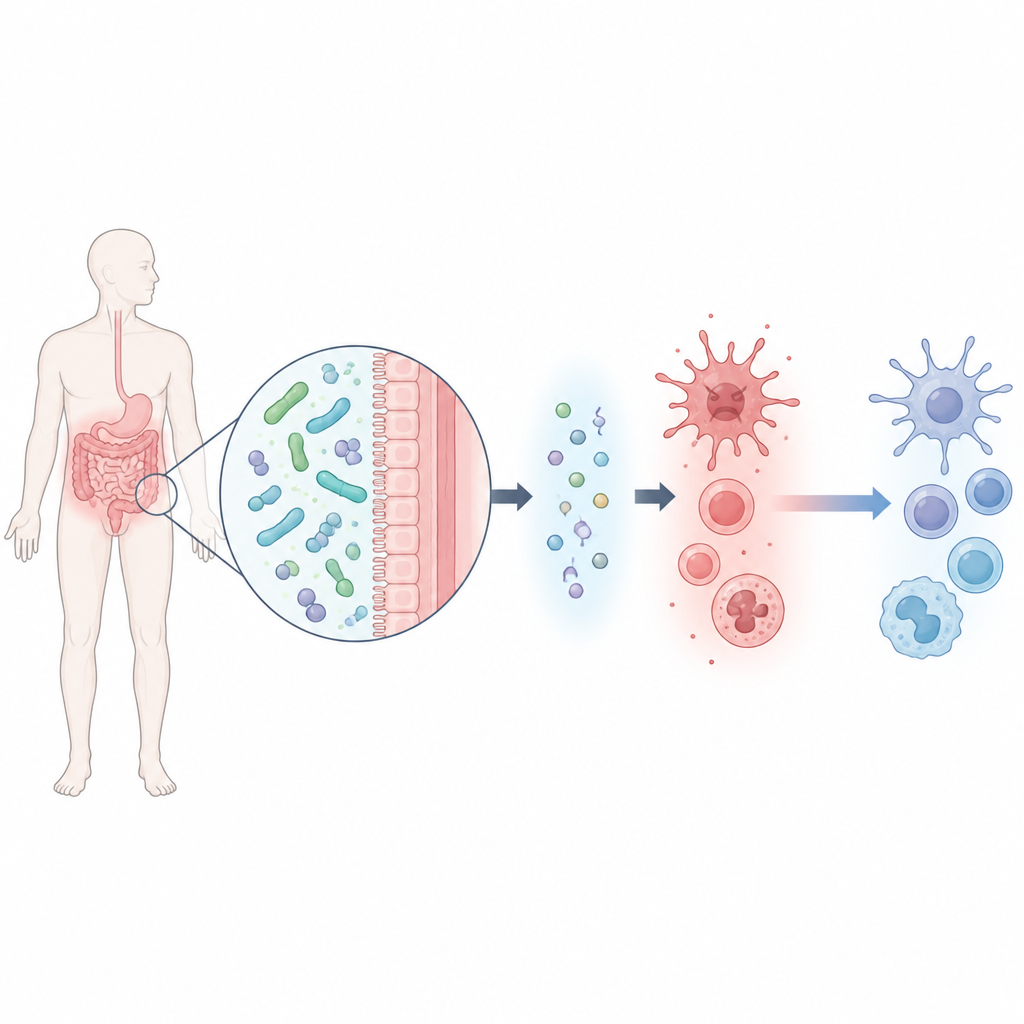
Un microbe intestinal utile et un petit signal chimique
L’équipe a commencé par isoler une souche de Lacticaseibacillus rhamnosus, nommée M2b, à partir de selles d’hommes en bonne santé ayant de faibles niveaux d’acide urique. Cette bactérie s’est montrée excellente pour dégrader l’acide urique en laboratoire. En réalisant un large inventaire des sous-produits chimiques libérés par le microbe, les scientifiques ont identifié six molécules candidates et testé lesquelles pouvaient protéger des cellules macrophages de souris stressées par l’acide urique. Une molécule, le β-hydroxybutyrate, s’est distinguée : elle améliore non seulement la survie cellulaire mais réduit fortement plusieurs médiateurs inflammatoires clés tout en augmentant le signal anti-inflammatoire IL-10.
Transformer des cellules d’attaque en cellules de réparation
Pour comprendre comment cette petite molécule modifiait le comportement immunitaire, les chercheurs ont exposé des macrophages à l’acide urique seul ou en présence de β-hydroxybutyrate ou de liquide de culture de M2b. L’acide urique seul poussait les cellules dans une posture d’attaque classique, avec des niveaux élevés de marqueurs associés à l’état M1 et des niveaux faibles de marqueurs liés à un état plus apaisant, de type M2. Lorsque le β-hydroxybutyrate ou le liquide de culture bactérien était ajouté, ces profils s’inversaient : les marqueurs d’attaque diminuaient, les marqueurs de réparation augmentaient et la morphologie des cellules au microscope montrait une apparence plus calme. Cela démontrait qu’un métabolite produit par une bactérie intestinale pouvait directement incliner les cellules immunitaires hors d’une réponse dommageable.
Un basculement de récepteur et un capteur d’énergie à l’intérieur de la cellule
L’histoire ne s’est pas arrêtée à l’observation de ces changements ; les scientifiques ont voulu savoir comment ils se produisaient. Ils se sont concentrés sur une protéine à la surface des macrophages connue sous le nom de GPR109a, qui peut détecter des molécules comme le β-hydroxybutyrate. La modélisation informatique a suggéré que le β-hydroxybutyrate s’emboîte bien dans ce récepteur. Les expériences ont confirmé que l’acide urique abaissait les niveaux de GPR109a, tandis que le β-hydroxybutyrate et le liquide de culture M2b les rétablissaient. Lorsque les chercheurs ont délibérément réduit GPR109a dans les cellules, le β-hydroxybutyrate a perdu ses effets calmants. Lorsqu’ils ont augmenté GPR109a, les cellules se sont naturellement orientées vers l’état réparateur, même sous stress par l’acide urique.
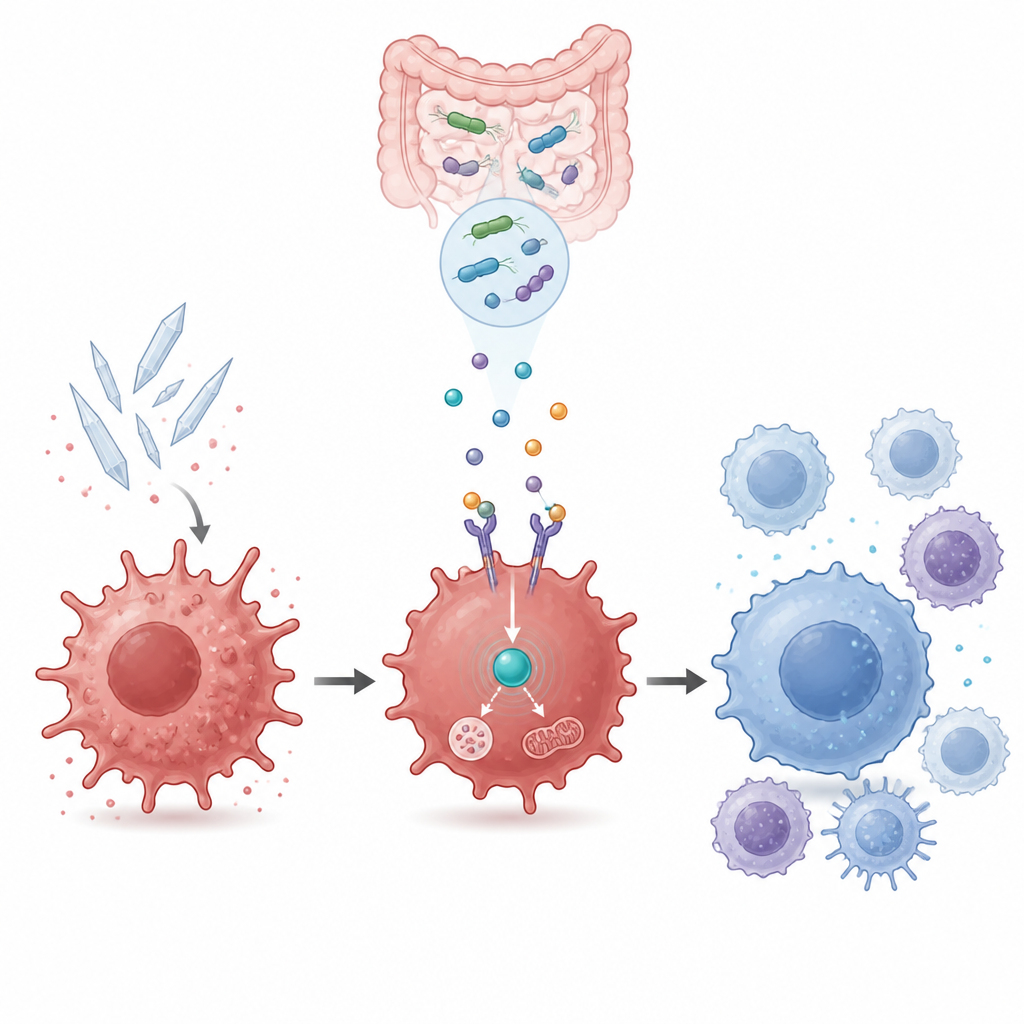
Relier l’utilisation d’énergie cellulaire au contrôle de l’inflammation
À l’intérieur de la cellule, GPR109a se connecte à un autre acteur clé appelé AMPK, un senseur du statut énergétique cellulaire. Les mesures de l’activité génique et des protéines ont montré que l’acide urique affaiblissait l’activité d’AMPK, tandis que le β-hydroxybutyrate la réactivait d’une manière dépendante de GPR109a. Le blocage d’AMPK avec un inhibiteur chimique supprimait les bénéfices du β-hydroxybutyrate et du liquide de culture M2b : les marqueurs inflammatoires réaugmentaient et les marqueurs de réparation diminuaient. Cela reliait le basculement immunitaire apaisant à un circuit interne de détection énergétique qui doit rester actif pour que le métabolite bactérien fasse effet.
Ce que cela pourrait signifier pour les personnes ayant un fort taux d’acide urique
Pris ensemble, ces résultats dessinent une chaîne d’événements simple : une bactérie intestinale produit du β-hydroxybutyrate, cette petite molécule active le récepteur GPR109a sur les cellules immunitaires, qui active à son tour AMPK et aide à faire passer les macrophages d’un mode d’attaque néfaste à un mode plus paisible et axé sur la réparation. Bien que le travail ait été réalisé sur des cellules de souris en culture et doive encore être testé chez l’animal et l’homme, il met en lumière la voie métabolite microbien → GPR109a → AMPK comme une cible prometteuse pour atténuer l’inflammation dans l’hyperuricémie, pouvant compléter les traitements classiques abaissant l’acide urique par des stratégies plus ciblées d’apaisement immunitaire.
Citation: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
Mots-clés: hyperuricémie, microbiote intestinal, polarisation des macrophages, β-hydroxybutyrate, voie GPR109a AMPK