Clear Sky Science · pl
Oś GPR109a-AMPK pośredniczy w osłabieniu polaryzacji makrofagów M1 indukowanej przez kwas moczowy przez β-hydroksymaślan z Lacticaseibacillus rhamnosus M2b
Dlaczego mikroby jelitowe mają znaczenie dla bolących stawów
Osoby z wysokim poziomem kwasu moczowego we krwi często rozwijają bolesną dnę moczanową i inne problemy zapalne, podczas gdy obecne terapie koncentrują się głównie na obniżaniu kwasu moczowego, a nie na uspokajaniu wywołanego przez niego układu odpornościowego. To badanie bada, jak pożyteczna bakteria jelitowa i jeden z jej małych produktów chemicznych mogą łagodnie przesunąć komórki odpornościowe z szkodliwego, agresywnego stanu w kierunku łagodzącego, naprawczego stanu, oferując nowe podejście do łagodzenia stanów zapalnych związanych z wysokim poziomem kwasu moczowego.
Od wysokiego kwasu moczowego do pobudzonych komórek odpornościowych
Hiperurykemia, czyli wysoki poziom kwasu moczowego, staje się coraz częstsza na całym świecie i wiąże się nie tylko z dną moczanową, lecz także z szerszym przewlekłym stanem zapalnym. Kwas moczowy może skłaniać pewne białe krwinki zwane makrofagami do agresywnego stanu, w którym wydzielają one substancje zapalne uszkadzające okoliczne tkanki. Naukowcy wiedzą, że ten agresywny stan, często określany jako typ M1, odgrywa kluczową rolę w chorobie, ale terapie, które bezpiecznie i bezpośrednio kierują te komórki z powrotem do spokojniejszego, naprawczego stanu, są wciąż ograniczone.
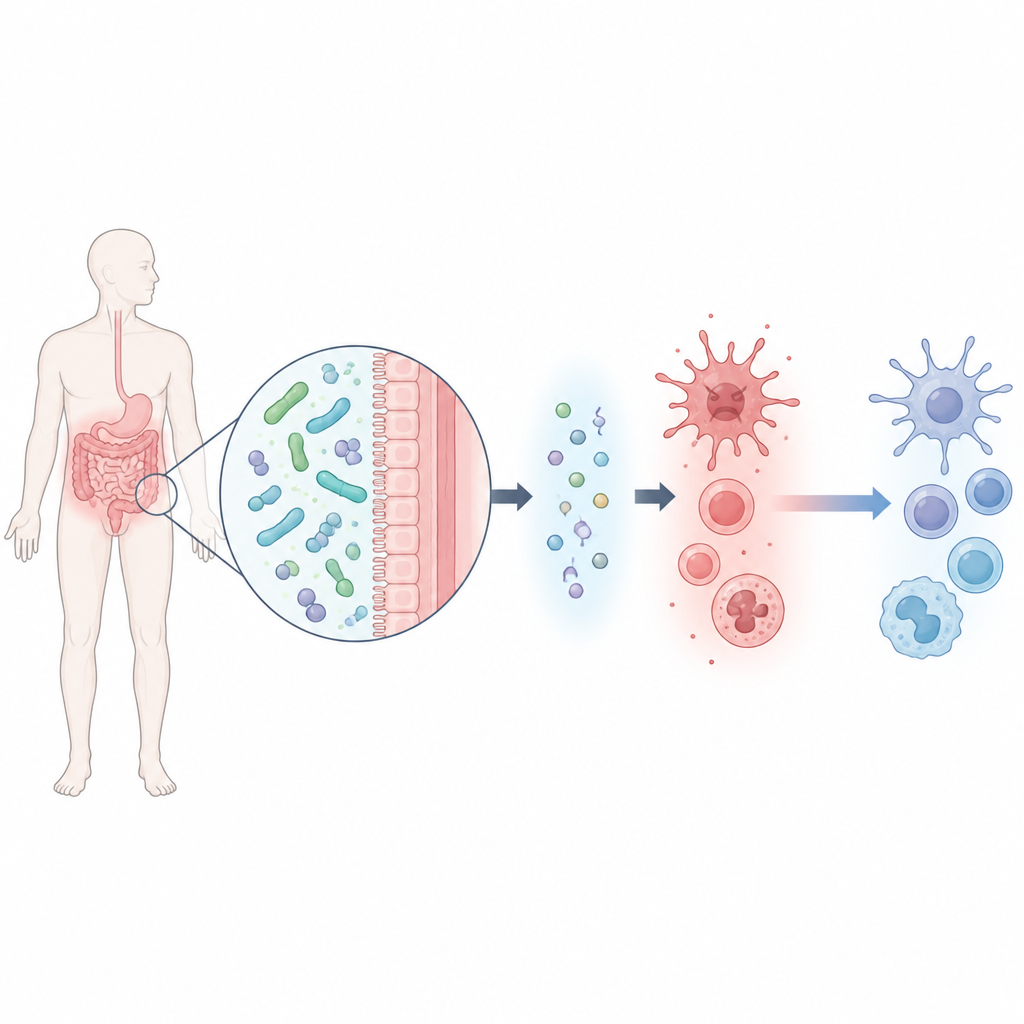
Pomocny mikroorganizm jelitowy i mały sygnał chemiczny
Zespół rozpoczął od wyizolowania szczepu Lacticaseibacillus rhamnosus, nazwanego M2b, ze stolca zdrowych mężczyzn o niskim poziomie kwasu moczowego. Bakteria ta znakomicie rozkładała kwas moczowy w warunkach laboratoryjnych. Korzystając z szerokiego przeglądu produktów chemicznych uwalnianych przez mikroba, naukowcy zidentyfikowali sześć kandydatów i przetestowali, które z nich mogą chronić mysie komórki makrofagów zestresowane kwasem moczowym. Jedna cząsteczka, nazwana beta-hydroksymaślanem, wyróżniła się: nie tylko poprawiała przeżywalność komórek, lecz także zdecydowanie zmniejszała poziomy kilku kluczowych substancji zapalnych, jednocześnie zwiększając sygnał przeciwzapalny o nazwie IL-10.
Zmiana komórek atakujących w komórki naprawcze
Aby sprawdzić, jak ta mała cząsteczka zmienia zachowanie odpornościowe, badacze wystawili makrofagi na działanie samego kwasu moczowego lub razem z beta-hydroksymaślanem albo z płynem pobranym z hodowli M2b. Sam kwas moczowy wprowadzał komórki w klasyczną postawę ataku, z wysokimi poziomami markerów związanych ze stanem M1 i niskimi poziomami markerów związanych ze stanem bardziej uspokajającym, przypominającym M2. Gdy dodano beta-hydroksymaślan lub płyn z hodowli bakterii, te wzorce się odwróciły: markery ataku spadły, markery naprawcze wzrosły, a kształt komórek pod mikroskopem przesunął się w stronę spokojniejszego wyglądu. To pokazało, że metabolit produkowany przez bakterię jelitową może bezpośrednio przechylić makrofagi z dala od szkodliwej reakcji.
Przełącznik receptora i czujnik energetyczny wewnątrz komórki
Historia nie zakończyła się na obserwowaniu tych zmian; naukowcy chcieli dowiedzieć się, jak do nich dochodzi. Skoncentrowali się na białku na powierzchni makrofagów znanym jako GPR109a, które może wyczuwać cząsteczki podobne do beta-hydroksymaślanu. Modelowanie komputerowe sugerowało, że beta-hydroksymaślan dobrze pasuje do tego receptora. Eksperymenty potwierdziły, że kwas moczowy obniżał poziomy GPR109a, podczas gdy beta-hydroksymaślan i hodowla M2b przywracały je. Gdy badacze celowo zmniejszyli ilość GPR109a w komórkach, beta-hydroksymaślan stracił swoje uspokajające działanie. Gdy zwiększyli ekspresję GPR109a, komórki naturalnie przeszły w stan naprawczy, nawet pod wpływem stresu wywołanego kwasem moczowym.
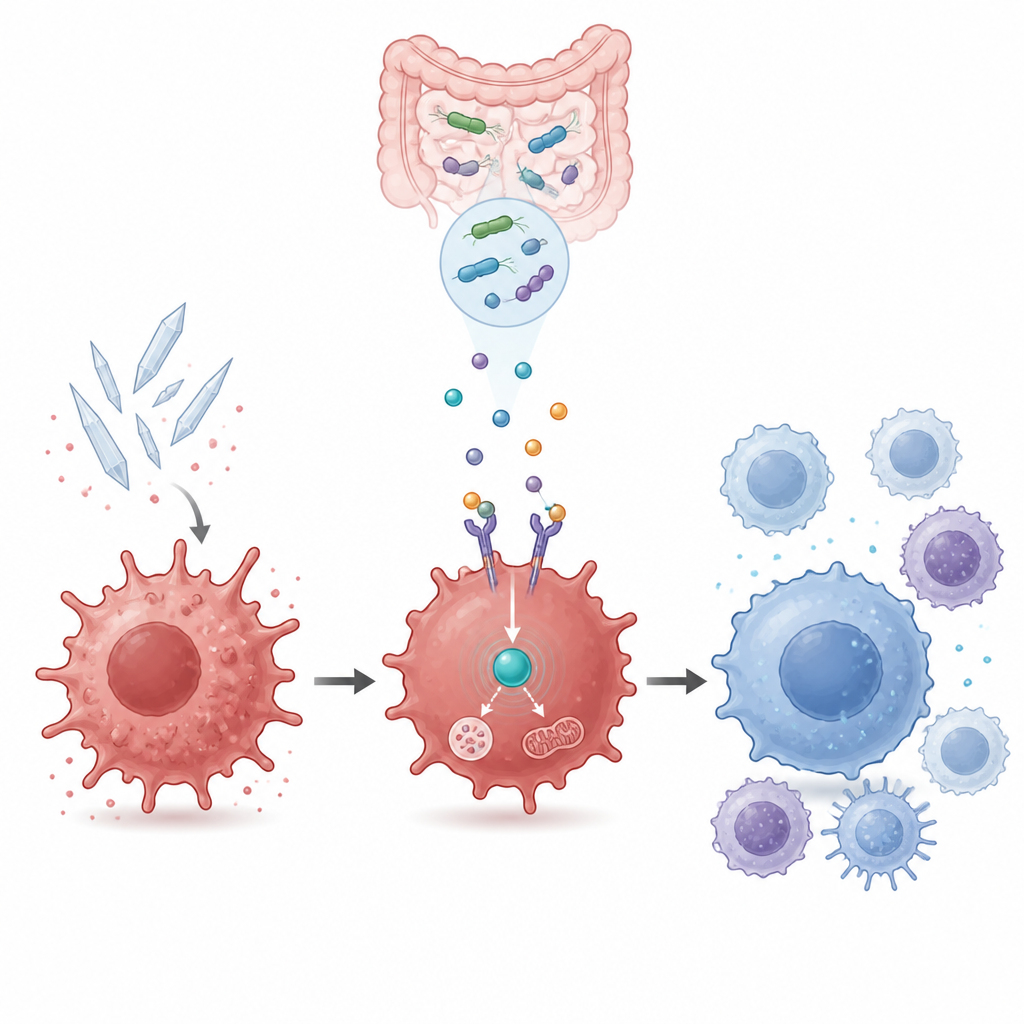
Powiązanie zużycia energii komórkowej z kontrolą zapalenia
Wewnątrz komórki GPR109a łączy się z innym kluczowym graczem zwanym AMPK, czujnikiem statusu energetycznego komórki. Pomiary aktywności genów i testy białkowe wykazały, że kwas moczowy przytępiał aktywność AMPK, podczas gdy beta-hydroksymaślan ożywiał ją w sposób zależny od GPR109a. Zablokowanie AMPK za pomocą chemicznego inhibitora usuwało korzyści płynące z beta-hydroksymaślanu i hodowli M2b: markery zapalne znów narastały, a markery naprawcze malały. To powiązało uspokajającą zmianę układu odpornościowego z wewnętrznym obwodem wykrywającym energię, który musi pozostać aktywny, aby metabolit bakteryjny mógł działać.
Co to może znaczyć dla osób z wysokim poziomem kwasu moczowego
Podsumowując, wyniki rysują prosty ciąg zdarzeń: bakteria jelitowa produkuje beta-hydroksymaślan, ta mała cząsteczka aktywuje receptor GPR109a na komórkach odpornościowych, co z kolei włącza AMPK i pomaga przesunąć makrofagi ze szkodliwego trybu ataku w bardziej pokojowy, naprawczy tryb. Choć badania przeprowadzono na hodowlach mysich komórek i wciąż wymagają testów na zwierzętach i ludziach, wskazują one na szlak metabolit bakteryjny → GPR109a → AMPK jako obiecujący cel łagodzenia zapalenia w hiperurykemii, potencjalnie uzupełniający standardowe leki obniżające kwas moczowy o precyzyjniejsze strategie uspokajania układu odpornościowego.
Cytowanie: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
Słowa kluczowe: hiperurykemia, mikrobiota jelitowa, polaryzacja makrofagów, beta-hydroksymaślan, szlak GPR109a AMPK