Clear Sky Science · de
GPR109a-AMPK-Achse vermittelt die Abschwächung der durch Harnsäure induzierten M1-Makrophagenpolarisation durch β-Hydroxybutyrat von Lacticaseibacillus rhamnosus M2b
Warum Darmbakterien für schmerzende Gelenke wichtig sind
Menschen mit erhöhtem Harnsäurespiegel im Blut entwickeln häufig schmerzhafte Gicht und andere entzündliche Beschwerden. Aktuelle Therapien konzentrieren sich jedoch meist darauf, die Harnsäure zu senken, statt das von ihr gereizte Immunsystem zu beruhigen. Diese Studie untersucht, wie ein hilfreiches Darmbakterium und eines seiner kleinen chemischen Produkte Immunzellen sanft von einem schädlichen Angriffsmodus hin zu einem beruhigenden Reparaturmodus lenken können und damit einen neuen Ansatz zur Linderung harnsäurebedingter Entzündungen bieten.
Von hoher Harnsäure zu aktiven Immunzellen
Hyperurikämie, also ein hoher Harnsäurespiegel, nimmt weltweit zu und ist nicht nur mit Gicht, sondern auch mit chronischen Entzündungen assoziiert. Harnsäure kann bestimmte weiße Blutzellen, so genannte Makrophagen, in einen aggressiven Zustand drängen, in dem sie entzündungsfördernde Stoffe ausschütten und umliegendes Gewebe schädigen. Forschende wissen, dass dieser aggressive Zustand, oft als M1-Typ bezeichnet, eine zentrale Rolle bei Erkrankungen spielt, doch direkte und sichere Therapien, die diese Zellen wieder in einen ruhigeren, heilungsfördernden Zustand steuern, sind noch begrenzt.
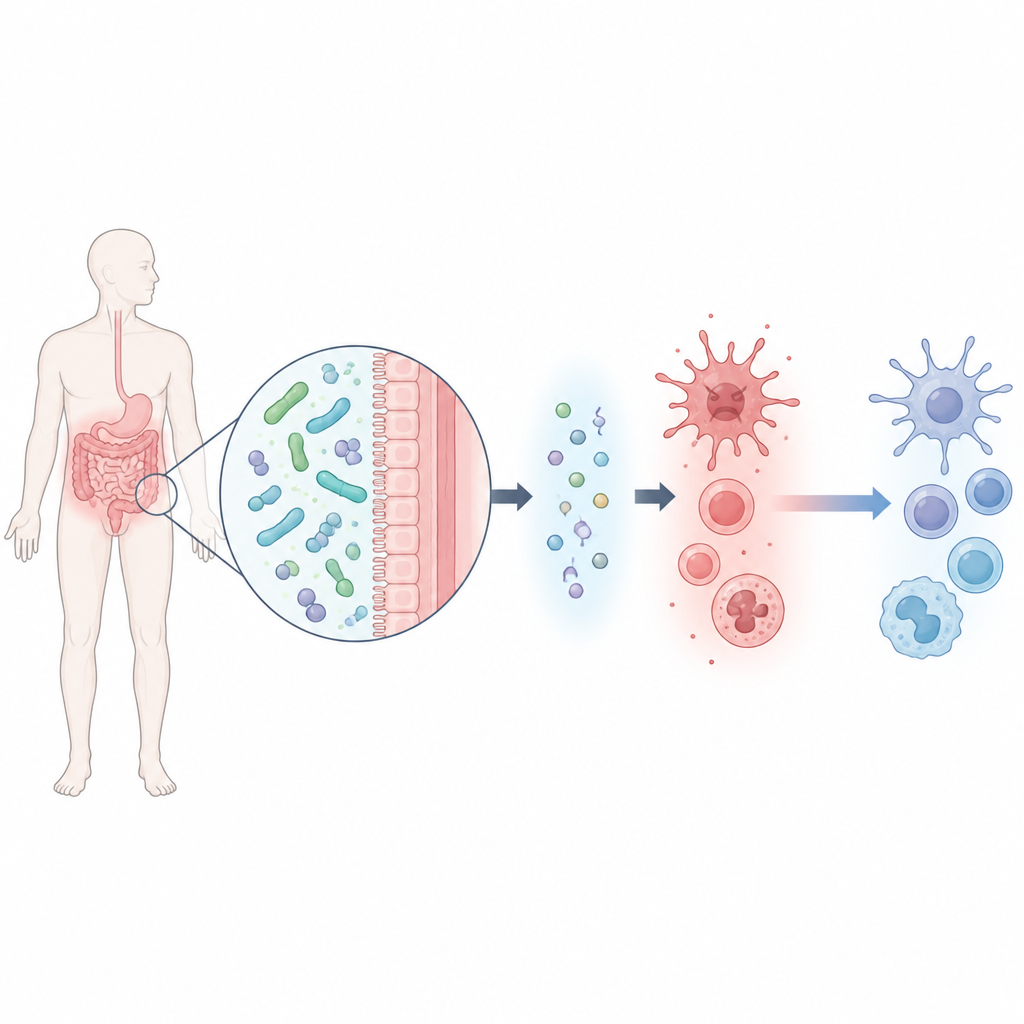
Ein hilfreiches Darmmikroben und ein kleines Signalsignal
Das Team isolierte eine Stamme von Lacticaseibacillus rhamnosus, genannt M2b, aus Stuhlproben gesunder Männer mit niedrigen Harnsäurewerten. Dieses Bakterium war im Labor besonders effektiv beim Abbau von Harnsäure. Mithilfe einer umfassenden Analyse der vom Mikroben freigesetzten Stoffwechselprodukte identifizierten die Wissenschaftler sechs Kandidatenmoleküle und prüften, welche davon Mäusemakrophagen, die durch Harnsäure belastet waren, schützen konnten. Ein Molekül, Beta-Hydroxybutyrat, stach hervor: Es verbesserte nicht nur das Überleben der Zellen, sondern reduzierte auch deutlich mehrere zentrale Entzündungsfaktoren und steigerte ein anti-entzündliches Signal namens IL-10.
Angriffszellen in Heilungszellen verwandeln
Um zu beobachten, wie dieses kleine Molekül das Immunverhalten veränderte, setzten die Forschenden Makrophagen entweder nur Harnsäure oder Harnsäure zusammen mit Beta-Hydroxybutyrat bzw. mit dem Kulturüberstand von M2b aus. Harnsäure allein trieb die Zellen in eine klassische Angriffsstellung: hohe Werte für Marker, die mit dem M1-Zustand assoziiert sind, und niedrige Werte für Marker, die zu einem beruhigenderen, M2-ähnlichen Zustand gehören. Mit Zugabe von Beta-Hydroxybutyrat oder dem bakteriellen Kulturüberstand kehrten sich diese Muster um: die Angriffsmarker sanken, die Heilungsmarker stiegen, und die Zellmorphologie unter dem Mikroskop nahm ein ruhigeres Erscheinungsbild an. Das zeigte, dass ein vom Darmbakterium hergestelltes Metabolit Makrophagen direkt von einer schädlichen Reaktion wegkanten kann.
Ein Rezeptorschalter und ein Energiesensor im Inneren der Zelle
Die Geschichte endete nicht bei der Beobachtung dieser Veränderungen; die Wissenschaftler wollten wissen, wie sie zustande kamen. Sie konzentrierten sich auf ein Protein an der Makrophagenoberfläche, bekannt als GPR109a, das Moleküle wie Beta-Hydroxybutyrat wahrnehmen kann. Rechnerische Modellierung deutete darauf hin, dass Beta-Hydroxybutyrat gut in diesen Rezeptor passt. Experimente bestätigten, dass Harnsäure die GPR109a-Spiegel senkte, während Beta-Hydroxybutyrat und der M2b-Kulturüberstand sie wiederherstellten. Wenn die Forschenden GPR109a gezielt in den Zellen reduzierten, verlor Beta-Hydroxybutyrat seine beruhigenden Effekte. Beim Hochregulieren von GPR109a verschoben sich die Zellen von sich aus in den Heilungszustand, selbst unter Harnsäurestress.
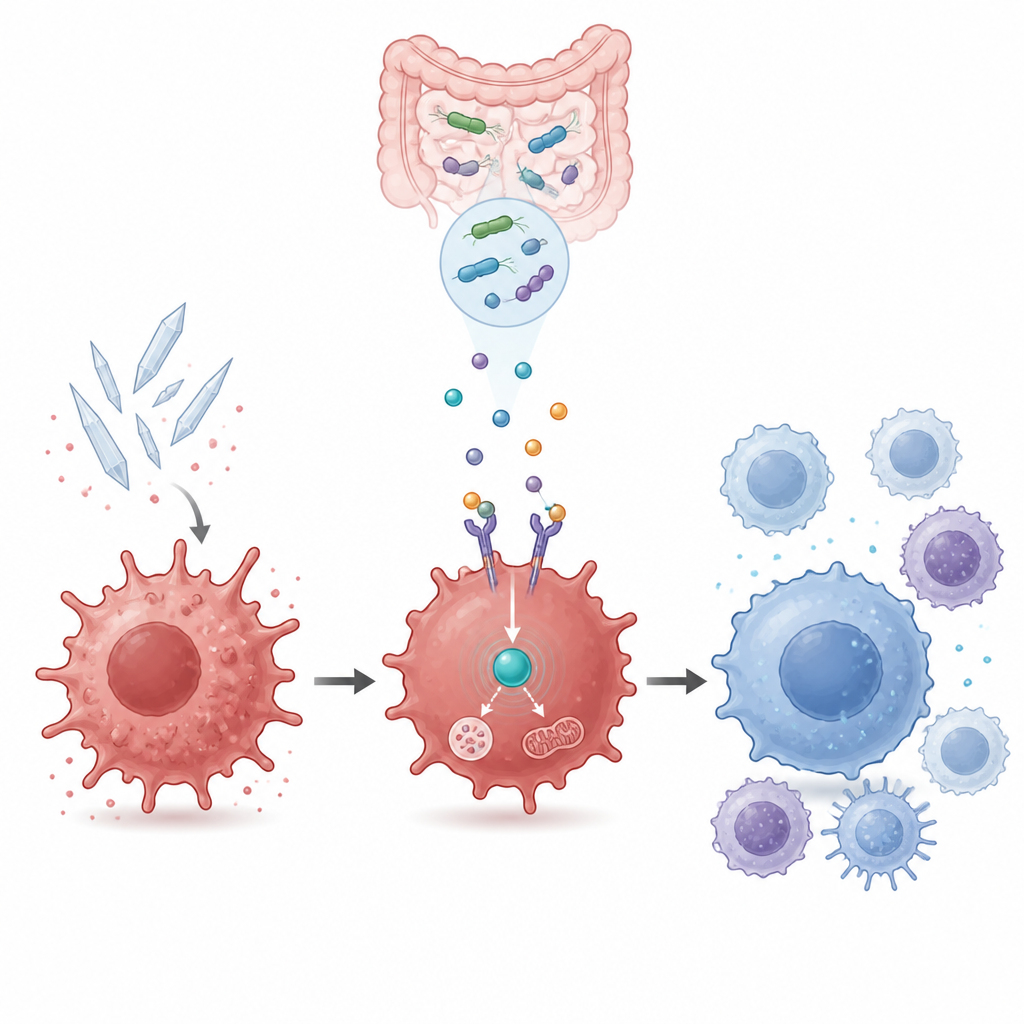
Energieverbrauch der Zelle mit Entzündungskontrolle verknüpfen
Im Inneren der Zelle steht GPR109a mit einem weiteren wichtigen Akteur in Verbindung: AMPK, einem Sensor für den Energiestatus der Zelle. Genexpressionsmessungen und Proteintests zeigten, dass Harnsäure die AMPK-Aktivität dämpfte, während Beta-Hydroxybutyrat sie auf eine Weise wiederbelebte, die von GPR109a abhängt. Die Blockade von AMPK mit einem chemischen Inhibitor beseitigte die Vorteile von Beta-Hydroxybutyrat und dem M2b-Kulturüberstand: Entzündungsmarker schossen wieder in die Höhe und Heilungsmarker gingen zurück. Damit koppeln die Forschenden die beruhigende Immunverschiebung an einen internen Energiesensor, der aktiv sein muss, damit das bakteriell erzeugte Metabolit wirkt.
Was das für Menschen mit hohem Harnsäurespiegel bedeuten könnte
Insgesamt skizzieren die Ergebnisse eine einfache Abfolge: Ein Darmbakterium produziert Beta-Hydroxybutyrat, dieses kleine Molekül aktiviert den GPR109a-Rezeptor auf Immunzellen, der wiederum AMPK einschaltet und Makrophagen vom schädlichen Angriffsmodus in einen friedlicheren, reparaturorientierten Zustand versetzt. Obwohl die Arbeit an kultivierten Maus-Zellen durchgeführt wurde und noch Tierversuche und Studien am Menschen erfordert, deutet sie den GPR109a-AMPK-Weg, vermittelt durch ein Mikrobiom-Metabolit, als vielversprechendes Ziel an, um Entzündungen bei Hyperurikämie zu lindern und möglicherweise die Standardtherapien zur Senkung der Harnsäure durch gezieltere immunberuhigende Strategien zu ergänzen.
Zitation: Du, M., He, Y., Zhu, Y. et al. GPR109a-AMPK axis mediates the Attenuation of uric acid-induced M1 macrophage polarization by β-hydroxybutyrate from Lacticaseibacillus rhamnosus M2b. Sci Rep 16, 14955 (2026). https://doi.org/10.1038/s41598-026-39746-3
Schlüsselwörter: Hyperurikämie, Darmmikrobiota, Makrophagenpolarisation, Beta-Hydroxybutyrat, GPR109a-AMPK-Weg