Clear Sky Science · zh
CAF富集的COL4A6在整体转录组呈逆相关的同时促进胃癌进展与间质重塑
为何肿瘤周围环境很重要
大多数人把癌症视为失控细胞的疾病,但这项研究表明肿瘤周围的“土壤”可能与癌细胞本身一样重要。在胃癌中,包围肿瘤的组织支架和支持细胞既可能抑制疾病,也可能促使其生长、转移并抗药。该研究揭示了一种特定支架蛋白COL4A6在不同部位表现出截然不同的行为,以及一类特定的支持细胞——与癌症相关的成纤维细胞(CAF)如何将该蛋白转变为促进肿瘤进展的重要同谋。
细看肿瘤“邻里”
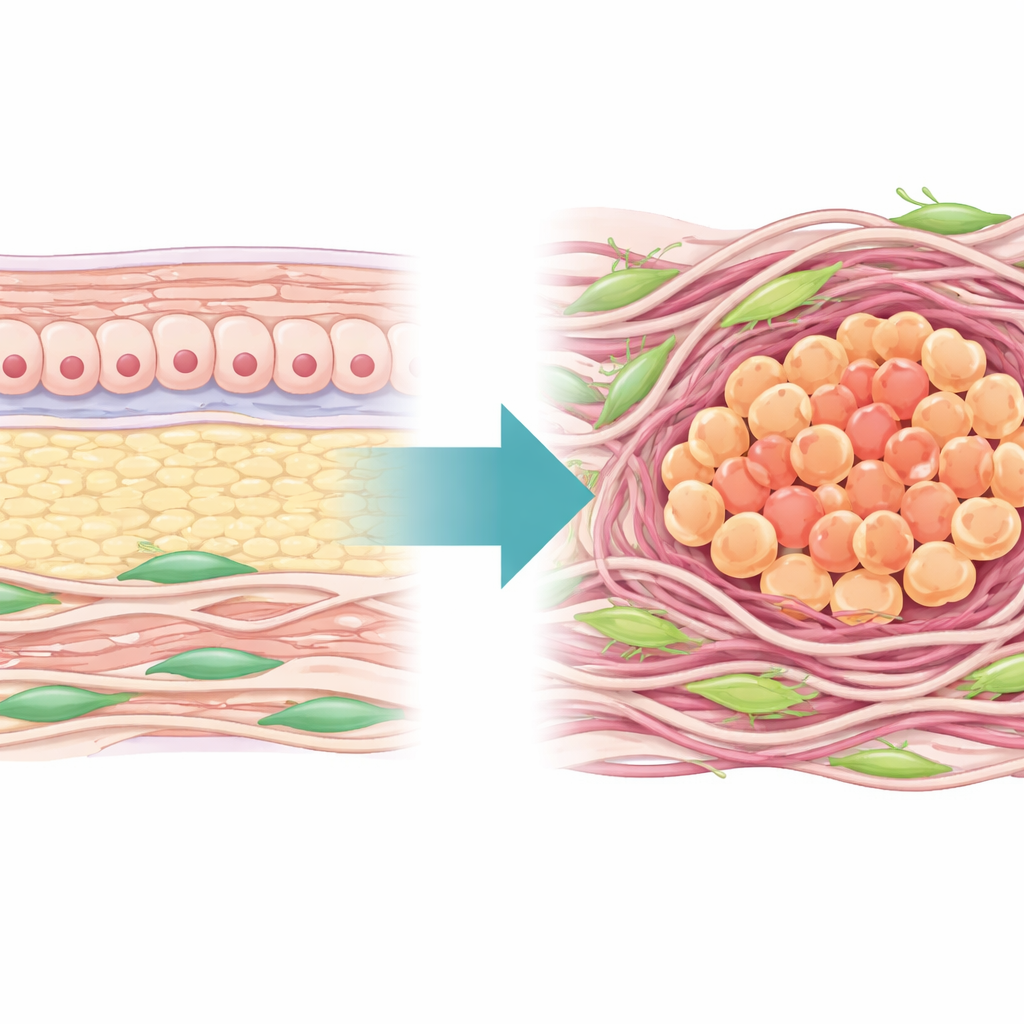
作者首先绘制了数百例人类胃肿瘤中细胞外基质的“地形”——围绕细胞的蛋白与纤维网络。他们发现近一半的核心基质基因在癌组织中相较于邻近正常组织发生了改变,证实胃肿瘤的物理环境被大幅重塑。基于这些基因,他们构建了一个基质风险评分(Matrisome Risk Score),该评分能够可靠地区分肿瘤与正常组织,并将患者分为两类:一类具有致密、高度重塑的基质且生存较差,另一类则基质较松散、预后较好。高基质组还表现出免疫“冷”肿瘤的特征,抑制性细胞增多、活跃的T细胞较少,并且对标准化疗的敏感性降低。
一个性格分裂的蛋白
在众多基质成分中,COL4A6尤为引人注意:在仅观察整块肿瘤样本的整体基因读数时,它似乎表现为一种“保护性”因子。从统计上看,这些整体数据中较高的COL4A6基因水平与较低的表观风险相关,这曾让一些人怀疑它可能有助于抑制癌症。但本研究怀疑存在隐藏的转折:整体测量混合了多种细胞类型的信号。当团队检查患者的实际肿瘤切片时,发现COL4A6蛋白在癌组织中实际上显著增加,且随着肿瘤进展,胶原纤维变得更粗、更丰富。
成纤维细胞是被隐藏的驱动者
通过荧光成像和单细胞测序,研究者确定了COL4A6的真正来源。它并非来自癌细胞本身,而主要来源于一类位于肿瘤结缔组织中的支持细胞——与癌症相关的成纤维细胞(CAF)。COL4A6的信号与CAF标志物高度重叠,表明这些成纤维细胞是主要来源。这解释了早先的混淆:癌性上皮细胞在基因水平上可能丧失COL4A6表达,但成纤维细胞群体增强产量并将蛋白沉积到周围基质中,而整体测定会把这些不同来源混合在一起。
COL4A6如何助长生长与转移
为测试CAF来源的COL4A6对肿瘤的影响,研究团队将胃癌细胞与被工程化为过表达或下调COL4A6的成纤维细胞培养在一起。当成纤维细胞过度产生COL4A6时,邻近的癌细胞变得更具迁移性和侵袭性,并向一种更具侵略性、具有形态可塑性的表皮-间质转化(EMT)状态转变。在小鼠体内,携带COL4A6丰富成纤维细胞的肿瘤生长更大,胶原沉积更致密,且在间质中可见强烈的COL4A6信号。同时,COL4A6似乎也反作用于成纤维细胞本身,使其内部骨架重组为粗壮的应激纤维并提升经典的活化标志物。本质上,COL4A6帮助将成纤维细胞转变为强有力的重塑者,致使组织变硬、形成物理屏障,并创造一个支持肿瘤侵袭和药物抗性的生态位。
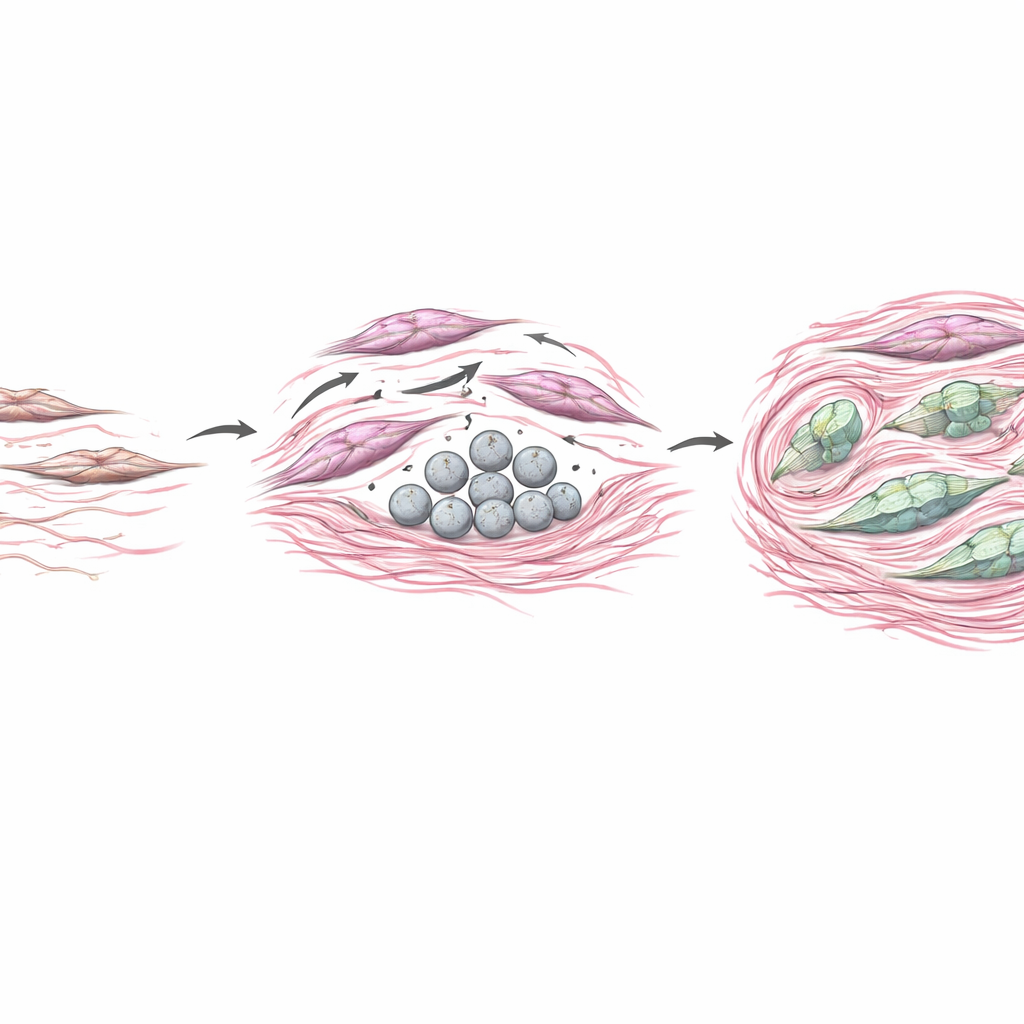
这对患者意味着什么
对非专业读者来说,主要信息是:同一种分子在不同测量方式和不同位置下可能看起来有利或有害。COL4A6在对所有肿瘤细胞取平均时可能显得“有保护作用”,但在正确的细胞区室中观察时,它会显现为由活化成纤维细胞产生、推动疾病的关键促进因子。通过定义基于基质的肿瘤亚型并揭示CAF–COL4A6轴作为免疫逃逸和化疗耐受的驱动因素,该研究为胃癌患者分层提供了新思路,并突出了肿瘤间质作为有前景的治疗靶点。未来干扰成纤维细胞中的COL4A6或软化周围基质的疗法,或有助于将冷性、耐药的胃肿瘤转变为对药物和免疫治疗更敏感的肿瘤。
引用: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
关键词: 胃癌, 肿瘤微环境, 与癌症相关的成纤维细胞, 细胞外基质, COL4A6