Clear Sky Science · pt
COL4A6 enriquecido por CAF promove progressão do câncer gástrico e remodelação do estroma apesar de uma associação inversa em transcriptomas de bloco
Por que o entorno do tumor importa
A maioria das pessoas pensa no câncer como uma doença de células desreguladas, mas este estudo mostra que o “solo” ao redor do tumor pode ser tão importante quanto as próprias células cancerosas. No câncer gástrico, o arcabouço tecidual e as células de suporte que cercam o tumor podem tanto retardar a doença quanto estimulá-la a crescer, disseminar-se e resistir ao tratamento. Esta pesquisa revela como uma proteína de suporte específica, chamada COL4A6, se comporta de maneiras muito diferentes dependendo de onde está localizada, e como um grupo específico de células de suporte, os fibroblastos associados ao câncer, pode transformar essa proteína em um poderoso cúmplice da progressão tumoral.
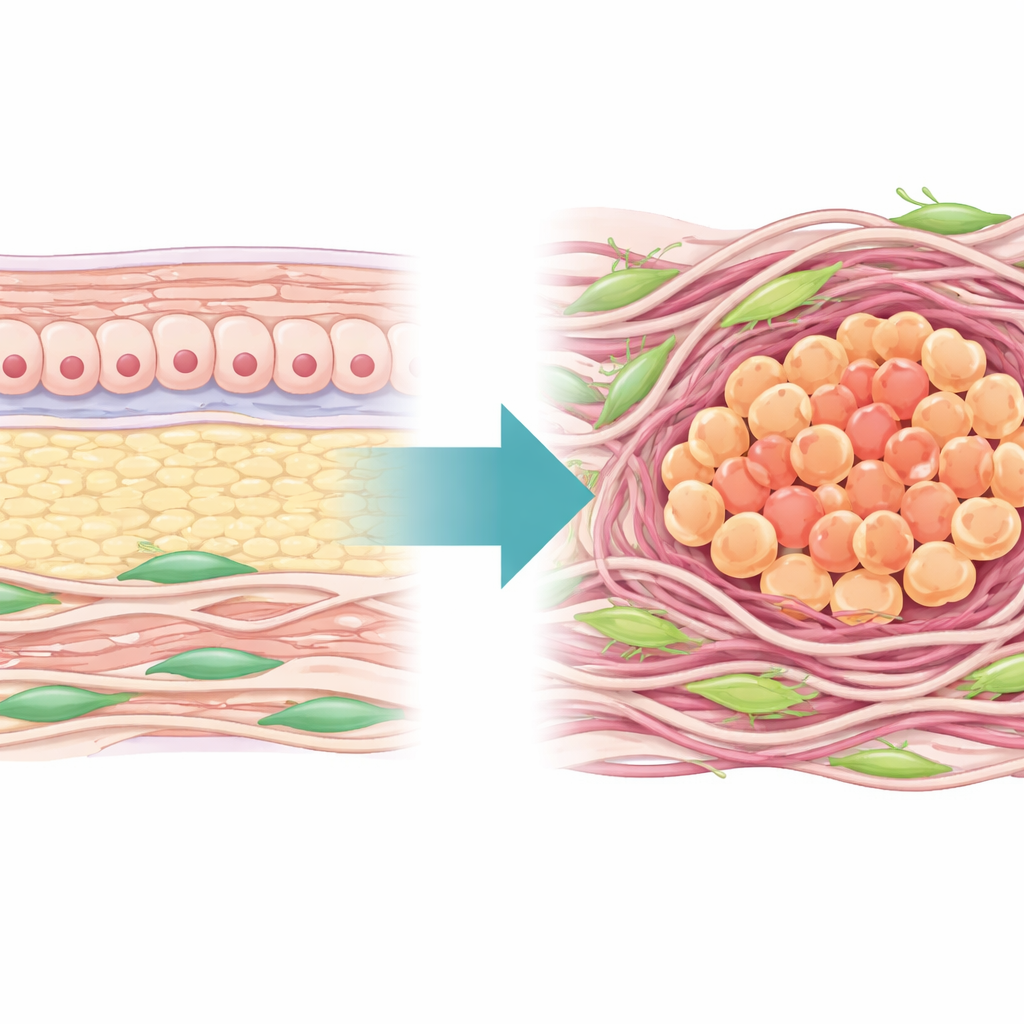
Um olhar mais atento ao bairro tumoral
Os autores começaram mapeando a “paisagem” da matriz extracelular — a rede de proteínas e fibras que envolve as células — em centenas de tumores gástricos humanos. Eles descobriram que quase metade dos genes centrais da matriz estavam alterados no tecido tumoral em comparação com o tecido normal adjacente, confirmando que o ambiente físico dos tumores gástricos é amplamente remodelado. Usando esses genes, construíram uma Pontuação de Risco da Matrisoma capaz de distinguir de forma confiável tumor de tecido normal e de separar os pacientes em dois grupos principais: um com matriz densa e fortemente remodelada e pior sobrevida, e outro com matriz mais frouxa e melhores desfechos. O grupo de alta matriz também mostrou sinais de tumor imunologicamente “frio”, com muitas células supressoras e poucas células T efetoras ativas, além de sensibilidade reduzida à quimioterapia padrão.
Uma proteína com dupla personalidade
Um componente da matriz, COL4A6, destacou-se porque parecia comportar-se como um fator “protetor” quando os pesquisadores analisaram apenas as leituras gênicas em bloco de amostras tumorais inteiras. Estatisticamente, níveis mais altos do gene COL4A6 nesses conjuntos de dados em bloco estavam associados a menor risco aparente, o que levou alguns a suspeitar que ele poderia ajudar a conter o câncer. Mas o estudo levantou uma reviravolta oculta: medições em bloco misturam sinais de muitos tipos celulares diferentes. Quando a equipe examinou cortes reais de tecido tumoral de pacientes, encontrou que a proteína COL4A6 estava, de fato, fortemente aumentada nos cânceres em comparação com o tecido gástrico normal, e que as fibras de colágeno tornavam-se mais espessas e abundantes à medida que os tumores progrediam.
Fibroblastos como motores ocultos
Usando imagem fluorescente e sequenciamento de célula única, os pesquisadores descobriram de onde o COL4A6 realmente vinha. Não eram as próprias células cancerosas, mas principalmente um tipo de célula de suporte chamado fibroblastos associados ao câncer, ou CAFs, alojados no tecido conjuntivo do tumor. Os sinais de COL4A6 se sobrepunham fortemente a um marcador de CAF, revelando que esses fibroblastos eram a principal fonte. Isso explicou a confusão anterior: enquanto as células epiteliais cancerosas podem perder expressão gênica de COL4A6, o compartimento de fibroblastos aumenta a produção e deposita a proteína na matriz ao redor — um padrão que os testes em bloco obscurecem.
Como o COL4A6 alimenta crescimento e disseminação
Para testar como o COL4A6 derivado de CAFs afeta os tumores, a equipe cultivou células de câncer gástrico junto com culturas de fibroblastos geneticamente modificadas para produzir mais COL4A6 ou menos dele. Quando os fibroblastos superproduziam COL4A6, as células cancerosas próximas tornaram-se mais móveis e invasivas, e transitaram para um estado mais agressivo e plásticos conhecido como transição epitélio–mesênquima. Em camundongos, tumores formados com fibroblastos ricos em COL4A6 cresceram mais, apresentaram depósitos de colágeno mais densos e mostraram sinais fortes de COL4A6 entrelaçados no estroma. Ao mesmo tempo, o COL4A6 pareceu agir sobre os próprios fibroblastos, reorganizando seu arcabouço interno em fibras de tensão espessas e aumentando marcadores clássicos de ativação. Em essência, o COL4A6 ajudou a converter os fibroblastos em remodeladores potentes que rigidificam o tecido, constroem barreiras físicas e criam um nicho que favorece a invasão tumoral e a resistência a drogas.
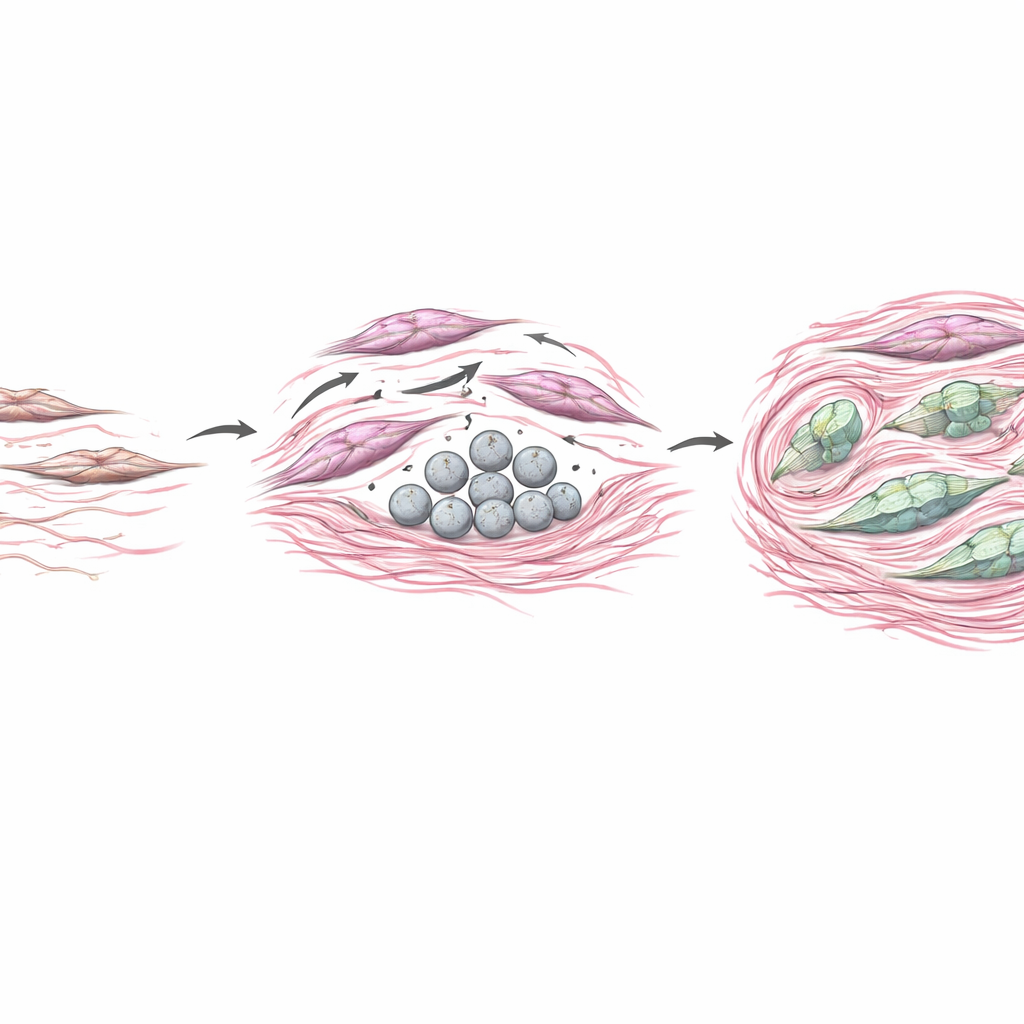
O que isso significa para os pacientes
Para não especialistas, a mensagem principal é que a mesma molécula pode parecer útil ou nociva dependendo de como e onde é medida. O COL4A6 pode parecer “protetor” quando é feito um balanço entre todas as células de um tumor, mas quando observado no compartimento correto emerge como um promotor chave da doença, produzido por fibroblastos ativados que constroem um ambiente denso e hostil. Ao definir subtipos tumorais baseados na matriz e expor esse eixo CAF–COL4A6 como motor da evasão imune e da resistência à quimioterapia, o estudo sugere novas maneiras de estratificar pacientes com câncer gástrico e destaca o estroma tumoral como um alvo promissor. Terapias que interrompam o COL4A6 nos fibroblastos ou amoleçam a matriz ao redor podem, um dia, ajudar a transformar tumores gástricos frios e resistentes em tumores mais responsivos a medicamentos e imunoterapia.
Citação: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
Palavras-chave: câncer gástrico, microambiente tumoral, fibroblastos associados ao câncer, matriz extracelular, COL4A6