Clear Sky Science · es
COL4A6 enriquecido por CAF promueve la progresión del cáncer gástrico y la remodelación estromal pese a una asociación inversa en transcriptomas totales
Por qué importan los alrededores del tumor
La mayoría de la gente piensa en el cáncer como una enfermedad de células descontroladas, pero este estudio muestra que el “suelo” que rodea al tumor puede ser tan importante como las propias células cancerosas. En el cáncer gástrico, el andamiaje tisular y las células de soporte que rodean el tumor pueden frenar la enfermedad o favorecer su crecimiento, diseminación y resistencia al tratamiento. Esta investigación revela cómo una proteína de la matriz en particular, llamada COL4A6, se comporta de forma muy distinta según su localización, y cómo un grupo específico de células de soporte, los fibroblastos asociados al cáncer, puede convertir esta proteína en una poderosa cómplice de la progresión tumoral.
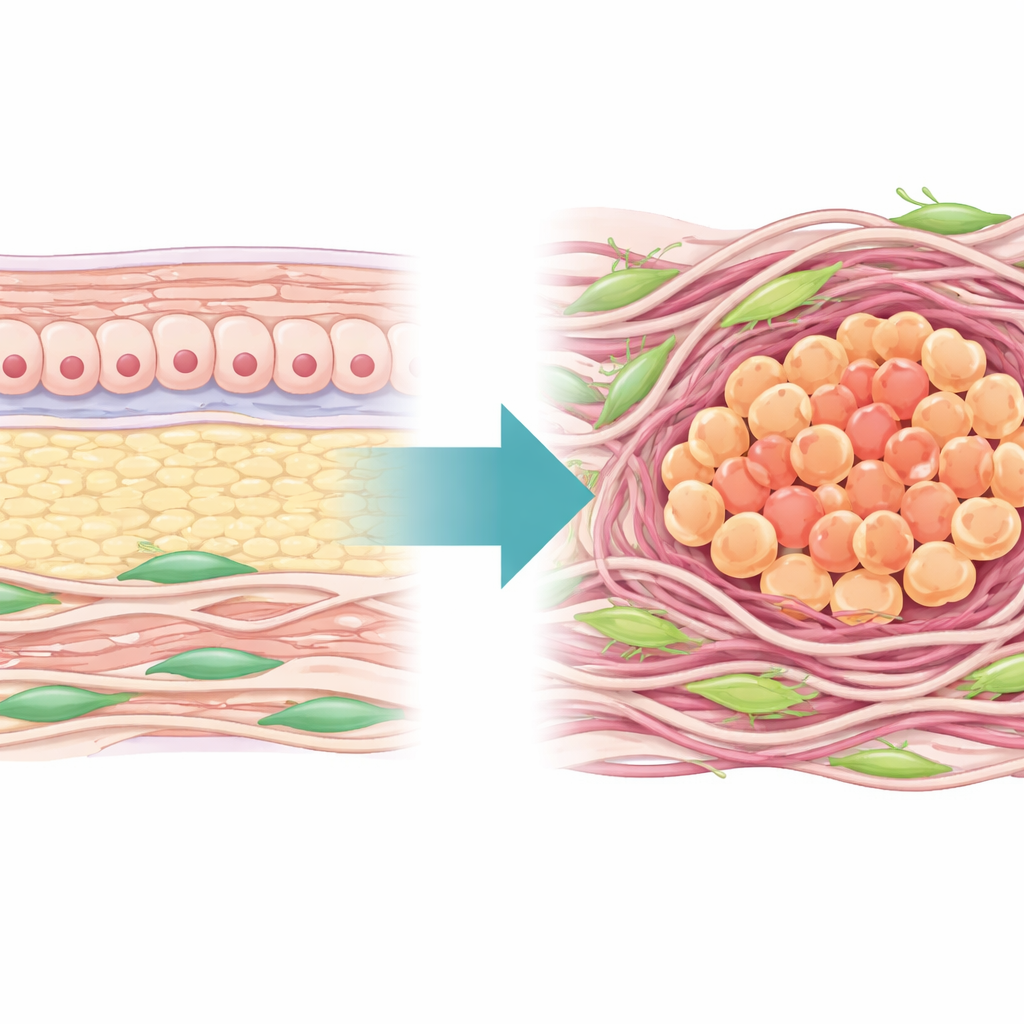
Una mirada más cercana al vecindario tumoral
Los autores empezaron mapeando el “paisaje” de la matriz extracelular—la malla de proteínas y fibras que rodea a las células—en cientos de tumores gástricos humanos. Encontraron que casi la mitad de los genes clave de la matriz estaban alterados en tejido canceroso en comparación con el tejido normal adyacente, lo que confirma que el entorno físico de los tumores gástricos está ampliamente remodelado. Con esos genes construyeron una Puntuación de Riesgo de Matrisoma capaz de distinguir de manera fiable tumor de tejido normal y de separar a los pacientes en dos grupos principales: uno con una matriz densa y muy remodelada y peor supervivencia, y otro con una matriz más laxa y mejores resultados. El grupo de alta matriz también mostraba rasgos de tumor “frío” inmunológicamente, con muchas células supresoras y pocas células T efectivas, además de menor sensibilidad a la quimioterapia estándar.
Una proteína con personalidad dividida
Un componente de la matriz, COL4A6, destacó porque parecía comportarse como un factor “protector” cuando los investigadores observaron únicamente lecturas génicas a nivel global de muestras tumorales completas. Estadísticamente, niveles más altos del gen COL4A6 en esos conjuntos de datos agregados se asociaban con un menor riesgo aparente, lo que llevó a algunos a sospechar que podría ayudar a frenar el cáncer. Pero este estudio planteó un giro oculto: las mediciones en conjunto mezclan señales de muchos tipos celulares. Cuando el equipo examinó cortes reales de tejido tumoral de pacientes, encontraron que la proteína COL4A6 estaba, de hecho, fuertemente aumentada en los cánceres en comparación con el tejido gástrico normal, y que las fibras de colágeno se volvían más gruesas y abundantes a medida que avanzaba el tumor.
Los fibroblastos como impulsores ocultos
Mediante imagen fluorescente y secuenciación unicelular, los investigadores localizaron la verdadera fuente de COL4A6. No eran las células cancerosas en sí, sino principalmente un tipo de células de soporte llamadas fibroblastos asociados al cáncer (CAF), situadas en el tejido conectivo del tumor. Las señales de COL4A6 se solapaban estrechamente con un marcador de CAF, revelando que estos fibroblastos eran la fuente principal. Esto explicó la confusión previa: mientras las células epiteliales cancerosas pueden perder expresión de COL4A6 a nivel génico, el compartimento de fibroblastos aumenta la producción y deposita la proteína en la matriz circundante, un patrón que las pruebas globales diluyen.
Cómo COL4A6 alimenta el crecimiento y la diseminación
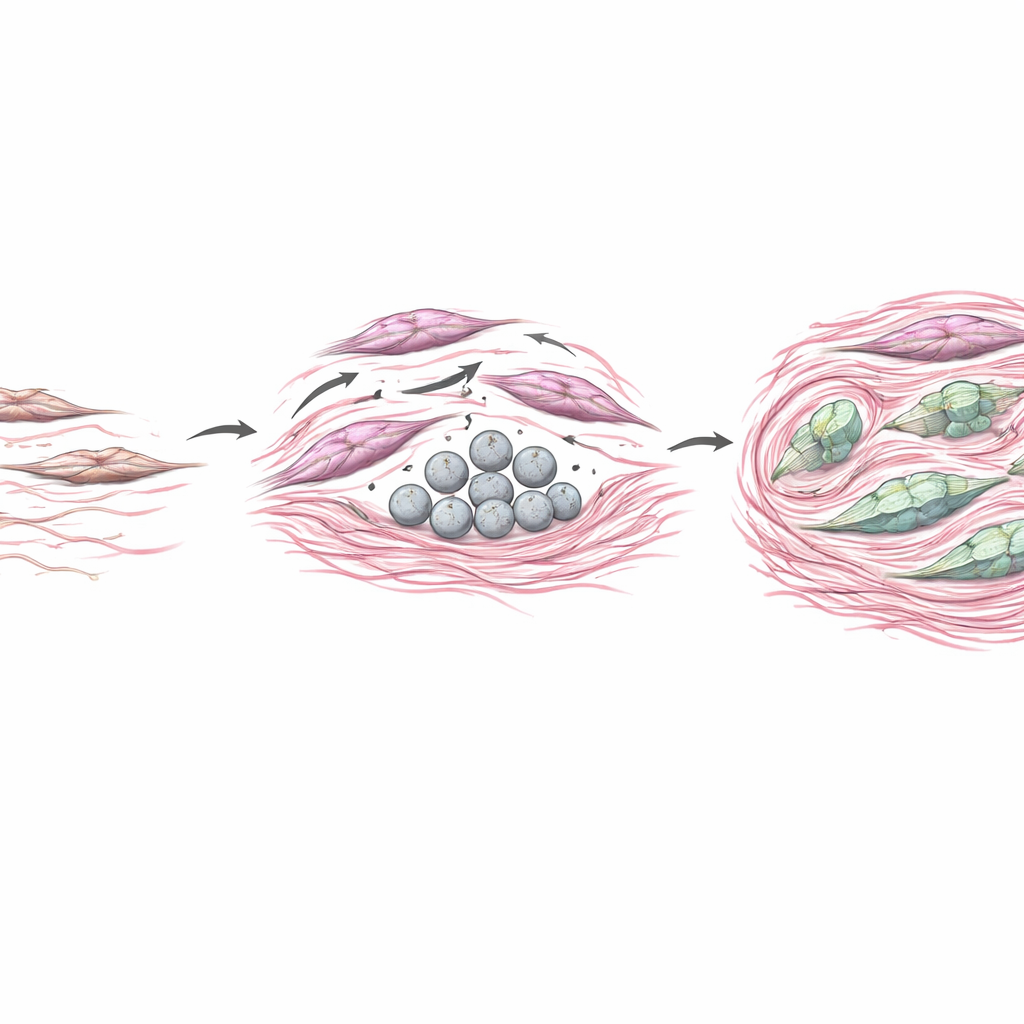
Para probar cómo el COL4A6 derivado de CAF afecta a los tumores, el equipo cultivó células de cáncer gástrico junto con cultivos de fibroblastos modificados para producir más COL4A6 o menos. Cuando los fibroblastos sobreproducían COL4A6, las células cancerosas cercanas se volvían más móviles e invasivas, y adquirían un estado más agresivo y cambiante conocido como transición epitelio‑mesénquima. En ratones, los tumores formados con fibroblastos ricos en COL4A6 crecieron más, tuvieron depósitos de colágeno más densos y mostraron señales intensas de COL4A6 integradas en el estroma. Al mismo tiempo, COL4A6 parecía actuar sobre los propios fibroblastos, reorganizando su andamiaje interno en gruesas fibras de tensión y potenciando marcadores clásicos de activación. En esencia, COL4A6 ayudó a convertir a los fibroblastos en remodeladores potentes que endurecen el tejido, construyen barreras físicas y crean un nicho que favorece la invasión tumoral y la resistencia a fármacos.
Qué significa esto para los pacientes
Para quienes no son especialistas, el mensaje principal es que la misma molécula puede parecer útil o dañina según cómo y dónde se mida. COL4A6 puede parecer “protectora” cuando se promedia entre todas las células de un tumor, pero al observarla en el compartimento adecuado emerge como un promotor clave de la enfermedad, producido por fibroblastos activados que construyen un entorno denso y hostil. Al definir subtipos tumorales basados en la matriz y revelar este eje CAF–COL4A6 como impulsor de la evasión inmune y la resistencia a la quimioterapia, el estudio sugiere nuevas formas de estratificar a pacientes con cáncer gástrico y destaca el estroma tumoral como un objetivo prometedor. Terapias que interrumpan COL4A6 en fibroblastos o ablanden la matriz circundante podrían algún día ayudar a convertir tumores gástricos fríos y resistentes en tumores más susceptibles a fármacos e inmunoterapia.
Cita: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
Palabras clave: cáncer gástrico, microambiente tumoral, fibroblastos asociados al cáncer, matriz extracelular, COL4A6