Clear Sky Science · fr
COL4A6 enrichi par les CAF favorise la progression du cancer gastrique et le remodelage du stroma malgré une association inverse dans les transcriptomes en masse
Pourquoi l’environnement du tumeur compte
La plupart des gens considèrent le cancer comme une maladie de cellules devenues rebelles, mais cette étude montre que le « sol » autour de la tumeur peut être aussi important que les cellules tumorales elles‑mêmes. Dans le cancer gastrique, l’armature tissulaire et les cellules de soutien entourant la tumeur peuvent soit ralentir la maladie, soit la pousser à croître, se propager et résister aux traitements. Cette recherche révèle comment une protéine matricielle particulière, appelée COL4A6, se comporte de façon très différente selon son emplacement, et comment un groupe spécifique de cellules de soutien, les fibroblastes associés au cancer, peut transformer cette protéine en un puissant complice de la progression tumorale.
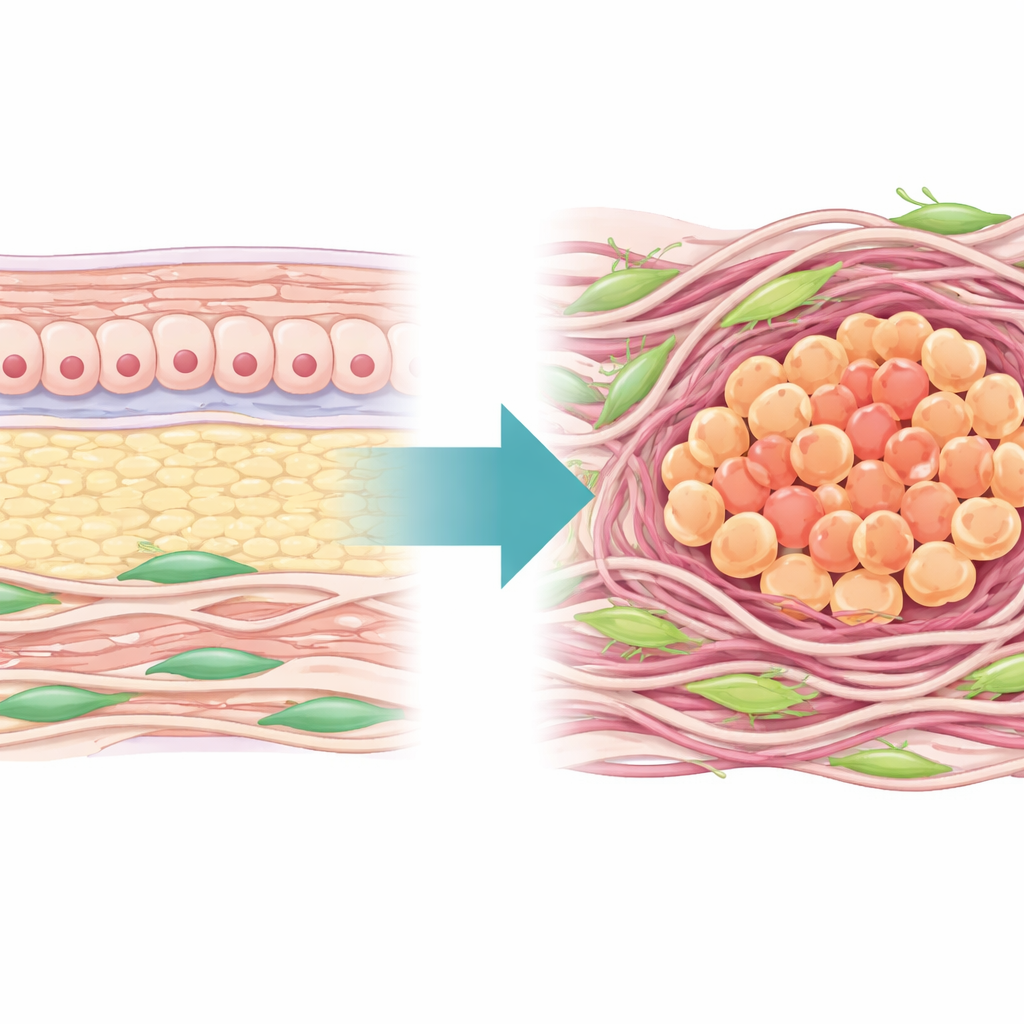
Un regard plus attentif sur le voisinage tumoral
Les auteurs ont commencé par cartographier le « paysage » de la matrice extracellulaire — le réseau de protéines et de fibres qui entoure les cellules — dans des centaines de tumeurs gastriques humaines. Ils ont constaté que près de la moitié des gènes matriciels principaux étaient modifiés dans le tissu cancéreux comparé au tissu normal adjacent, confirmant que l’environnement physique des tumeurs gastriques est largement remodelé. À partir de ces gènes, ils ont construit un score de risque matrisome capable de distinguer de façon fiable la tumeur du tissu normal et de répartir les patients en deux groupes principaux : l’un avec une matrice dense et fortement remodelée et une survie plus mauvaise, l’autre avec une matrice plus lâche et de meilleurs résultats. Le groupe à matrice élevée présentait également des signes d’une tumeur « froide » du point de vue immunitaire, avec de nombreuses cellules suppressives et peu de lymphocytes T effecteurs, ainsi qu’une moindre sensibilité aux chimiothérapies standard.
Une protéine à double visage
Un composant matriciel, COL4A6, s’est démarqué car il semblait se comporter comme un facteur « protecteur » lorsque les chercheurs n’examinaient que les lectures transcriptomiques en masse provenant d’échantillons tumoraux complets. Statistiquement, des niveaux plus élevés du gène COL4A6 dans ces jeux de données en masse étaient associés à un risque apparent plus faible, ce qui avait conduit certains à penser qu’il pouvait aider à freiner le cancer. Mais cette étude soupçonnait un retournement : les mesures en masse mêlent les signaux de nombreux types cellulaires. Lorsqu’ils ont examiné des coupes de tissu tumoral de patients, ils ont trouvé que la protéine COL4A6 était en fait fortement augmentée dans les cancers par rapport à l’estomac normal, et que les fibres de collagène devenaient plus épaisses et plus abondantes à mesure que les tumeurs progressaient.
Les fibroblastes, moteurs cachés
Grâce à l’imagerie fluorescente et au séquençage unicellulaire, les chercheurs ont découvert d’où provenait réellement COL4A6. Ce n’étaient pas les cellules cancéreuses elles‑mêmes, mais principalement un type de cellules de soutien appelées fibroblastes associés au cancer, ou CAF, nichés dans le tissu conjonctif tumoral. Les signaux de COL4A6 se chevauchaient étroitement avec un marqueur de CAF, révélant que ces fibroblastes en étaient la principale source. Cela explique la confusion initiale : tandis que les cellules épithéliales tumorales peuvent perdre l’expression génique de COL4A6, le compartiment fibroblastique augmente la production et dépose la protéine dans la matrice environnante, un schéma que les tests en masse brouillent.
Comment COL4A6 alimente la croissance et la dissémination
Pour tester l’effet de COL4A6 d’origine CAF sur les tumeurs, l’équipe a cultivé des cellules de cancer gastrique avec des cultures de fibroblastes modifiées pour produire soit plus, soit moins de COL4A6. Lorsque les fibroblastes surproduisaient COL4A6, les cellules cancéreuses voisines devenaient plus mobiles et invasives, et basculaient vers un état plus agressif et plasticien connu sous le nom de transition épithélio–mésenchymateuse. Chez la souris, les tumeurs formées avec des fibroblastes riches en COL4A6 étaient plus volumineuses, présentaient des dépôts de collagène plus denses et montraient de forts signaux de COL4A6 tissés dans le stroma. Dans le même temps, COL4A6 semblait agir sur les fibroblastes eux‑mêmes, réorganisant leur échafaudage interne en fibres de stress épaisses et augmentant les marqueurs classiques d’activation. En somme, COL4A6 aidait à convertir les fibroblastes en remodelleurs puissants qui rigidifient le tissu, construisent des barrières physiques et créent un niche favorisant l’invasion tumorale et la résistance aux médicaments.
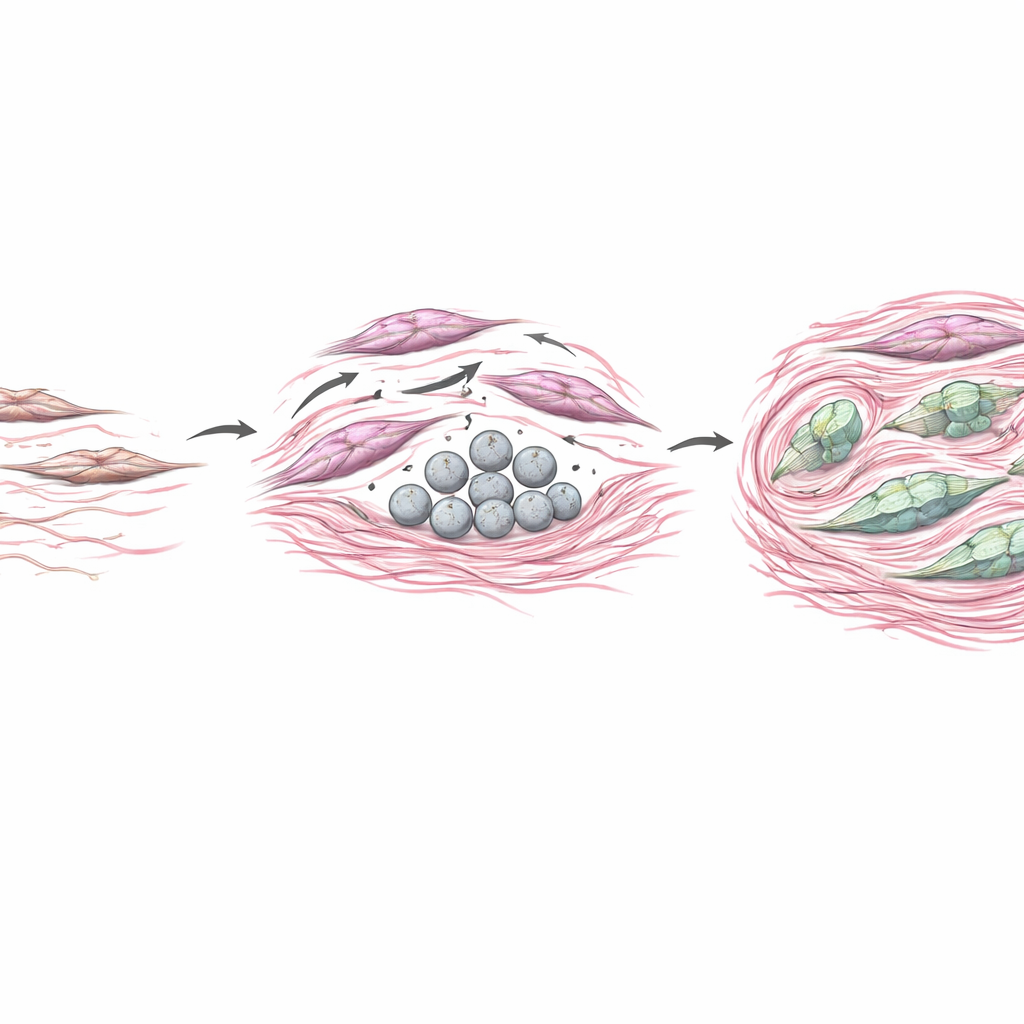
Ce que cela signifie pour les patients
Pour les non‑spécialistes, le message principal est que la même molécule peut paraître utile ou nuisible selon la façon et l’endroit où elle est mesurée. COL4A6 peut sembler « protectrice » lorsqu’elle est moyennée sur toutes les cellules d’une tumeur, mais, examinée dans le bon compartiment, elle apparaît comme un promoteur clé de la maladie, produite par des fibroblastes activés qui construisent un environnement dense et hostile. En définissant des sous‑types tumoraux basés sur la matrice et en révélant cet axe CAF–COL4A6 comme un moteur d’évasion immunitaire et de résistance à la chimiothérapie, l’étude suggère de nouvelles façons de stratifier les patients atteints de cancer gastrique et met en évidence le stroma tumoral comme une cible prometteuse. Des thérapies visant à perturber COL4A6 dans les fibroblastes ou à assouplir la matrice environnante pourraient un jour aider à transformer des tumeurs gastriques froides et résistantes en tumeurs plus sensibles aux médicaments et à l’immunothérapie.
Citation: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
Mots-clés: cancer gastrique, microenvironnement tumoral, fibroblastes associés au cancer, matrice extracellulaire, COL4A6