Clear Sky Science · it
COL4A6 arricchito nei CAF promuove la progressione del cancro gastrico e il rimodellamento stromale nonostante un’associazione inversa nei trascrittomi in blocco
Perché l’ambiente intorno al tumore conta
La maggior parte delle persone pensa al cancro come a una malattia delle cellule ribelli, ma questo studio mostra che il “terreno” intorno al tumore può essere altrettanto importante delle cellule neoplastiche stesse. Nel cancro gastrico, l’impalcatura tissutale e le cellule di supporto che circondano il tumore possono rallentare la malattia oppure favorirne la crescita, la diffusione e la resistenza alle terapie. Questa ricerca svela come una specifica proteina della matrice, chiamata COL4A6, si comporti in modo molto diverso a seconda del luogo in cui si trova, e come un particolare gruppo di cellule di supporto, i fibroblasti associati al cancro, possa trasformare questa proteina in un potente complice della progressione tumorale.
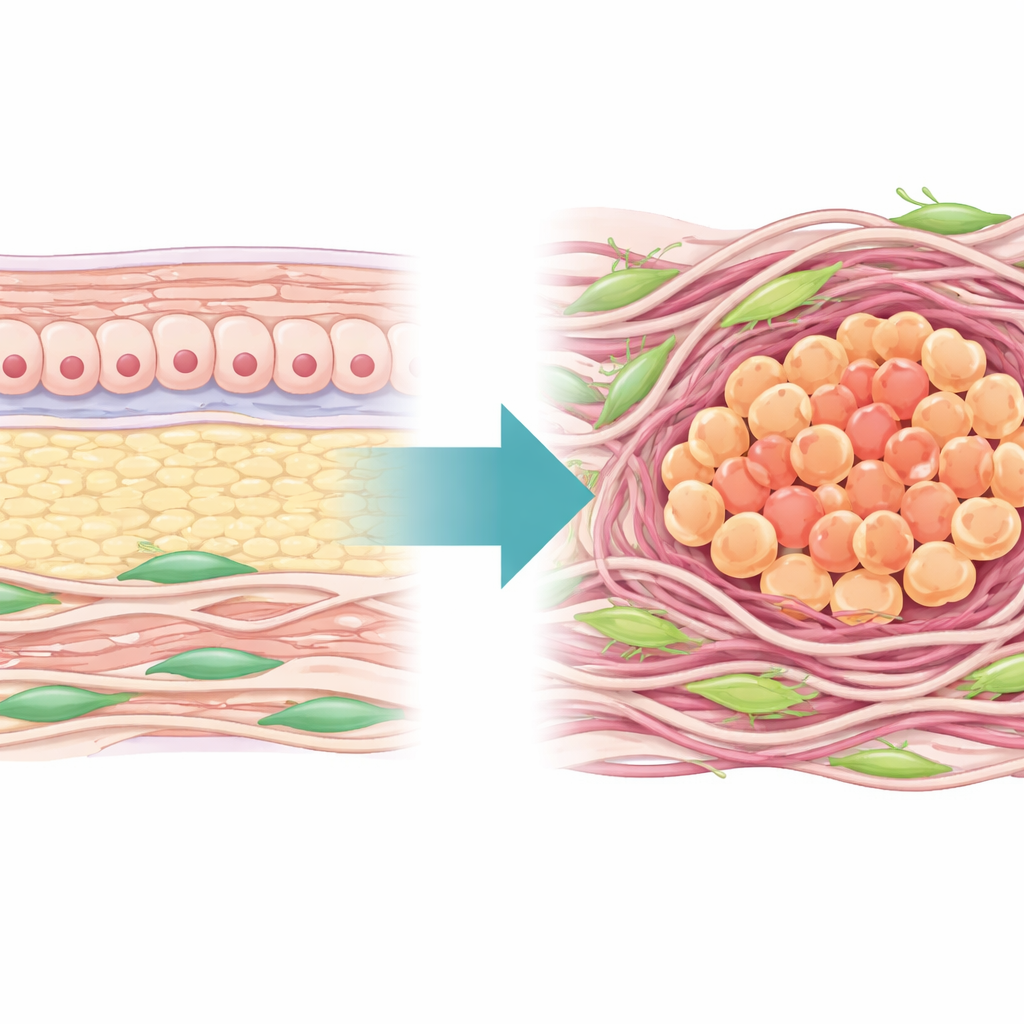
Uno sguardo più ravvicinato al quartiere tumorale
Gli autori hanno iniziato mappando il “paesaggio” della matrice extracellulare — la rete di proteine e fibre che circonda le cellule — in centinaia di tumori gastrici umani. Hanno scoperto che quasi la metà dei geni fondamentali della matrice era alterata nel tessuto tumorale rispetto al tessuto normale adiacente, confermando che l’ambiente fisico dei tumori gastrici subisce un marcato rimodellamento. Sulla base di questi geni hanno costruito un Matrisome Risk Score in grado di distinguere in modo affidabile il tumore dal tessuto normale e di separare i pazienti in due gruppi principali: uno con una matrice densa e altamente rimodellata e una sopravvivenza peggiore, e un altro con una matrice più lassa e risultati migliori. Il gruppo con matrice densa mostrava anche segni di tumore “freddo” dal punto di vista immunitario, con molte cellule immunosoppressive e poche cellule T attive, oltre a una ridotta sensibilità alla chemioterapia standard.
Una proteina dalla doppia personalità
Un componente della matrice, COL4A6, ha attirato l’attenzione perché sembrava comportarsi come un fattore “protettivo” quando i ricercatori analizzavano soltanto i dati trascrittomici in blocco ottenuti da campioni tumorali interi. Statisticamente, livelli più alti del gene COL4A6 in questi dataset in blocco erano associati a un rischio apparente più basso, il che aveva indotto alcuni a sospettare che potesse contribuire a contenere il cancro. Ma lo studio ipotizzava una svolta nascosta: le misurazioni in blocco mescolano segnali provenienti da molti tipi cellulari diversi. Quando il team ha esaminato sezioni tessutali tumorali provenienti da pazienti, ha scoperto che la proteina COL4A6 era infatti fortemente aumentata nei tumori rispetto al tessuto gastrico normale, e che le fibre di collagene diventavano più spesse e più abbondanti con l’avanzare del tumore.
I fibroblasti come motori nascosti
Usando immagini fluorescenti e sequenziamento a singola cellula, i ricercatori hanno identificato la vera provenienza di COL4A6. Non erano le cellule cancerose stesse, bensì principalmente un tipo di cellule di supporto chiamate fibroblasti associati al cancro, o CAF, annidate nel tessuto connettivo tumorale. I segnali di COL4A6 si sovrapponevano strettamente a un marcatore dei CAF, rivelando che questi fibroblasti erano la fonte principale. Questo ha spiegato la confusione iniziale: mentre le cellule epiteliali neoplastiche possono perdere l’espressione di COL4A6 a livello genico, il compartimento dei fibroblasti aumenta la produzione e deposita la proteina nella matrice circostante, uno schema che le analisi in blocco tendono a mescolare e a nascondere.
Come COL4A6 alimenta crescita e diffusione
Per valutare come COL4A6 derivato dai CAF influisca sui tumori, il team ha coltivato cellule di cancro gastrico insieme a colture di fibroblasti ingegnerizzate per produrne di più o di meno. Quando i fibroblasti sovraproducevano COL4A6, le cellule tumorali vicine diventavano più mobili e invasive, e si spostavano verso uno stato più aggressivo e plastico noto come transizione epitelio-mesenchimale. Nei topi, i tumori formatisi con fibroblasti ricchi di COL4A6 crescevano di più, presentavano depositi di collagene più densi e mostravano forti segnali di COL4A6 distribuiti nello stroma. Allo stesso tempo, COL4A6 sembrava agire anche sui fibroblasti stessi, riorganizzando il loro impalcatura interna in spessi stress fiber e potenziando marcatori classici di attivazione. In sostanza, COL4A6 contribuiva a trasformare i fibroblasti in potenti rimodellatori che irrigidiscono il tessuto, costruiscono barriere fisiche e creano una nicchia che favorisce l’invasione tumorale e la resistenza ai farmaci.
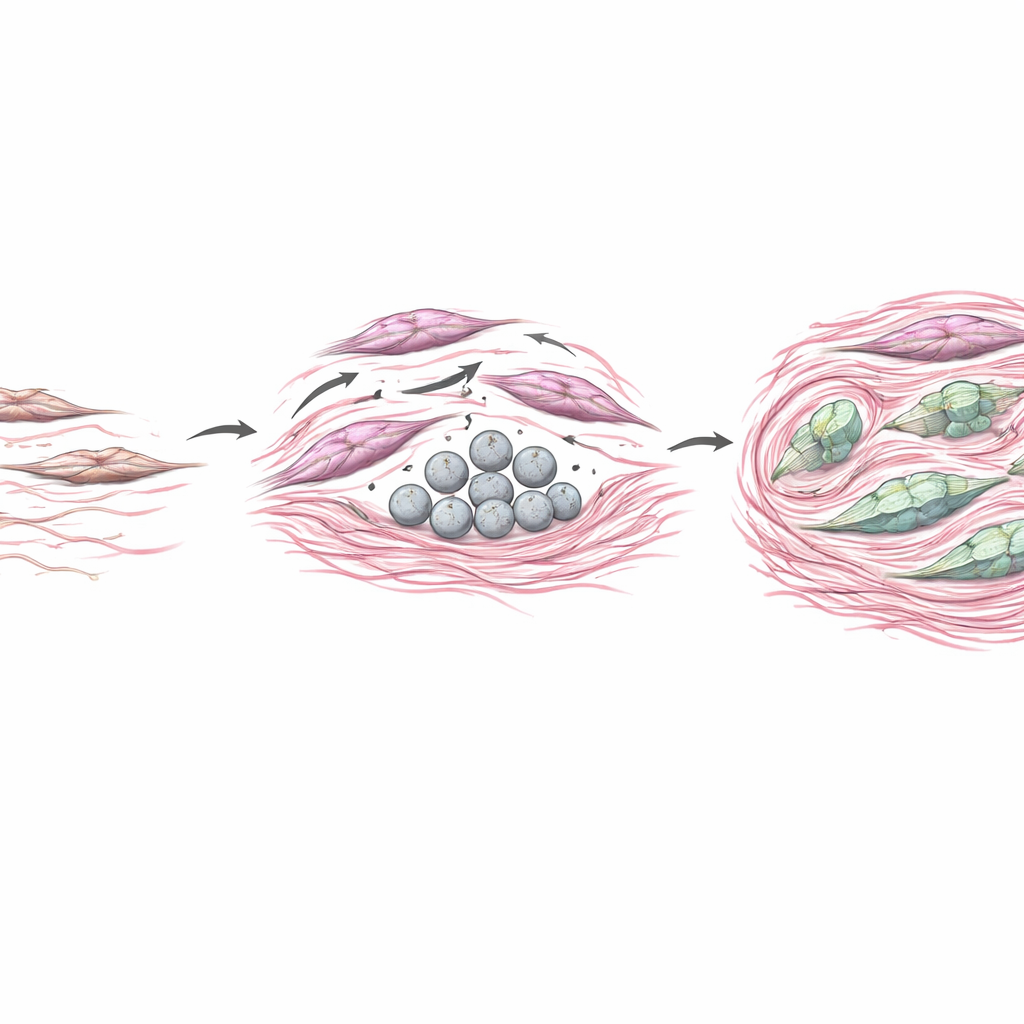
Cosa significa per i pazienti
Per i non specialisti, il messaggio principale è che la stessa molecola può apparire utile o dannosa a seconda di come e dove viene misurata. COL4A6 può sembrare “protettiva” quando viene mediata su tutte le cellule di un tumore, ma se osservata nel compartimento corretto emerge come un promotore chiave della malattia, prodotta da fibroblasti attivati che costruiscono un ambiente denso e ostile. Definendo sottotipi tumorali basati sulla matrice ed esponendo questo asse CAF–COL4A6 come motore di elusione immunitaria e resistenza alla chemioterapia, lo studio suggerisce nuovi modi per stratificare i pazienti con cancro gastrico e mette in luce lo stroma tumorale come un bersaglio promettente. Terapie che interrompano COL4A6 nei fibroblasti o ammorbidiscano la matrice circostante potrebbero un giorno aiutare a trasformare tumori gastrici “freddi” e resistenti ai trattamenti in tumori più sensibili a farmaci e immunoterapia.
Citazione: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
Parole chiave: cancro gastrico, microambiente tumorale, fibroblasti associati al cancro, matrice extracellulare, COL4A6