Clear Sky Science · de
CAF-angereicherte COL4A6 fördert das Fortschreiten von Magenkrebs und die Umgestaltung des Stromas trotz inverser Assoziation in Bulk-Transkriptomen
Warum die Umgebung des Tumors zählt
Die meisten Menschen denken bei Krebs an entartete Zellen, doch diese Studie zeigt, dass der „Boden“ um den Tumor ebenso wichtig sein kann wie die Krebszellen selbst. Beim Magenkrebs können das Gewebegerüst und die umgebenden Stütz‑ und Hilfszellen das Fortschreiten der Krankheit entweder bremsen oder begünstigen, ihr Wachstum, ihre Ausbreitung und ihre Therapie‑Resistenz fördern. Diese Arbeit legt offen, wie ein bestimmtes Gerüstprotein namens COL4A6 je nach seinem Aufenthaltsort sehr unterschiedlich wirkt und wie eine bestimmte Gruppe von Stützzellen, die krebsassoziierten Fibroblasten, dieses Protein in einen starken Mitspieler der Tumorprogression verwandeln können.
Ein genauerer Blick auf die Tumornachbarschaft
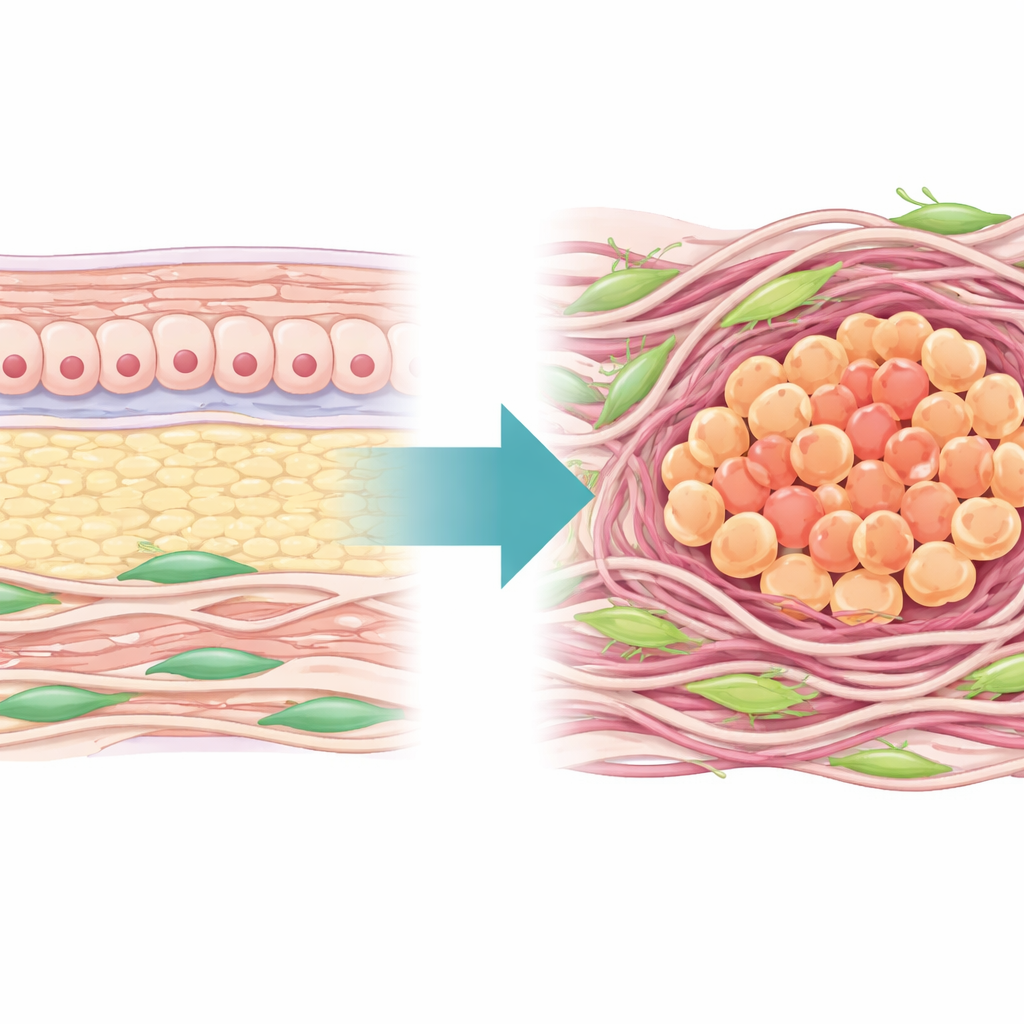
Die Autorinnen und Autoren begannen damit, die „Landschaft“ der extrazellulären Matrix — das Netzwerk aus Proteinen und Fasern, das Zellen umgibt — in Hunderten menschlicher Magentumoren zu kartieren. Sie fanden heraus, dass nahezu die Hälfte der Kernmatrix‑Gene in Tumorgewebe im Vergleich zum angrenzenden normalen Gewebe verändert war, was bestätigt, dass die physikalische Umgebung von Magentumoren stark umgebaut wird. Auf Basis dieser Gene entwickelten sie einen Matrisome‑Risikoscore, der Tumor- und Normalgewebe zuverlässig unterscheiden und Patientengruppen in zwei Hauptkategorien einteilen konnte: eine mit dichter, stark umgestalteter Matrix und schlechterer Überlebensrate sowie eine mit lockererer Matrix und besseren Ergebnissen. Die Gruppe mit hoher Matrix zeigte außerdem Merkmale eines immunologisch „kalten“ Tumors, mit vielen unterdrückenden Zellen, wenigen aktiven T‑Zellen und verminderter Ansprechbarkeit auf Standard‑Chemotherapien.
Ein Protein mit geteiltem Charakter
Ein Matrixbestandteil, COL4A6, fiel auf, weil er in den Auswertungen aus Bulk‑Genexpressionsdaten scheinbar wie ein „schützender“ Faktor wirkte. Statistisch waren höhere COL4A6‑Genlevel in diesen Gesamtdatensätzen mit geringerem scheinbarem Risiko assoziiert, weshalb einige vermuteten, es könnte krebshemmend sein. Die Studie vermutete jedoch einen verborgenen Dreh: Bulk‑Messungen vermischen Signale vieler Zelltypen. Bei der Untersuchung tatsächlicher Tumorschnitte von Patientinnen und Patienten zeigte sich, dass das COL4A6‑Protein in Wirklichkeit in Krebsgewebe deutlich erhöht war im Vergleich zum normalen Magenschleimhautgewebe und dass Kollagenfasern mit Tumorprogression dicker und häufiger wurden.
Fibroblasten als verborgene Treiber
Mithilfe fluoreszenzbasierter Bildgebung und Einzelzellsequenzierung fanden die Forschenden heraus, woher COL4A6 tatsächlich stammte. Es kamen nicht primär die Krebszellen selbst in Frage, sondern vor allem eine Art Stützzellen, die krebsassoziierten Fibroblasten (CAFs), die im Bindegewebe des Tumors liegen. COL4A6‑Signale überlappten stark mit einem CAF‑Marker, was zeigte, dass diese Fibroblasten die Hauptquelle sind. Das erklärt die frühere Verwirrung: Während tumoröse epithelialen Zellen auf Genebene möglicherweise COL4A6 verlieren, fährt die Fibroblastenpopulation die Produktion hoch und lagert das Protein in der umgebenden Matrix ab — ein Muster, das Bulk‑Tests verwischt.
Wie COL4A6 Wachstum und Ausbreitung antreibt
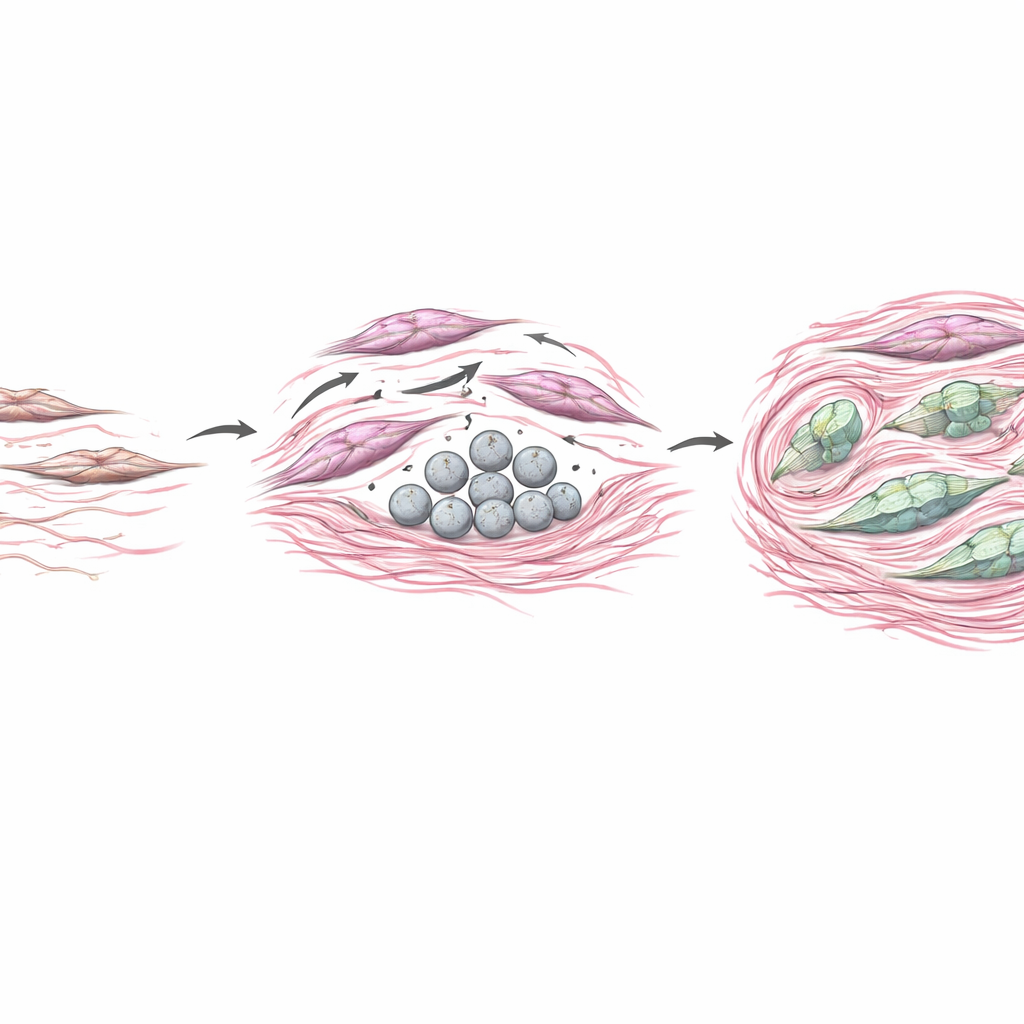
Um zu testen, wie CAF‑abgeleitetes COL4A6 Tumoren beeinflusst, kultivierte das Team Magenkrebszellen zusammen mit Fibroblasten, die so verändert waren, dass sie mehr oder weniger COL4A6 produzierten. Wenn Fibroblasten COL4A6 überproduzierten, wurden benachbarte Krebszellen beweglicher und invasiver und gingen in einen aggressiveren, formverändernden Zustand über, der als epithelial–mesenchymale Transition bekannt ist. In Mausmodellen wuchsen Tumoren, die von COL4A6‑reichen Fibroblasten begleitet wurden, größer, wiesen dichtere Kollagenablagerungen auf und zeigten starke COL4A6‑Signale, die sich durch das Stroma zogen. Gleichzeitig schien COL4A6 auch rückwirkend auf die Fibroblasten zu wirken, deren internes Zytoskelett in dicke Stressfasern umorganisiert wurde und klassische Aktivierungsmarker erhöht waren. Im Kern half COL4A6 dabei, Fibroblasten in kraftvolle Umgestalter zu verwandeln, die das Gewebe versteifen, physische Barrieren aufbauen und eine Nische schaffen, die Tumorinvasion und Medikamentenresistenz fördert.
Was das für Patientinnen und Patienten bedeutet
Für Nicht‑Fachleute lautet die Hauptbotschaft: Dasselbe Molekül kann je nach Messkontext hilfreich oder schädlich erscheinen. COL4A6 mag in Durchschnittsmessungen über alle Zellen eines Tumors hinweg „schützend“ wirken, aber wenn man es im richtigen Kompartiment betrachtet, entpuppt es sich als zentraler Förderer der Erkrankung, produziert von aktivierten Fibroblasten, die eine dichte, feindliche Umgebung aufbauen. Indem die Studie matrixbasierte Tumorsubtypen definiert und diese CAF–COL4A6‑Achse als Treiber von Immunflucht und Chemotherapie‑Resistenz offenlegt, werden neue Möglichkeiten zur Stratifizierung von Magenkrebspatienten vorgeschlagen und das Tumorstroma als vielversprechendes Ziel hervorgehoben. Therapien, die COL4A6 in Fibroblasten stören oder die umgebende Matrix auflockern, könnten eines Tages helfen, kalte, therapieresistente Magentumoren in solche zu verwandeln, die besser auf Medikamente und Immuntherapien ansprechen.
Zitation: Sun, Q., Wei, S., Yao, J. et al. CAF-enriched COL4A6 promotes gastric cancer progression and stromal remodeling despite an inverse association in bulk transcriptomes. Sci Rep 16, 10399 (2026). https://doi.org/10.1038/s41598-026-38120-7
Schlüsselwörter: Magenkrebs, Tumormikroumgebung, krebsassoziierte Fibroblasten, extrazelluläre Matrix, COL4A6